J Med Chem: 双PROTAC来了:我国学者首次提出双重靶向降解(Dual PROTACs)药物设计新概念
2021-06-01 “E药世界”公众号 “E药世界”公众号
近日,华中科技大学同济药学院李华教授、周宜荣副教授和沈阳药科大学无涯创新学院陈丽霞教授作为共同通讯作者,在药物化学顶级期刊 Journal of Medicinal Chemistry 发表了题为:R
蛋白质水解靶向嵌合体(proteolysis targeting chimera, PROTAC)是一种双功能小分子,其中目标蛋白配基和E3泛素连接酶配基通过连接臂连在一起,与传统小分子抑制剂相比,PROTAC有着多种优势,包括无需与靶蛋白活性位点结合就能发挥作用、可以降解难于成药靶点、其作用是事件驱动而具有催化性质,可以在更低剂量下起作用,因此特别在抗癌药物的开发中具有巨大的潜力。

近日,华中科技大学同济药学院李华教授、周宜荣副教授和沈阳药科大学无涯创新学院陈丽霞教授作为共同通讯作者,在药物化学顶级期刊 Journal of Medicinal Chemistry 发表了题为:Rational Design and Synthesis of Novel Dual PROTACs for Simultaneous Degradation of EGFR and PARP 研究论文。
该研究创造性地提出双重靶向降解药物(Dual PROTACs)的设计新概念,以现有的EGFR抑制剂Gefitinib和PARP抑制剂Olaparib为原料,合成不同链接长度和不同E3连接酶(CRBN-和VHL-)招募的EGFR和PARP蛋白双重靶向降解嵌合分子(Dual PROTACss),在细胞水平成功地同时降解癌细胞内的EGFR和PARP蛋白,这是Dual PROTACs第一个成功的例子。

设计概念示意图:小龙女(Dual PROTACs)使出“左右互博”,以两种武功打败金轮法王(肿瘤)。图片来源:李华教授课题组
现代药物发现的基础是针对特定靶点开发高效、富有选择性的药物。在过去几十年中,一个药物一个靶点的理论对于指导单一病因疾病的药物研发取得了巨大的成功,特别是抗生素等针对特定单一病原体蛋白靶点的药物。然而,复杂的疾病如癌症或炎症性疾病,通常是多种因素相互作用的结果,涉及多个介导疾病病因的协同作用或多个受体的上调,以及它们之间信号网络的串扰。在癌症中,肿瘤细胞常常上调不同的促生长因子,这些因子可以独立发挥作用,也可以通过信号网络在细胞内相互促进。肿瘤细胞很容易通过上调替代因子或者转换促进增殖的信号通路而获得抗药性;因此,仅针对单一靶点的治疗具有局限性。
除了耐药性之外,单靶点治疗药物还会因为副作用和组织毒性等,导致疗效降低、病人生活质量下降。为了克服单靶点药物的不足,针对两个与疾病发展有关的不同途径进行联合用药,可以得到加合或协同效应,并降低耐药性,而且因为各个单药剂量的降低,减少了副作用,这已成为一种公认的有效方法。
另一种提高疗效的策略是设计融合两个或多个药效团的单一杂合分子,同时靶向两种或两种以上的抗肿瘤表位或靶点。这些杂合分子能够同时调节多个靶点或通路,因此通常具有更好疗效和较少的副作用。在过去十年里,这些杂合分子因为在治疗复杂疾病方面的优势获得了相当大的成功,逐渐成为联合用药的替代方法,这包括双特异性抗体和其他双靶点或多靶点小分子药物。
受双靶点药物,特别是双特异性抗体巨大成功的启发,李华教授等提出把PROTAC和双靶向的概念结合起来,制造能够同时降解两个完全不同通路靶点的双重靶向降解分子(Dual PROTACs),不但同时降解两个靶点,而且同时吸收PROTAC和双靶点药物的优势,有可能达到和双抗体类似疗效,并仍然相对保持小分子药物的优点。
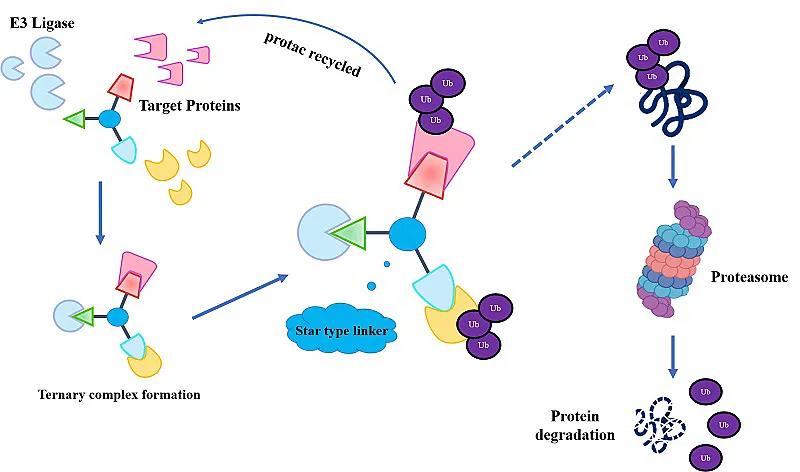
Dual PROTACs设计概念。图片来源:李华教授课题组
为了验证这个创新的概念,他们设计了具有两个不同“弹头”的双重靶向降解嵌合分子(Dual PROTACs),由一个E3配体(CRBN或VHL配基)同时连接两个完全不同类型(通路)靶点的抑制剂,实现了一个小分子同时降解肿瘤细胞中的两个完全不同的靶蛋白。他们以现有的EGFR抑制剂Gefitinib和PARP抑制剂Olaparib为原料,合成不同链接长度和不同E3连接酶(CRBN-和VHL-)招募的EGFR和PARP蛋白双重靶向降解嵌合分子(Dual PROTACss),在细胞水平成功地同时降解癌细胞内的EGFR和PARP蛋白,这是Dual PROTACs第一个成功的例子。
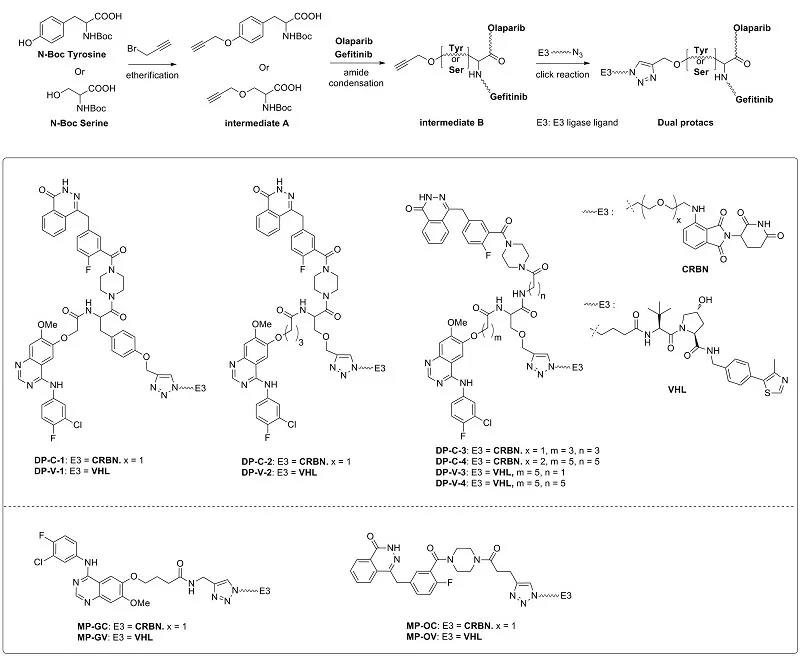
Dual PROTACs分子结构与合成。图片来源:J. Med. Chem.
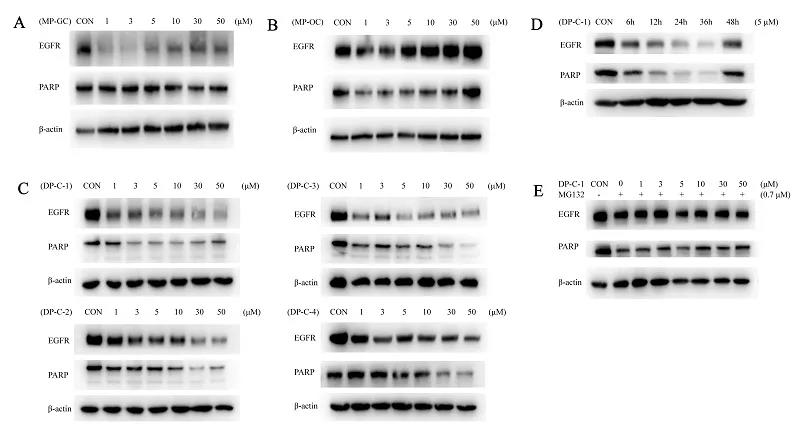
Dual PROTACs在细胞水平同时降解癌细胞内EGFR和PARP。图片来源:J. Med. Chem.
本研究还创造性地利用生物相容性的氨基酸作为连接骨架,快速实现了双靶向三体化合物的合成。本研究创立的技术和方法可以很容易稍作改变用于更多双靶向PROTAC分子的合成,极大地拓展了PROTAC技术的应用,打开了一个全新的药物发现领域。
目前在临床上两个不同靶点抑制剂联合用药的治疗方案,甚至有些双特性抗体的治疗,都可以运用本研究的策略设计相应的单个Dual PROTACs分子进行双靶向降解而替代,而起到相同的、甚至更好的疗效。
在癌症联合治疗的领域中,Dual PROTACs可以很快地应用,例如可以设计两个合成致死激酶抑制剂的Dual PROTACs,肿瘤免疫靶点加辅助免疫靶点、激酶靶点、或能量代谢靶点的Dual PROTACs,表观遗传靶点加抗凋亡靶点的Dual PROTACs等。
当然,Dual PROTACs除了有上述显而易见的优点外,但因为分子量增大,会使它在成药性和药代动力学方面带来一定的问题。要解决这些问题可能有两个方向,一个方向是纳米载药系统进行递送以改善药物的吸收,另一个方向就是想办法简化抑制剂部分,保留最小药效团。这些都值得进一步研究。
华中科技大学同济药学院博士后郑梦竹、研究助理霍峻锋、博士生顾小霞为共同第一作者,华中科技大学同济药学院李华教授、周宜荣副教授和沈阳药科大学无涯创新学院陈丽霞教授为共同通讯作者。
原始出处:
Mengzhu Zheng, et al. Rational Design and Synthesis of Novel Dual PROTACs for Simultaneous Degradation of EGFR and PARP. J. Med. Chem. 2021.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









好弔的文章
100
#PROTAC#
95
#药物设计#
64
#TAC#
57
#我国学者#
76
#PROTACs#
39
#ACS#
46
#PRO#
40
#Med#
58