
9月8日晚间,据科技新闻网站STAT独家报道称,英国阿斯利康(AstraZeneca)和牛津大学正在开发的一款新冠疫苗(AZD1222)的大规模三期临床试验已被搁置,因为英国的一名参与者似乎出现了严重的不良反应。
阿斯利康公司的在一份声明中表示,公司的 "标准审查程序触发了疫苗接种的暂停,以便审查安全数据"。阿斯利康在后续声明中表示,它启动了研究暂停,而非监管机构下令。公司声明指出,在大型实验中,偶然有出现不良反应的情况,必须独立谨慎检查。严重不良反应可能是出现需要住院的问题,也可能构成生命威胁或死亡。公司声明还说,阿斯利康正在努力加快对单个事件的审查,以最大程度地减少对临床研究时间表的任何潜在影响。
据一位知情人士透露,该不良反应的性质和发生的时间并不立即知晓,不过参与者有望康复。该起严重不良反应触发事件对阿斯利康其他疫苗的临床实验以及其他疫苗制造商的临床实验产生影响,疫苗生产商正在寻找类似反应的迹象。
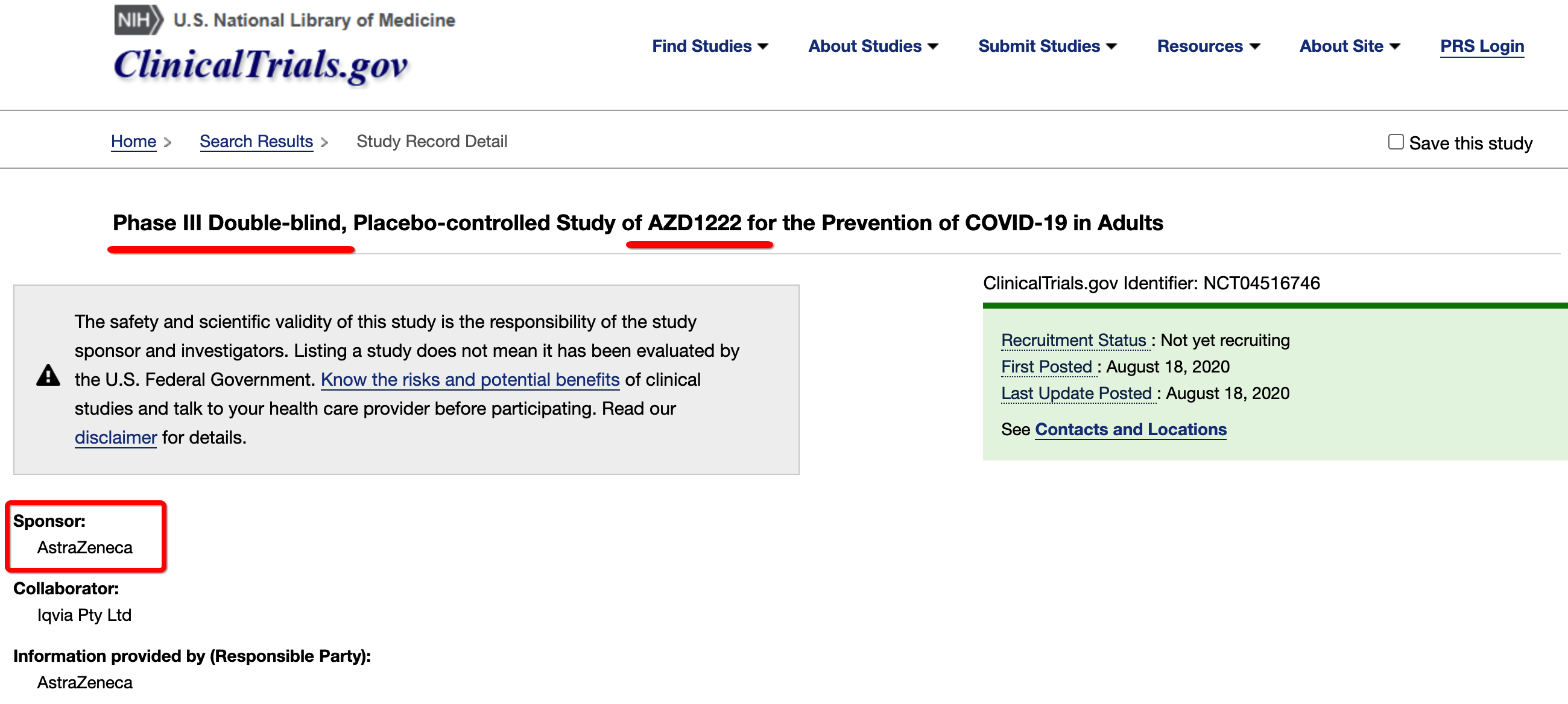
阿斯利康新冠疫苗三期临床试验https://clinicaltrials.gov/ct2/show/NCT04516746
阿斯利康AZD1222开发时间线:
l 3月27日:牛津大学开始招募患者进行安慰剂对照试验,该试验将招募510名健康志愿者。 该大学表示,这种疫苗将在数周之内准备就绪。
l 4月30日:阿斯利康宣布将与牛津大学合作开发疫苗。
l 7月20日:牛津大学发布了1/2期数据,证明了具有轻度至中度副作用的免疫反应。
l 8月31日:阿斯利康开始参与美国的第3期试验,该试验将有30000名志愿者参加。
l 9月8日:阿斯利康表示,涉嫌不良反应的暂停三期临床试验
报道指出,临床试验搁置并不罕见,目前还不清楚阿斯利康的临床搁置可能会持续多久。但鉴于迫切需要新的方法来遏制全球流行病,该公司的试验进展以及所有在研的新冠疫苗的进展受到密切关注。
虽然目前尚不清楚不良事件的严重程度和罕见程度,但这一发现可能会影响英国试验的有效性数据的获得速度。这些数据被认为是寻求美国食品和药物管理局对这种疫苗进行紧急使用授权的任何提议的组成部分,并有可能危及特朗普总统在11月大选之前快速追踪该疫苗的努力。
阿斯利康8月下旬才开始在美国进行3期试验。根据政府登记处clinicaltrials.gov的数据,美国的试验目前在全国62个地点进行,不过有些地方还没有开始招募参与者。此前在英国、巴西和南非也开始了2/3期试验。目前也不清楚该起不良反应发生在哪项临床试验中,不过一个明确的可能性是英国正在进行的2/3期试验。
在7月《柳叶刀》上发表的1/2期研究显示,接种疫苗的1000名参与者中约有60%出现了副作用。所有的副作用,包括发烧,头痛,肌肉疼痛和注射部位反应,均被视为轻度或中度。在研究过程中,所报告的所有副作用也均消失了。

https://www.hopkinsmedicine.org/
据《纽约时报》援引一位熟悉情况的人士的报道称,该不良反应参与者患有横贯性脊髓炎,这是一种影响脊髓的炎性综合征,通常是由病毒感染引起的。但该病是否与阿斯利康疫苗直接相关尚不清楚,阿斯利康拒绝对此报道发表评论。
目前全球有9种候选疫苗正在进行3期试验。阿斯利康新冠疫苗成为全球首个暂停的三期疫苗试验。

布朗大学的Ashish Jha博士在Twitter上表示,中断的重要性尚不清楚,但他“仍然乐观”认为在未来几个月内将找到有效的疫苗。他写道:“但是乐观并不是证据。” “让科学来推动这一过程。”
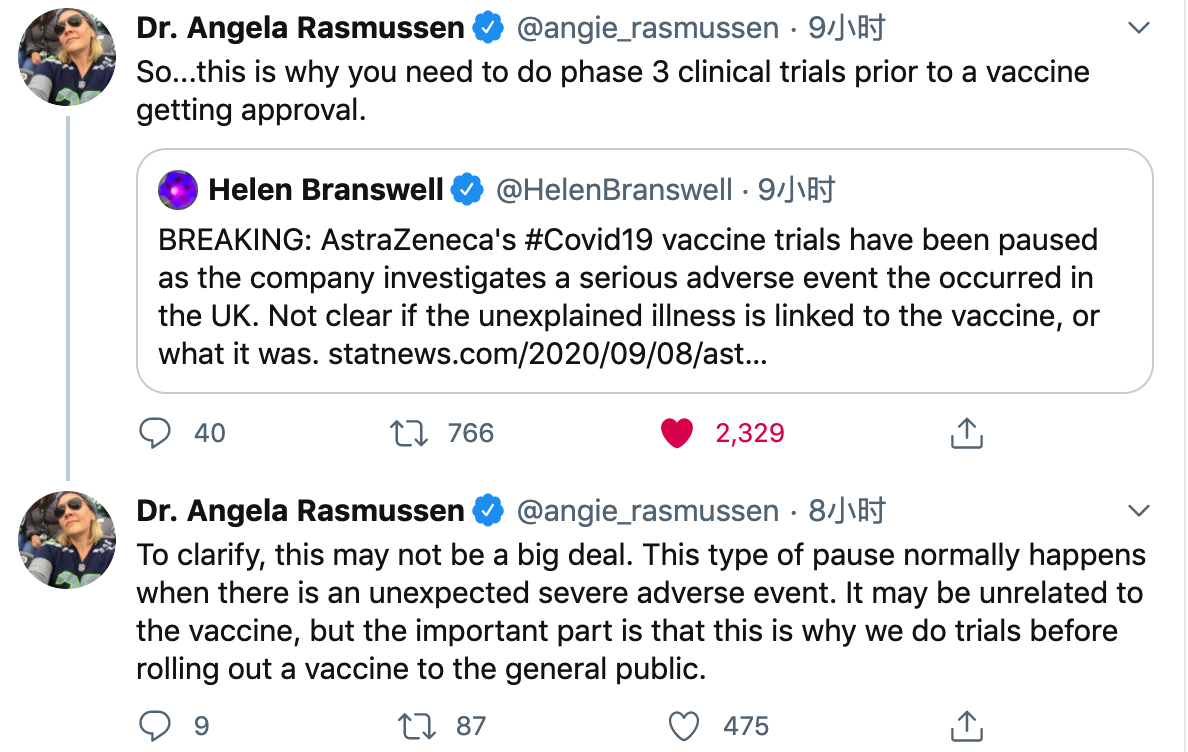
纽约哥伦比亚大学的病毒学家安吉拉·拉斯穆森(Angela Rasmussen)发推文说,疾病可能与疫苗无关,“但重要的是,这就是我们在向公众推出疫苗之前进行试验的原因。”

阿斯利康官方推特支持9家药企发起的“坚持科学”承诺
8日早些时候,阿斯利康与BioNTech,Moderna,辉瑞,Novavax,赛诺菲,葛兰素史克,强生和默克等8家制药公司签署了一项承诺书,宣布在疫苗研发过程中,不会仓促推出疫苗,坚持疫苗的科学安全和功效标准。
宣布此消息之前,人们担心美国总统特朗普将向美国FDA施压,要求其在证明安全有效之前批准疫苗。美国已投入数十亿美元,以快速开发针对新冠的多种疫苗。但是公众担心疫苗不安全或无效会带来灾难性的后果。根据最新的《今日美国》 /萨福克民意调查显示,三分之二的美国选民表示,他们不会立即尝试获得冠状病毒疫苗,而四分之一的选民表示他们永远都不会想要获得新冠病毒疫苗。
据报道,宣布试验暂停后,阿斯利康在美国上市的股票在盘后交易中下跌了6%以上,在常规交易中上涨了2.1%,报收于54.71美元。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#不良反应#
39
#三期临床#
42
#三期临床试验#
36
疫苗研制势在必行!
88
#牛津大学#
30
新冠肺炎,疫情何时才能消失
52
机制研究离临床仍然有距离,不过与临床结合思考,仍然有帮助的,不能仅仅是纯临床思维,转化思维同样重要
55
失败是成功之母
145
emmmm...噩耗...中国疫苗坚持住了..
153
学习
113