真实世界证据支持药物研发审评,这四点思考值得关注!
2020-01-11 朱晶 E药经理人
1月7日,国家药监局把2020年的一号文件,留给了此前就备受行业关注的真实世界证据支持药物研发与审评。 在其官网上,药监局同时公布了《真实世界证据支持药物研发与审评指导原则(试行)》,以及该文件的起草说明。作为国内发布的首个真实世界证据支持药物研发与审评的指导文件,这被视为新药研发审评道路上的里程碑事件,并迅速引起了行业的密切关注。事实上,如何利用真实世界证据评价药物的有效性和安全性
1月7日,国家药监局把2020年的一号文件,留给了此前就备受行业关注的真实世界证据支持药物研发与审评。 在其官网上,药监局同时公布了《真实世界证据支持药物研发与审评的指导原则(试行)》,以及该文件的起草说明。作为国内发布的首个真实世界证据支持药物研发与审评的指导文件,这被视为新药研发审评道路上的里程碑事件,并迅速引起了行业的密切关注。
事实上,如何利用真实世界证据评价药物的有效性和安全性,早已经成为国内外药物研发和监管决策中日益关注的热点问题。这是基于一个行业现状,即随机对照临床试验(RCT)虽然被认为是评价药物安全性和有效性的金标准,但其研究结论外推于临床实际应用时可能会面临挑战,或者存在传统的药物临床试验可能难以实施或需高昂的时间成本等问题。关于真实世界证据的研究也就应运而生。
这一点国外进行的显然更早。2016年12月,美国颁布《21世纪治愈法案》,要求FDA在医疗产品审评和监管程序中纳入真实世界证据(Real-World Evidence, RWE),而自此之后,美国市场也已有产品借此而获批,例如去年辉瑞的乳腺癌药物爱博新基于真实世界证据而被获批用于男性乳腺癌治便被认为是目前真实世界证据在药品研发上市中代表性的案例。
而中国则是在2018年8月,吴阶平医学基金会和中国胸部肿瘤研究协作组发布了《2018年中国真实世界研究指南》。国家药监局正式启动相关指导原则的起草工作则是在2018年的11月,经数次研讨后,2019年5月,CDE发布了《真实世界证据支持药物研发的基本考虑》(意见稿),于2019年5—8月广泛征求意见,并收到千余条反馈意见。在此基础上,《真实世界证据支持药物研发与审评的指导原则(试行)》才正式形成。
01 何为真实世界研究?
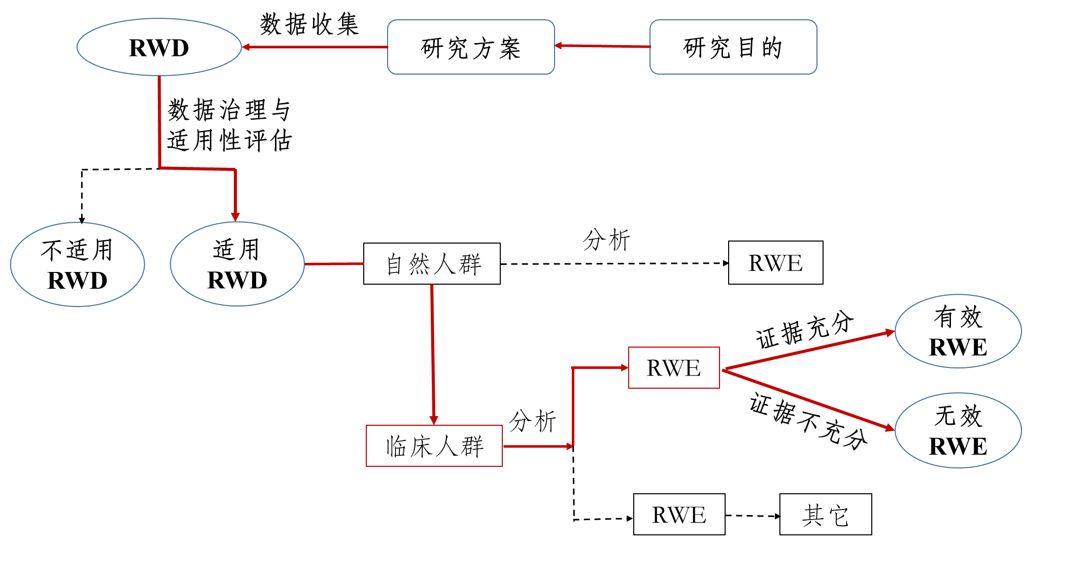
真实世界研究是指针对预设的临床问题,在真实世界环境下收集与研究对象健康有关的数据(真实世界数据)或基于这些数据衍生的汇总数据,通过分析,获得药物的使用情况及潜在获益-风险的临床证据(真实世界证据)的研究过程。
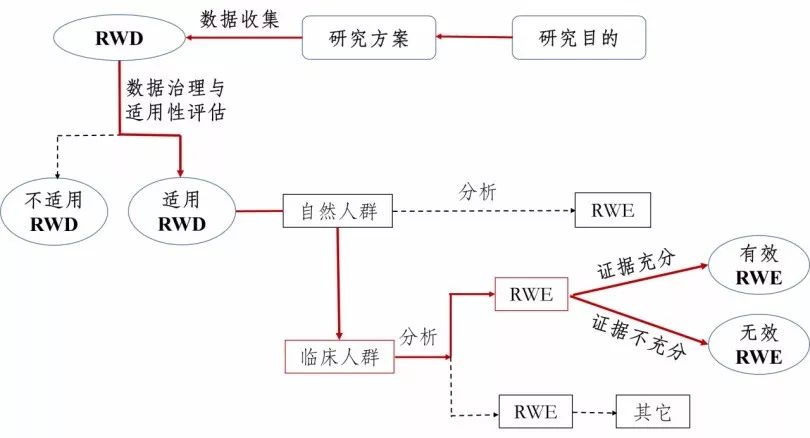
与真实世界证据对应的是随机对照试验(RCT),RCT一般被认为是评价药物安全性和有效性的金标准,并为药物临床研究普遍采用。曾经一位专家举了个生动的例子来描述RWS与传统RCT的关系:RCT是在一个理想状态下钓鱼,比如一个鱼塘或者一个网箱,这是一个高度控制的人工环境;而真实世界研究是在现实中钓鱼,是真实的江河湖泊,这是自然环境。
02 这些领域将显著受益
之所以一经发布便引发行业密切关注,很大程度上在于关于真实世界证据的研究,将在很大程度上给接下来药物的研发、审评以及药物的监管政策带来新的思路。

(一)为新药注册上市提供有效性和安全性的证据;
显而易见,该指导原则对中药来说有非凡的意义。对于中药,用观察性研究代替一期二期研究,提出研发路径,弥补历史数据的缺失。
在业内人士看来,在中药注射剂等在临床面临存在安全性信息有限、疗效结论外推不确定、用药方案未必最优、经济学效益缺乏等不足的挑战之时,利用真实世界数据进行更全面的评估,可以得到充分的临床证据。
实际上,在此前还处于RWS(真实世界研究)阶段时,已经有相当多的国内中药企业开始了相关的尝试。例如,2015年贵州益佰制药推动的全球首个抗肿瘤药艾迪注射液的10万例真实世界临床研究启动;2016年12月,安徽九方制药的葛酮通络胶囊10万例真实世界研究项目启动;以及翔宇药业的蒲苓盆炎康颗粒、上海和黄药业的生脉注射液、步长制药的脑心通胶囊等均开展了RWS项目。
从数据上来看,来自中国的研究登记逐年上升。据ClinicalTrials数据不完全统计,以“Real world”相关关键词登记在册的研究达到 1700 多项,其中来自中国的研究登记超过180 项,涉及肿瘤、心血管、内分泌、肝病和不良药物事件等多个领域。且据该数据研究完成时间预计2018—2022年将出现真实世界研究结论发布的井喷。
03 这四点思考仍值得关注
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












学习
83
#真实世界#
38
#研发#
37
#药物研发#
29