药品研发 1、默沙东宣布,其重磅抗PD-1疗法Keytruda,在治疗高风险早期三阴性乳腺癌(TNBC)的关键性3期临床试验中获得积极结果。试验结果显示,中位随访时间为39个月时,与化疗-安慰剂方案相比,Keytruda治疗方案将EFS事件风险降低了37%。 药品审批 1、强生旗下杨森宣布,美国FDA批准Darzalex Faspro联合泊马度胺和地塞米松,用于治疗既往接受过至少一种前期治疗的多发性骨髓瘤成人患者。 1、阿斯利康重磅PD-L1抑制剂度伐利尤单抗(商品名:英飞凡)的新适应症申请已在中国获批。据悉,度伐利尤单抗本次获批用于广泛期小细胞肺癌的一线治疗。 1、英国MHRA对默克靶向抗癌药Tepmetko(tepotinib)治疗携带MET基因14号外显子跳过改变的晚期非小细胞肺癌患者发表了积极的科学意见。
2、武田在欧洲过敏和临床免疫学联合大会期间公布了显示Takhzyro疗效更具持久性的数据。在这项3期长期扩展试验中,接受武田Takhzyro治疗的患者在长达2.5年的时间内,保持了其最初的疗效和安全性。并且数据还显示,患者症状发作减少的情况,在患人口统计学和疾病特征上呈现出一致的结果。
3、礼来与BAI宣布达成一项战略研究合作,开展抗β淀粉样蛋白抗体donanemab的3期预防试验。这是一项随机、双盲、安慰剂对照研究,将入组有风险发生与阿尔茨海默病相关的认知和功能下降的试验参与者,评估donanemab治疗是否能延缓试验参与者AD的临床进展。
4、Affinivax和安斯泰来公布,其联合开发的创新肺炎球菌疫苗ASP3772在2期临床试验中获得积极结果。结果表明,ASP3772具有良好的耐受性。此外,ASP3772激发针对24种肺炎球菌多糖抗原的抗体反应,对疫苗呈现的2种保守肺炎球菌蛋白抗原也产生了抗体反应。
5、Alexion公布了评估Ultomiris治疗全身型重症肌无力成人患者3期演的阳性顶线结果。数据显示,研究达到了主要终点:在治疗第26周,重症肌无力-日常生活能力量表总评分较基线的变化有高度的统计学意义,并且对于迄今为止已完成26周扩展研究的患者子集,总共治疗52周后仍保持阳性疗效。
6、Galectin Therapeutics公布了一项belapectin与Keytruda联合治疗黑色素瘤和头颈癌的1b期临床试验扩展队列的顶线临床数据。数据显示,在晚期难治性和进展性疾病患者中,belapectin与Keytruda联合治疗疗效显著:在黑色素瘤患者中,疾病控制率达到了56%,在头颈癌患者中DCR达到了40%。
7、Vir Biotechnology宣布,在慢性乙型肝炎病毒感染者中进行的2期MARCH临床试验已完成首例患者给药。该试验旨在研究其小干扰核糖核酸疗法VIR-2218,联合中和单克隆抗体疗法VIR-3434的疗效,目的是实现乙肝的功能性治愈。
8、Kymera Therapeutics宣布,其STAT3特异性靶向降解药物在治疗异常STAT3活化的外周T细胞淋巴瘤时显示出治疗潜力。临床前研究结果显示:STAT3降解剂在体外和体内均可导致ALK阳性间变性大细胞淋巴瘤,以及携带STAT3突变体的NK/T细胞淋巴瘤,和ALK阴性ALCL细胞系的生长停滞和细胞死亡增加。
9、Caribou Biosciences宣布,该公司开发的创新同种异体CAR-T疗法CB-010,在治疗复发/难治性B细胞非霍奇金淋巴瘤患者的1期临床试验中完成首例患者给药。
10、Hepion Pharmaceuticals宣布,在NASH患者中,其在研新型亲环素抑制剂CRV431的2a期AMBITION临床试验获得积极的顶线结果,达到试验的所有主要终点。试验中,相比安慰剂组,每日单次给药两种剂量的CRV431均显示出具有统计学意义的显著ALT降低。在28天内,患者血清的ALT下降了10%-15%。
11、Genocea Biosciences宣布,其在研外周T细胞疗法GEN-011在1/2a期临床试验中完成首例患者给药。
12、Sigilon Therapeutics血友病A细胞疗法SIG-001的首次人体试验遭遇挫折。1名受试者出现了严重并发症,随后FDA叫停了这项试验。
13、恒瑞医药宣布其自主研发的AR拮抗剂SHR3680的一项3期临床取得积极结果,联合雄激素剥夺疗法治疗高瘤负荷的mHSPC。研究结果表明,SHR3680可显著降低高瘤负荷的mHSPC患者的疾病进展或死亡风险。恒瑞将于近期向CDE递交上市前的沟通交流申请。
14、信达生物宣布其抗PD-1/CD137双特异性抗体的1a/1b期临床研究完成中国首例患者给药。该项研究主要目的为评估IBI319双特异性抗体治疗在标准治疗失败的晚期恶性肿瘤受试者中的安全性、耐受性和抗肿瘤活性。
15、基石药业公布了舒格利单抗用于一线治疗IV期非小细胞肺癌的临床研究最新结果。根据延长随访时间的数据,舒格利单抗联合化疗,呈现出了更长久的无进展生存期,高于去年8月公布的期中分析结果。
16、康方生物宣布,公司自主研发的肿瘤免疫治疗新药二代CD47单抗日前完成澳洲I期剂量爬坡试验,AK117在各个剂量爬坡队列受试者中均未发生DLT和未出现有临床意义的贫血,各队列受试者对药物耐受性良好,无需使用低剂量预激给药。
17、中国药物临床试验登记与信息公示平台显示,华东医药子公司中美华东制药、ImmunoGen等公司已在中国启动一项评估IMGN853治疗晚期卵巢癌患者的3期临床研究。
18、圣诺制药宣布,该公司候选药物STP705在用于预防瘢痕疙瘩的2期临床试验中完成首例患者给药。
2、美国FDA于14日发布无标题信,斥责安进对其Neulasta(pegfilgrastim,非格司亭)具有误导性的广告,可能会使医生感到困惑并阻碍相应低成本生物类似药的使用。
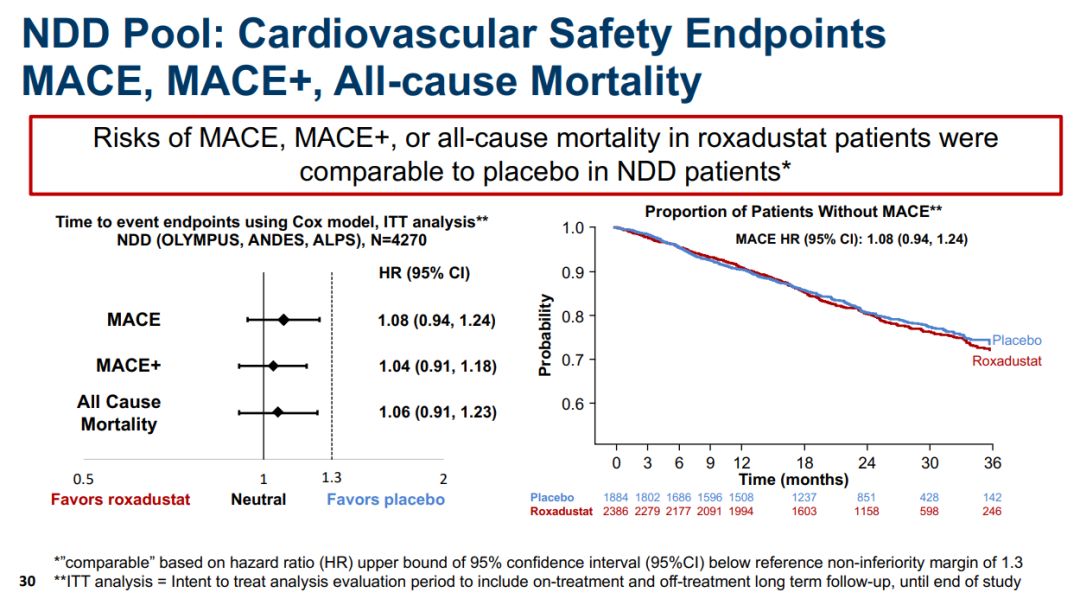
3、15日,美国FDA心血管和肾脏药物咨询委员会(CRDAC)投票反对批准珐博进/阿斯利康开发的口服HIF-PH抑制剂罗沙司他(Roxadustat)用于治疗慢性肾病贫血患者的上市申请,其中针对透析CKD贫血患者的投票结果为12:2,针对非透析CKD贫血患者的投票结果为13:1。该委员会的投票是基于一项包括8000多例患者的全球性III期临床项目数据。
4、FDA在一份关于已批准产品的潜在新安全问题的报告中指出Sprout的“女性伟哥”Addyi可能存在药物过敏的风险。该机构称,正在“评估监管行动的必要性”。
5、Alkeus Pharmaceuticals公司宣布,美国FDA已授予其维生素A衍生药物ALK-001突破性疗法认定,用于治疗眼底黄色斑点症。
6、开拓药业宣布福瑞他恩治疗雄激素性脱发的II期临床试验申请已获得美国FDA同意开展。
2、拜耳宣布copanlisib和利妥昔单抗联用创新疗法的上市申请已获CDE受理,适应症为惰性非霍奇金淋巴瘤的二线治疗。
3、CDE官网公示,武田口服小分子新药mobocertinib胶囊上市申请已正式获NMPA受理。此次申报上市适应症为:治疗既往接受过化疗且携带表皮生长因子受体20号外显子插入突变的局部晚期或转移性非小细胞肺癌成人患者。
4、CDE公示显示,辉瑞的lorlatinib片两项申请已被纳入拟优先审评,拟开发治疗特定的ALK阳性局部晚期或转移性非小细胞肺癌患者。
5、CDE官网显示,强生的JNJ-56136379片、JNJ-73763989注射剂被拟纳入突破性疗法,均用于治疗慢性乙型肝炎病毒感染。
6、赛诺菲注射用重组人凝血因子VIII Fc-血管性血友病因子-XTEN融合蛋白获CDE拟突破性疗法,拟定的适应症是用于患有A型血友病的成人和儿童:1.常规预防治疗,用于减少出血的发生频率;2.出血的按需治疗;3.围手术期出血的处理。
7、CDE公示显示,梯瓦5.1类新药“醋酸格拉替雷注射液”已在中国递交上市申请,并获得受理。根据公司财报,醋酸格拉替雷注射液是一款多发性硬化药物。
8、CDE官网显示,第一三共HER3 ADC新药U3-1402获批临床,拟用于非小细胞肺癌。
9、复星医药在股东大会上回复投资人问询时表示,NMPA对mRNA新冠疫苗“复必泰”的审定工作已经基本完成,专家评审已经通过,目前正在加紧进行行政审批阶段。
10、根据CDE官网,贝达药业和Agenus共同申报的1类新药泽弗利单抗注射液临床申请获NMPA默示许可,用于晚期实体瘤。
11、CDE最新公示,信达生物FGFR 1/2/3抑制剂pemigatinib片,以“符合附条件批准的药品”拟纳入优先审评,拟定适应症为:用于既往至少接受过一种系统性治疗,且经检测确认存在有FGFR2融合或重排的晚期、转移性或不可手术切除的胆管癌成人患者的治疗。
12、海正药业发布公告称,全资子公司瀚晖制药收到NMPA核准签发的关于氨氯地平阿托伐他汀钙片(商品名“多达一”)的《药品补充申请批准通知书》。多达一为国内上市的原研药品,适用于高血压或心绞痛患者合并高胆固醇血症或混合型高脂血症的治疗。
13、NMPA公示,迈博药业的注射用英夫利西单抗生物类似药获批上市。该药本次获批的适应症包括:类风湿关节炎、成人及儿童克罗恩病、瘘管性克罗恩病、强直性脊柱炎、银屑病及成人溃疡性结肠炎患者,商品名为类停。
14、NMPA发布药品批准证明文件,联邦制药三代胰岛素门冬胰岛素注射液和门冬胰岛素30注射液同时获批上市。该药不仅适用于成人、青少年和儿童糖尿病患者,而且还可用于妊娠期糖尿病。
15、上海医药发公告称,全资子公司上药东英的注射用帕瑞昔布钠收到NMPA颁发的《药品注册证书》,该药品获得批准生产,主要用于手术后疼痛的短期治疗。
16、安科生物发公告称,注射用人生长激素收到NMPA下发的《药品补充申请批准通知书》,增加适应症为性腺发育不全所致女孩的生长障碍。
17、上海莱士发公告称,其全资子公司人凝血酶原复合物获得《药品注册证书》。该药物主要用于治疗先天性和获得性凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ缺乏症包括凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ缺乏症包括乙型血友病;抗凝剂过量、维生素K 缺乏症;因肝病导致的凝血机制紊乱;播散性血管内凝血时,凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ被大量消耗,可在肝素化后应用;各种原因所致的凝血酶原时间延长而拟作外科手术患者,但对凝血因子Ⅴ缺乏者可能无效;治疗已产生因子Ⅷ抑制物的甲型血友病患者的出血症状;逆转香豆素类抗凝剂诱导的出血。
18、白云山发公告称,分公司白云山制药总厂收到NMPA签发的《药品补充申请批准通知书》,阿莫西林胶囊已通过仿制药一致性评价。
19、NMPA显示,华益泰康4类仿制药琥珀酸美托洛尔缓释片获批生产并视同过评,为国内首仿。琥珀酸美托洛尔缓释片是一款选择性的β1受体阻滞剂,适用于高血压,心绞痛,伴有左心室收缩功能异常的症状稳定的慢性心力衰竭。
20、NMPA显示,倍特药业以仿制3类报产的盐酸右美托咪定氯化钠注射液获批。盐酸右美托咪定是一种相对选择性α2-肾上腺素受体激动剂,适用于行全身麻醉的手术患者气管插管和机械通气时的镇静、用于重症监护治疗期间开始插管和使用呼吸机患者的镇静。
21、CDE官网公示,拟将华兰生物四价流感病毒裂解疫苗纳入优先审评审批,用于6个月至3岁以下人群预防相关型别的流感病毒引起的流行性感冒。
22、扬子江2款以新注册分类报产的仿制药进入行政审批阶段,分别为氟比洛芬酯注射液、塞来昔布胶囊,两款产品均为抗炎抗风湿药。
23、正大天晴以仿制4类报产的氢溴酸伏硫西汀片进入行政审批阶段,有望获批,并视同过评。氢溴酸伏硫西汀片是一种抗抑郁药物,主要用于成人重度抑郁症。
24、正大天晴、先声药业以仿制4类报产的甲磺酸仑伐替尼胶囊均进入行政审批阶段,用于治疗肝癌。
25、海思科以仿制4类报产的培哚普利吲达帕胺片进入行政审批阶段,有望拿下首仿。该产品为复方降压药。
26、福元医药、圣华曦药业以仿制4类报产的依折麦布片均进入行政审批阶段,有望获批并视同过评。依折麦布为降脂药。
27、石药集团欧意药业以仿制4类报产的马来酸阿法替尼片进入行政审批阶段,有望获批。该药用于既往未接受过EGFR-TKI治疗的EGFR基因敏感突变的局部晚期或转移性非小细胞肺癌,及含铂化疗期间或化疗后疾病进展的局部晚期或转移性鳞状组织学类型非小细胞肺癌。
28、荣昌生物维迪西妥单抗第2项适应症上市申请获NMPA受理。预计该适应症为治疗尿路上皮癌。
29、贝达药业发公告称,公司申报的盐酸恩沙替尼胶囊(贝美纳)拟用于“适用于间变性淋巴瘤激酶阳性的局部晚期或转移性非小细胞肺癌患者的治疗”的上市许可申请已获得NMPA受理。
30、通化东宝宣布,两款预混型门冬胰岛素——门冬胰岛素30注射液、门冬胰岛素50注射液上市申请获CDE受理。
31、兴齐眼药发公告称,盐酸莫西沙星滴眼液收到NMPA下发的药品注册受理通知书。该药申报的临床适应症为敏感微生物引起的细菌性结膜炎。
32、CDE公示显示,奕拓医药的SHP2变构抑制剂ET0038片获得两项临床试验默示许可,拟开发用于治疗MAPK信号通路异常的晚期实体瘤。
33、欧康维视宣布,其治疗儿童近视发展的核心产品OT-101获CDE批准开展3期临床,以评估OT-101治疗儿童受试者近视进展的安全性和有效性。
34、CDE官网显示,翰森制药申报的治疗用生物制品HS-20093、HS-20089的1类新药临床申请获得受理。
35、科华生物公告,产品抗环瓜氨酸肽抗体测定试剂盒获得医疗器械注册证。该产品供医疗机构用于体外定量测定人血清样本中抗环瓜氨酸肽抗体的含量,作辅助诊断用。
2、和黄医药宣布,欧洲药品管理局已确认并受理索凡替尼用于治疗胰腺和胰腺外神经内分泌瘤的上市许可申请。EMA已确认提交材料的完整性,并且已准备好启动正式的审评程序。
3、蓝鸟生物表示,欧盟药物警戒风险评估委员会已认定Zynteglo的治疗收益大于风险,决定重新批准该药物进入欧洲的血液病治疗市场。这也意味着在中断5个月后,蓝鸟克服了另一项障碍,重新在欧洲推出β-地中海贫血基因疗法Zynteglo。
4、海创药业宣布,其“HC-1119新冠住院患者治疗2/3期临床试验”申请获得巴西卫生监督局批准,将在巴西正式展开相关临床试验。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#罗沙司他#
82
#英夫利西单抗#
40
学习了
64