Nature:为什么COVID-19肺炎比典型肺炎持续时间更长,造成的损害更大?
2021-01-13 MedSci原创 MedSci原创
新冠肺炎与其他原因引起的肺炎有显著不同。
Nature上一项新发表的研究报告称,新冠肺炎与其他原因引起的肺炎有显著不同。它展示了病毒如何劫持肺部自身的免疫细胞,并利用它们在肺部扩散数周。感染会留下损伤,并加剧COVID-19患者的发热、低血压和肾脏、大脑、心脏和其他器官的损伤。通过这些,科学家发现了治疗新冠肺炎的一个靶点。

导致肺炎的细菌或病毒,如流感,可以在数小时内在肺部大面积传播。在现代的重症监护室里,这些细菌或病毒通常在发病前几天由抗生素或人体免疫系统控制。但在1月11日发表在《自然》(Nature)杂志上这篇研究中,Northwestern Medicine的研究人员表示,COVID-19肺炎是不同的。
SARS-CoV-2不会迅速感染肺部的大片区域,而是会在肺部的多个小区域扎根。然后它劫持肺部自身的免疫细胞,并利用它们在肺部扩散,持续数天甚至数周,就像森林里蔓延的多次野火。随着感染在肺部缓慢移动,它会留下损伤,并持续助长发烧、低血压,损害COVID-19患者的肾脏、大脑、心脏和其他器官。
该研究的作者表示,与其他肺炎相比,COVID-19的严重并发症可能与较长的病程有关,而不是与更严重的疾病有关。
这是科学家首次系统分析COVID-19肺炎患者肺部的免疫细胞,并将其与来自其他病毒或细菌的肺炎患者的细胞进行比较。
通过详细分析,研究人员确定了治疗严重SARS-CoV-2肺炎和减少其危害的关键目标。目标是免疫细胞:巨噬细胞和T细胞。该研究表明,通常负责保护肺部的巨噬细胞可能会被SARS-CoV-2感染,并有助于通过肺部传播感染。
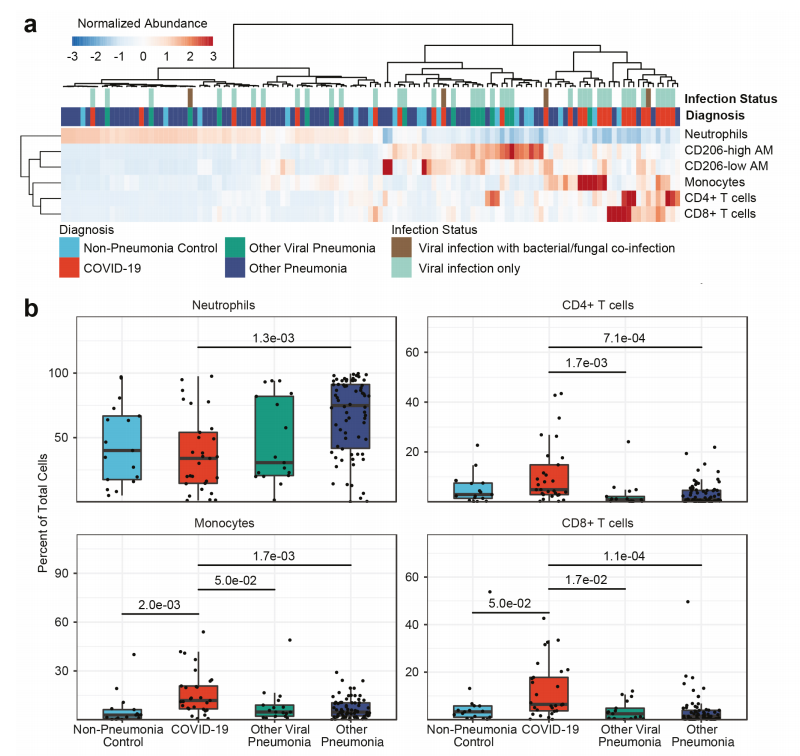
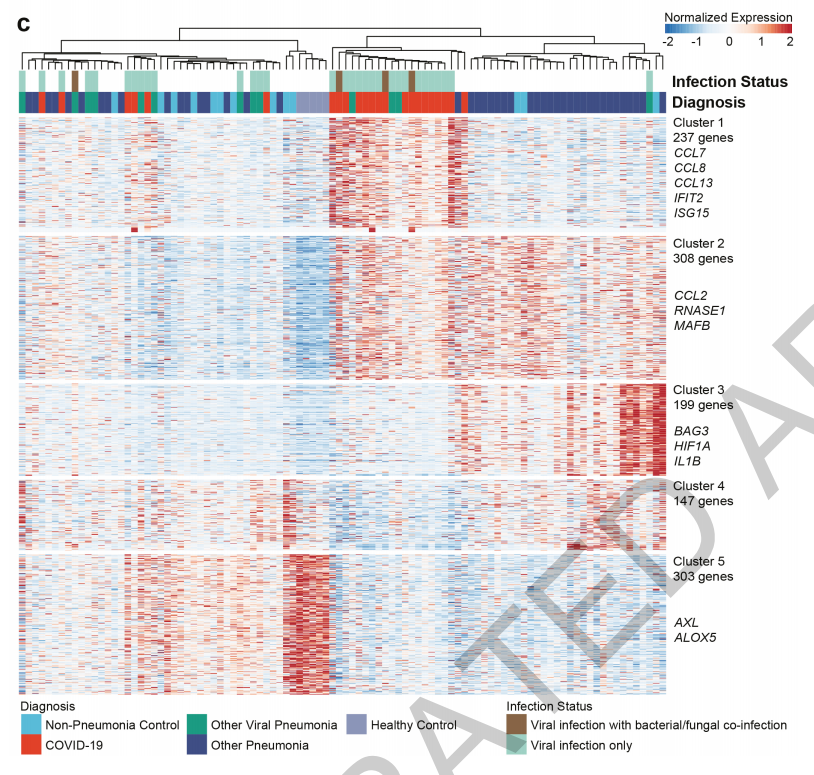
在气管插管时,严重SARS-CoV-2肺炎患者的肺泡腔富含T细胞和单核细胞,并含有SARS-CoV-2rna和表达干扰素应答基因的肺泡巨噬细胞
Northwestern Medicine将在2021年初的一项临床试验中测试一种实验性药物,用于治疗COVID-19肺炎患者的这些目标。被测试的药物可以抑制这些免疫细胞的炎症反应,从而启动受损肺部的修复过程。
资深合著者、Feinberg大学肺部和危重病医学助理教授、Northwestern Medicine医生Ben Singer博士表示,与流感一样,COVID-19不太可能永远消失,即使大部分人口接种了疫苗。
“Northwestern Medicine和其他地方的研究人员已经在预测这种迅速变异的RNA病毒将逃避现有疫苗的机制,” Singer博士说。“这项研究将帮助我们开发治疗方法,减轻COVID-19患者的严重程度。
该研究还揭示了为什么使用呼吸机治疗COVID-19的患者因常规肺炎的死亡率低于使用呼吸机的患者。肺部的剧烈燃烧(普通肺炎)有更高的死亡风险。COVID-19肺炎患者患病时间较长,但肺部炎症不像普通肺炎那么严重。
“如果COVID-19患者得到仔细管理,卫生保健系统没有不堪重负,医护人员就可以帮助他们度过这一时期。虽然这些病人病得很重。他们需要很长时间才能好转。但如果你有足够的床位和医护人员,你可以将死亡率保持在20%。当卫生系统不堪重负时,死亡率翻倍,高达40%。”所以关键点在于医疗资源。
在这项研究中,科学家对86名使用呼吸机的COVID-19患者的肺液进行了高分辨率分析,并将其与256名使用呼吸机的其他类型肺炎患者的肺液进行了比较。出于安全考虑,世界上只有少数几个组织对COVID-19患者肺部的免疫反应进行了分析。因此,关于导致COVID-19重症患者死亡的原因的重要信息丢失了。
Northwestern Medicine进行的这项研究是独特的,因为这些研究者在大流行之前就已经研究肺炎很多年了。因此,当COVID-19大流行袭来时,他们准备以安全和系统的方式收集这些患者肺部的液体,并将其与大流行前收集的其他重症监护室肺炎患者的液体进行比较。这一研究基础设施使他们能够证明COVID-19患者的肺炎不同于其他肺炎,更重要的是,它是如何不同的。科学家从病人的肺液中提取细胞,观察这些细胞表达的RNA和蛋白质,使他们能够确定这些免疫细胞如何导致炎症。
总之,这项研究提供的数据集支持一个可测试的模型,在该模型中,携带SARS-CoV-2的肺泡巨噬细胞与分泌IFNγ-的T细胞形成正反馈循环,促进了严重COVID-19患者的肺泡炎。
参考文献:Rogan A. Grant, Luisa Morales-Nebreda, Nikolay S. Markov, Suchitra Swaminathan, Melissa Querrey, Estefany R. Guzman, Darryl A. Abbott, Helen K. Donnelly, Alvaro Donayre, Isaac A. Goldberg, Zasu M. Klug, Nicole Borkowski, Ziyan Lu, Hermon Kihshen, Yuliya Politanska, Lango Sichizya, Mengjia Kang, Ali Shilatifard, Chao Qi, Jon W. Lomasney, A. Christine Argento, Jacqueline M. Kruser, Elizabeth S. Malsin, Chiagozie O. Pickens, Sean B. Smith, James M. Walter, Anna E. Pawlowski, Daniel Schneider, Prasanth Nannapaneni, Hiam Abdala-Valencia, Ankit Bharat, Cara J. Gottardi, G. R. Scott Budinger, Alexander V. Misharin, Benjamin D. Singer, Richard G. Wunderink and The NU SCRIPT Study Investigators. Circuits between infected macrophages and T cells in SARS-CoV-2 pneumonia. Nature, 2021; DOI: 10.1038/s41586-020-03148-w
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#Nat#
30
#持续时间#
46