JCO:无RCT证据支持的药物也会被批准上市么?FDA批准的无RCT证据支持的抗癌药上市后会存在哪些隐患?
2018-04-16 慧语 肿瘤资讯
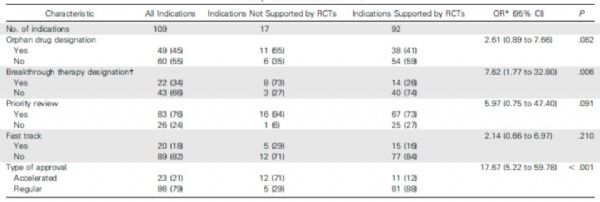
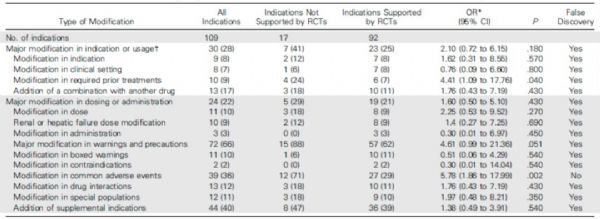
在没有随机对照临床试验(RCT)证据支持的条件下,仍然会有抗癌药物被FDA批准上市,尤其是在某些罕见病和尚无有效疗法的疾病中比较常见。这其中的隐患是,上市前并没有充分的数据对药物疗效和安全性进行验证,伴随的问题则往往是在药物上市后才会发现某些严重的甚至致命的不良反应,此时势必会对药物标签进行修正。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#FDA批准#
28
#JCO#
25
#抗癌药#
22