国内外不良反应因果判断原则及评价方法解读
2018-11-30 魏戌,谢雁鸣 魏戌,谢雁鸣
[摘要] 不良反应因果关系判断是药物警戒研究的通用程序,目前尚无统一的判断标准与分类标准。时间性、一致性、 特异性、反应程度是不良反应因果判断应遵循的基本原则。不良反应因果关系评价方法众多,大致可分为标准化算法、专家判断法、贝叶斯法。部分评价方法分类标准之间定义模糊不清、病例资料的不完整、评价者临床应用时的不同理解均是造成评价结果不同的重要原因。几乎每一种方法均对不良反应因果关系进行
[摘要] 不良反应因果关系判断是药物警戒研究的通用程序,目前尚无统一的判断标准与分类标准。时间性、一致性、 特异性、反应程度是不良反应因果判断应遵循的基本原则。不良反应因果关系评价方法众多,大致可分为标准化算法、专家判断法、贝叶斯法。
部分评价方法分类标准之间定义模糊不清、病例资料的不完整、评价者临床应用时的不同理解均是造成评价结果不同的重要原因。几乎每一种方法均对不良反应因果关系进行分级,主要为 5 级分类,但评级方法间的基本原理、评价标准、特异度与敏感度有所差异。每一种方法均有其优缺点,尚无一项标准化的方法适用于所有的不良反应评价。
[关键词] 不良反应; 个例评价; 因果判断原则; 因果评价方法
不良反应因果判断是特定的治疗与观察到的不良事件之间因果关系可能性的评价,已经成为药物警戒研究中通用 的程序。本文综述国内外不良反应个例评价的因果判断原 则与评价方法,讨论不良反应因果评价存在的问题,比较评 价方法间的异同点,分析不同方法的优缺点。
1 不良反应因果判断原则
1. 1 时间性
时间性是指用药与不良反应的出现有无合理的时间关系,尤其是符合药物作用的潜伏期。先因后果,原因与结果的间隔时间符合已知的规律,如常发生Ⅰ型变态反应的中药注射剂,引起的过敏性反应多发生在用药后 0.5 h 内[1];
吩噻嗪类药物引发肝损害一般为服药 3 ~ 4 周以后出 现。另外,可观察用药与首次出现不良事件的时间间隔是否符合该药的药动学参数。在因果关系评价中, WHO、法国、瑞典、中国等药品管理机构均将可疑药物与临床事件之间的时间序列关系作为首要的判断条件。
1. 2 一致性
因果判断的一致性是指发生的反应是否与药物已有的信息一致,如已知的不良反应类型、厂家、批号、剂型、用法与用量、用药原因,能够用来解释特异性临床表现的药理学理论,以及相关文献的观点等。
Emanueli[25]等因果评价方法均将其作为记分的重要评价标准。也有学者[6]认为 因果判断的一致性是指不应有时间、地点、人群的特异性,而 且对于不同的观察方法得出的结论也是一致的。
1. 3 特异性
不良反应因果关系的特异性,直接决定评价的可靠程度。应明确是否有合并治疗药物( 药物交互作用) 、原患疾病( 高血压病、糖尿病、血脂异常、冠心病、肝肾功能异常等) 及其他治疗( 手术、放疗、化疗) 的影响,这些混杂因素的存在无法判断该治疗药物与发生的不良事件是否有明确的因果关系。混杂因素是对结果产生影响的混淆,若将对结果有影响的混杂因素引入评价,可能错误的判定最终结果是由某一种单一因素引起。
1.4 发生强度
不良反应因果关系的发生强度是指发生不良事件后,通过去激发试验与再激发试验来表达,观察停药与减量后临床事件是否继续存在、减轻或消失,再次用药后临床事件是否复现,剂量-反应曲线是关系强度的最好例证。 再激发试验往往由于已经发生的严重不良反应,甚至是不可逆的器官损害而不能进行,影响了因果关系评估的准确性。 当有可能进行且为伦理道德所接受时,应尽可能接受激发试验,尤其在认为药物为患者所必须时[6]。再激发必须给予同样的剂量,并有足够的疗程。
国内学者[7]提出因果联系强度还可表现在未撤药、未减量的情况下,应用特定的拮抗药后观察反应是否有所好转; 停药并进行相应的治疗后反应是否有所好转。
2 不良反应因果评价方法
2. 1 标准化算法
标准化算法是结构化与标准化的评价方 法,以问卷的形式提出一系列特定的问题,将因果关系的可 能性进行分级评定,是不良反应因果判断最常用的方法。国 际比较常用的2 种方法是1977 年提出的 Karch 与 Lasagna 评 定法[8]与 1981 年提出的 Naranjo 评定法[9]。
Karch 与 Lasagna 评定法主要考虑5 个方面的内容: 反应的发生是否与可疑药物有时间先后关系,是否为已知的不良反应类型,去激发试验,再激发试验,是否为其他原因所解释。Naranjo C A 等学者根据所罗列的 10 条细目的评分总和,根据总评分的结果分为“肯定”、“很可能”、“可能”、“可 疑” 4 个等级,用来描述不良反应因果关系的程度( 简称为 Naranjo 评定法 ) 。“肯定”≥9 分,“很可能” 5 ~ 8 分,“可能”1 ~4 分,“可疑”≤0 分( 表 1) 。

上述 2 种方法对于“肯定相关”的不良反应因果关系的评价是一致的,包括与药物有合理的时间序列关系,并且药物浓度在体液或组织内已被证实; 反应是可疑药物已知的不良反应类型; 撤药时不良反应改善或消失,再次用药不良反应复现。 除普适性的标准化算法外,国外学者提出了针对药源性急性肝损害的不良反应因果关系评价方法 RUCAM ( Roussel-Uclaf causality assessment method) [10]。
该方法考虑到肝细胞型、胆汁郁积型或混合型不同的肝损害特点, 从反应发生时间一致程度、演变过程的一般程度、危险因素、合并用药、非药物原因引起的可能性、该药已知信息、 再激发的反应等 7 个方面来进行判断,总分范围为 - 9 ~ 15 分,分为“极可能”、“很可能”、“可能”、“可疑”、“不可 能” 5个等级。
2. 2 专家判断法
专家判断法是临床医生或者临床药理学家根据可疑不良反应的所有数据,估计其相对重要性和权重,推断药物与发生不良事件之间因果关系的方法[11-12] 。最具代表性的是 WHO 乌普萨拉监测中心提出的因果关系判断方法( 简称为 UMC 评定法) 。UMC 法将可疑不良反应的因 果关系分成 6 级,包括“肯定( certain ) ”,“很可能( probable/ likely ) ”,“可能( possible ) ”,“不可能( unlikely ) ”,“待评价 ( conditional/unclassified ) ”,“无法评(unassessible/unclassifiable) ” [13]( 表 2) 。

UMC 评定法重视临床事件与可疑药物使用的时间序列 关系,并且考虑了临床与药理学方面的信息,对“不可能相 关”的病例进行了定义。该方法为了观察未知的或者未期望 的不良反应,在因果评价内容中并未考虑之前药物所发生的 不良反应信息。 中国国家药品不良反应监测中心参照 UMC 法于 1994 年制定了相应的因果判断准则( 简称为卫生部评定法) ( 表 3)[14]。
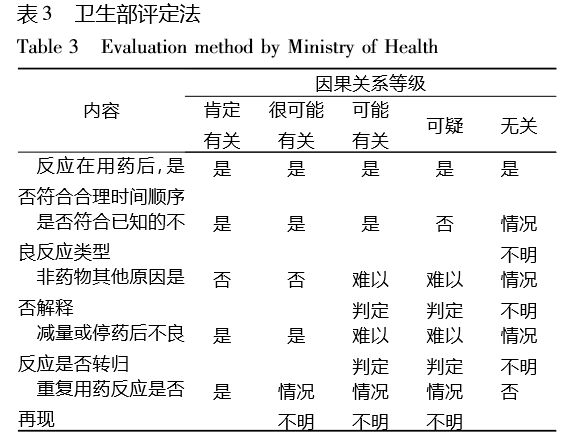
卫生部评定法遵循了不良反应因果关系判断的基本原则,考虑了不良反应发生的时间性、一致性、发生强度、特异性方面的因素,其内容类似于 Karch 与 Lasagna 评定法。 卫生部评定法对于判断不良反应的因果关系的权重和先后应用次序并不相同,前3 项是因果关系成立的必要条件[15]。 当第 1, 3 项符合,而第 2 项不符合时,需要考虑是否为新的 不良反应类型。
2. 3 贝叶斯法
贝叶斯法是运用概率论语言进行可疑不良反应因果关系评价,考虑到所有可利用的流行病学背景以及病例信息,目标是计算药物 D 引起特定不良事件E的后验比 ( posterior odds) ,即支持药物是不良事件原因的后验比[16]。 澳大利亚首次将概率论的方法运用于因果评价中[17]。 该方法[18]评价可能影响药物引发特定不良反应可能性 的 5 个要素,包括用药史、发作时间、症状特征、去激发试验结果、再激发试验结果。
通过后验概率说明在几种可能的原因中,某种原因导致该事件的大小。其中贝叶斯法的实施步骤主要分为: 确定病例的参数,收集病例有关资料,估算先验比,估算似然率,计算后验比。
3 不良反应因果评价方法的解读
3. 1 因果关系评价存在的问题
相同的评价方法,相同的 病例数据,不同的评价者,其评价结果都会存在差异。在不 良反应因果关系评价中,部分分类标准间定义模糊不清、病例资料的不完整、评价者临床应用时的不同理解均是造成评 价结果不同的重要原因[19]。不良反应因果关系评价正如完成系统评价一样,一份好的系统综述取决于所纳入的随机对照临床试验的质量,随机对照试验质量较好,系统评价报告才能颇具价值。
反之,由于所纳入的单个随机对照试验的方法学质量问题,无法得出确切的结论。鉴于此,国外学者[20] 建议应将药物使用起始时间、去激发试验信息、混杂因素、再激发试验信息、药物暴露的程度与时间、流行病学背景与临床信息等资料详细记录在病例报告中。
3. 2 因果评价方法的异同点
综合国内外不良反应因果判 断方法,虽然不同的方法间存在差异,但是也有共同的特点。 几乎每一种方法均对不良反应因果关系进行分级,通过分级来判断可疑药物与发生的不良事件之间的因果关系。根据因果关系评价方法的介绍,评价等级主要分为5 个层次: 肯 定( definite/causative/certain) ,很有可能( probable/likely) ,可 能( possible) ,可疑( doubtful) ,无关( remote/unlikely ) 。“待评 价”与“无法评价”尚不属于因果关系评价的正式术语。
因果评价方法间的基本原理有所差异。标准化算法是通过半定量的方法来评价药物与事件因果关联的程度,根据 所得总分进行定量转换估计,划分因果等级; 专家判断法是 依靠评价者的临床经验、知识背景,得出定性的结论; 贝叶斯 方法以贝叶斯定理为基础,应用概率理论,估算药物原因的 先验概率和后验比,推测具有最大可能性的原因。
因果评价方法间的评价标准有所差异。UMC 评定法考虑到了临床药理学研究的发现,而一些评价方法则认为药理病理学研究在临床实际中可操作性差,无法迅速作出因果判断; 当不只是一种药物可疑时, Kramer算法[21]能够对可疑药 物进行单独评价,很多评价方法均未考虑到这一点; 法国因果评价法[22]省去了“肯定相关”与“与药物无关”的评价,认为尚无法得出明确的因果关系结论。
因果评价方法间的特异度和敏感度有所差异。赖世 隆[23]比较了 Naranjo 评定法与卫生部评定法在判断不良反 应中的差异,研究显示卫生部评定法的特异性较高,而 Naranjo 法的敏感性较高。Naranjo 法更有利于不良反应的发现,尤其是罕见的不良反应,但可使报告的不良反应发生率偏高,建议将得分在 6 ~8 分定义为“很可能相关”。
3. 3 因果评价方法的优缺点
标准化算法与专家判断法相比,其优点是提高了评价者间的可靠性,能够发现不同评价 者在评价同一病例时不一致的评价条目。但记分法仍然缺 乏灵活性,因为考虑到临床的可操作性以致于评价条目均是 基于有限的信息,无法包括观察到的附加信息。此外,混杂 因素识别是对算法最大的挑战,混杂因素的存在会降低算法 的敏感性与特异度[24]。
Emanueli 与 Sacchetti 算法适用于大型临床试验不良反应的分析,但如果不能排除临床状态或者 其他治疗因素的影响,使用该方法难以评定比“可能有关”更 高的等级[2]。Karch 与 Lasagna 评定法较其他算法而言更加 简洁,易于操作,更适于计算机语言,但难以证实新的不良反 应,或者头一些病例的不良反应,因为需要之前不良事件的 描述[8]。
Naranjo 评定法评价单一药物发生不良反应的可能性,并不能评价 2 种药物交互作用的影响[25]。UMC 法增加了临床药理学方面的观察内容,重视观察质量,然而该方法并未考虑之前药物的信息与统计学概率的问题[13]。贝叶斯法最大的优点在于不受病例资料信息的限制,能够同时评价可能的原因,定量描述可疑药物对不良事件支持的程度。但是在研究中难以获得资料[26]。
综上所述,每一种因果关系评价方法均有其优缺点,现 有文献尚无证据证明某一种方法可作为因果判断的“金标 准”,因此在临床实际中应遵循因果判断的基本原则,考虑患 者的实际情况和可操作性,选择较为常用、能够基本反映疗 法不良反应特征的评价方法。
[参考文献]
[1] 魏戌,谢雁鸣,王永炎. 皮试试验与中药注射剂上市后临床安 全性再评价[ J] . 中国中药杂志, 2011, 36( 20) :2877.
[2] Emanueli A, Sacchetti G. An algorithm for the classification of untoward events in large scale clinical trials[J] . Agents Actions Suppl, 1980, 7:318.
[3] Venulet J, Ciucci A, Berneker G C. Standardised assessment of drug-adverse reaction associations: rationale and experience[J] . Int J Clin Pharmacol Ther Toxicol, 1980, 18:381.
[4] Jones J K. Adverse drug reactions in the community health setting: approaches to recognizing, counseling, and reporting[J]. Fam Community Health, 1982, 5:58.
[5] Wiholm B E. The Swedish drug-event assessment methods: spe
cial workshopregulatory[ J] . Drug Inf J, 1984, 18:267.
[6] 刘建平,邢建民 . 循证的药品不良反应评价方法[ J] . 中国药 物警戒, 2010, 7( 1) :12.
[7] 管玫,钟光德,黄文志. 药品不良反应病例报告评价标准的探 讨[ J] . 中国药房, 2008, 19( 26) :2054.
[8] Karch F E, Lasagna L. Toward the operational identification of adverse drug reactions[ J] . Clin Pharmacol Ther, 1977, 21:247.
[9] Naranjo C A, Busto U, Sellers E M, et al. A method for estimating the probability of adverse drug reactions[J]. Clin Pharmacol Ther, 30( 2) :239.
[ 10] Benichou C, Danan G, Flahault A. Causality assessment of adverse reactions to drugs: II. An original model for validation of
drug causality assessment methods: case reports with positive rechallenge[ J] . J Clin Epidemiol, 1993, 46:1331.
[11] Hoskins R E, Mannino S. Causality assessment of adverse drug reactions using decision support and informatics tools[J]. Pharmacoepidemiol Drug Saf, 1992, 1:235.
[ 12] Arimone Y, Begaud B, Miremont-Salame G, et al. A new method
for assessing drug causation provided agreement with experts' judgment[ J] . J Clin Epidemiol, 2006, 59:308.
[ 13] World Health Organization( WHO) , Uppsala Monitoring Centre.
The use of the WHO-UMC system for standardised case causality assessment. WHO[EB/OL] . [2012611] . http: / /www. who
umc. org/graphics/26649. pdf.
[ 14] 杜文民,王永铭,程能能. 药品不良反应的判定及其研究方法 [ J] . 药物警戒, 2005, 2( 1) :11.
[ 15] 王家良 . 临床流行病学———临床科研设计、测量与评价[M] . 上海: 上海科学技术出版社, 2009:458.
[ 16] Lane D A. The Bayesian approach to causality assessment: an introduction[ J] . Drug Infor J, 1986, 20:455.
[ 17] Mashford M L. The Australian method of drug-event assessment.
Special Workshopregulatory[ J] . Drug Inf J, 1984, 18:271.
[ 18] 魏水易,剻丽萍,顾文华. 贝叶斯法与可疑药物不良反应因果 评价[ J] . 药物不良反应杂志, 2002,( 2) :102.
[ 19] Liu B A, Knowles S R, Mittmann N, et al. Reporting of fatal adverse drug reactions[ J] . Can J Clin Pharmacol, 2001, 8:84.
[ 20] Kelly W N. The quality of published adverse drug event reports: review[ J] . Ann Pharmacother, 2003, 37:1774.
[ 21] Kramer M S, Leventhal J M, Hutchinson T A, et al. An algorithm for the operational assessment of adverse drug reactions: I. Background, description, and instructions for use[J] . JAMA, 1979, 242:623.
[22] Dangoumau J, Evreux J C, Jouglard J. Method for determination of undesirable effects of drugs[ J] . Therapie, 1978, 33:373.
[ 23] 许卫华,温泽淮,赖世隆 . 2 种药物不良反应因果关系判断方 法的比较与分析[J] . 中药新药与临床药理, 2000, 11( 4) :
248.
[ 24] Naranjo C A, Busto U, Sellers E M, et al. A method for estimating the probability of adverse drug reactions[J]. Clin Pharmacol Ther, 1981, 30:239.
[25] Kane-Gill S L, Kirisci L, Pathak D S. Are the Naranjo criteria re
liable and valid for determination of adverse drug reactions in the intensive care unit? [ J] . Ann Pharmacother, 2005, 39:1823.
[26] Hoskins R E, Mannino S. Causality assessment of adverse drug reactions using decision support and informatics tools[J] . Pharmacoepidemiol Drug Saf, 1992, 1:235.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












学习
117
#因果判断#
34
#不良反应#
40
#评价#
41