Science:胶质细胞激活引发的神经炎症让人更容易感到疼痛
2016-11-15 佚名 生物探索
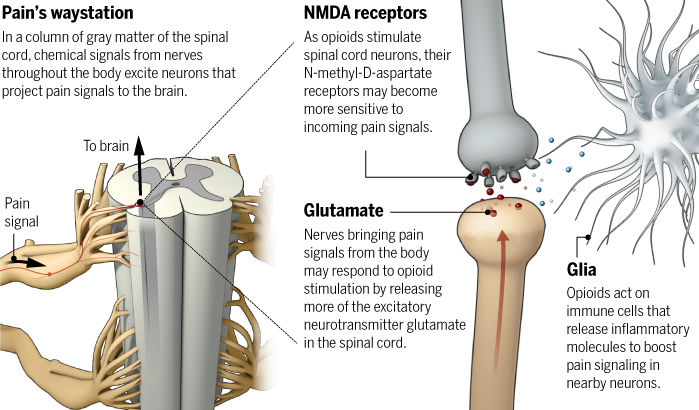
近日,来自维也纳医科大学脑研究中心的研究人员发现,疼痛不进通过神经细胞传播,同时也牵涉到非神经细胞——胶质细胞,后者不仅与临床相关的疼痛模型密切相关,同时它们的激活还能够产生疼痛放大效应。这一研究发表于Science杂志上。疼痛发生的机制尚不完全清楚。一般认为,神经末梢的伤害性感受器受到各种伤害性刺激后,经神经通路将兴奋传递给脊髓,脊髓将这些信息预处理之后再传递给大脑,进而引起疼痛感觉。但是,来自

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#神经炎#
26
#SCIE#
36
#胶质细胞#
24