J Exp Med:SARS-CoV-2可感染神经细胞,并导致组织损伤
2021-01-21 MedSci原创 MedSci原创
一个科学家小组最近一项研究提供了SARS-CoV-2可以直接感染中枢神经系统(CNS)中的细胞,并导致组织损伤的证据。
一个科学家小组最近一项研究提供了SARS-CoV-2可以直接感染中枢神经系统(CNS)中的细胞,并导致组织损伤的证据。
SARS-CoV-2通过与细胞表面血管紧张素转换酶II(ACE-2)受体结合而感染肺组织。一旦病毒与细胞结合,病毒就可以进入细胞,引起呼吸系统症状,如呼吸急促和干咳。
然而,最近的研究表明,这种病毒也可以感染中枢神经系统的细胞,并且可阻碍中枢神经系统的血液流动。这项研究于1月12日发表于《实验医学杂志(Journal of Experimental Medicine)》
这项研究可以解释为什么COVID-19患者会产生头晕、神志不清、中风和昏迷等神经系统症状。
研究小组使用了三种不同的大脑模型:人脑类器官、基因工程小鼠以及对已死亡的COVID-19患者进行尸检。
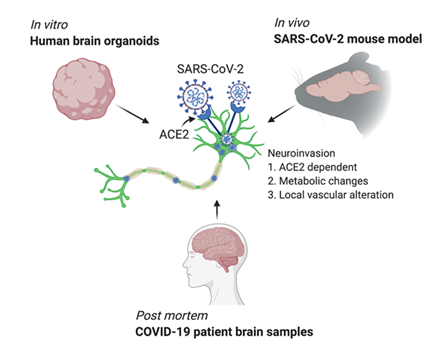
首先,利用人脑类器官,研究人员找到了人脑感染的明确证据,且发现感染伴随邻近神经元的代谢变化,但并没有证据显示产生了I型干扰素应答。他们还发现用抗体阻断ACE-2受体或给予COVID-19患者脑脊液可以预防神经元感染。
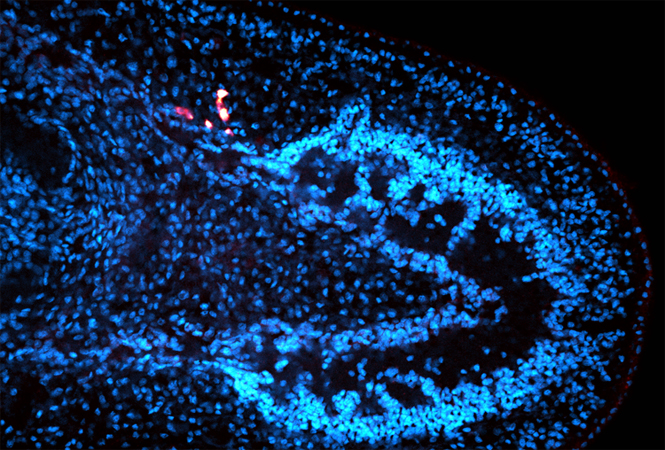
研究人员还观察到人脑类器官在特定的脑区积聚了SARS-CoV-2阳性细胞,这为病毒感染神经元并自我复制提供了证据。
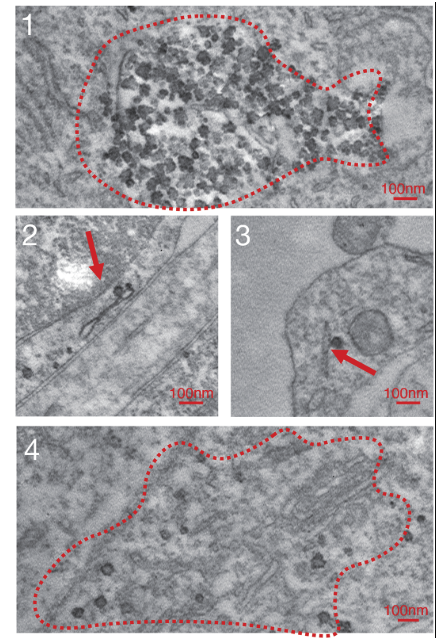
电镜下人脑类器官中的SARS-CoV-2病毒
其次,研究人员利用过度表达人ACE-2的小鼠模型证明了SARS-CoV-2在体内可侵袭神经细胞。
研究人员在SARS-CoV-2病毒感染小鼠脑中检测到高水平的受感染神经细胞,且与血管的显著变化有关,这些变化可能会破坏大脑内的氧气流动。
最后,研究人员检查了三名死于严重COVID-19并发症的患者的大脑,这三明患者都有过呼吸衰竭,并被送入重症监护室的经历。
在受感染的大脑区域内,有组织损伤和细胞死亡的迹象,表现为缺血性梗死。
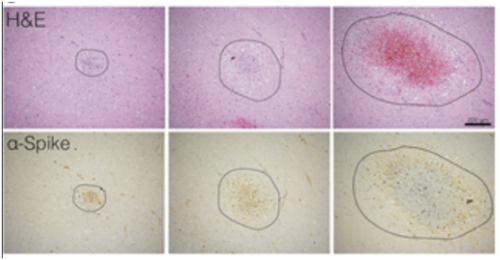
阳性病毒染色主要出现在梗死边缘周围
研究还发现,尽管SARS-CoV-2具有嗜神经特性,可以感染患者的神经元,但它并没有像其他嗜神经病毒那样引起典型免疫反应。
原始出处:Eric Song, Ce Zhang, Benjamin Israelow, et al. Neuroinvasion of SARS-CoV-2 in human and mouse brain. Journal of Experimental Medicine. January 12 2021
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#组织损伤#
34
#SARS-CoV#
24
#SARS#
25
#损伤#
34
#神经细胞#
34
#Med#
28