2019年市值飙升千亿 疫苗行业迎高光时刻!
2020-01-08 DAISY E药经理人(ID:eyjlr2013)
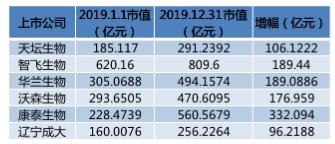
业绩预期大幅增长,上市公司市值迅速飙升,重磅新品集中获批……刚刚过去的2019年,经历过假疫苗、劣质疫苗等诸多大案之后的中国疫苗行业显然已经开始呈现出一个完全不同的面相。飙升千亿的市值变化以及重磅发布的政策背后,能够看出的是疫苗行业的新走势。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











很好的学习机会
53