痴呆症对个人和家庭造成了破坏,并且已经达到了流行病的程度,美国有500多万人受到影响,全世界有4380万人,并且预计其流行率在短期内会上升。血管周围排泄的损害(肝脏功能障碍)和脑小血管疾病(CSVD)可能在认知障碍(从认知障碍到痴呆)中起着机制性的作用。神经元功能与脑血管健康密切相关;因此,大脑疾病中的神经血管单元(即神经元、胶质细胞和血管)功能障碍可能与血管供应功能障碍密切相关。血管周围空间(PVS)是连接神经血管单元和大脑血管的组成部分之一,位于小血管和神经元之间的界面,是清除代谢物如β淀粉样蛋白(Aβ)的途径。

图1: 论文封面图
动物研究表明,随着动脉血管向脑微循环过渡,大动脉血管周围的PVS过渡到虚拟空间,在微循环水平上富含水蒸发蛋白4通道,形成血脑屏障的一部分,参与与脑实质间的液体和代谢物交换。在AD患者中发现血管周围的水通道蛋白4减少,并与Aβ沉积和Braak阶段的增加有关。其他使用共聚焦显微镜的动物研究显示了体内血管周围流动的可视化,并进一步表明血管周围流动可能因高血压而受损,这表明血管周围流动的功能障碍可能与高血压等血管风险因素的不利影响有关。
磁共振成像(MRI)上可见的血管周围空间可以被量化,并可能反映CSVD和代谢物清除途径的功能障碍(即肝功能障碍)。无症状者的血管周围引流功能障碍和CSVD可能在多年后逐渐发展。因此,MRI上可见的PVS的检测和量化可作为血管风险和神经变性的亚临床标志物,可能是对有痴呆风险的个体进行早期风险分层的有用工具。然而,先前的荟萃分析发现,PVS和认知障碍的关系存在矛盾的证据,研究之间存在明显的异质性,方法也存在差异,这就需要更多的研究来帮助确定PVS在神经退行性疾病中的潜在病理生理学参与。鉴于美国和世界范围内痴呆症的流行比例,早期发现高风险的个体成为一项重要的任务;而早期风险分层又对痴呆症有效预防措施的界定和实施至关重要。
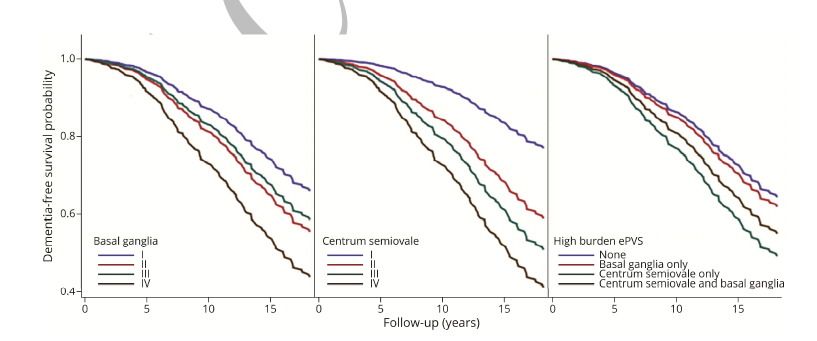
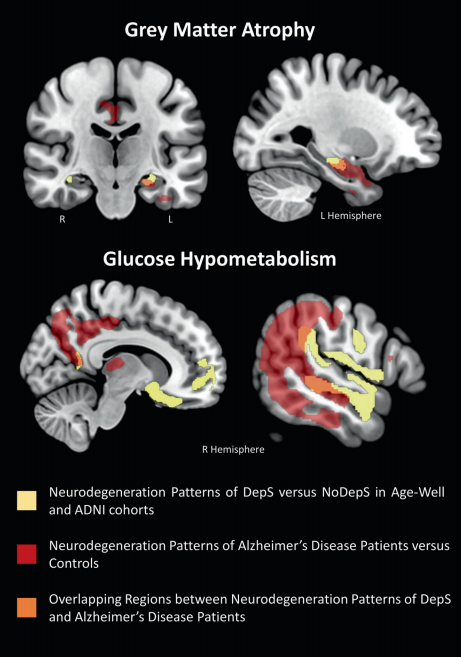
图2:论文结果图
除了作为痴呆症风险的早期标志物的潜在作用外,PVS可能反映了最常见的散发性CSVD形式的影响:高血压动脉病(主要影响深部脑区)和脑淀粉样血管病(CAA,影响脑叶区),混合分布代表两者的相互作用或晚期高血压血管损伤。在尸检研究中,这些动脉病变的发病率约占老年人的10%至30%,占所有痴呆症患者的35%至90%。因此,PVS可能代表一种高度相关的亚临床生物标志物,反映了痴呆症病理生理学的关键方面。
藉此,波士顿大学的Jose Rafael Romero等,在一个大样本的社区居民中评估PVS与痴呆症的关系,并根据PVS的大脑地形评估这种关系的差异。
该研究纳入了社区居住的弗雷明汉心脏研究原始和后代队列参与者,他们有可用的脑部MRI-PVS评分,没有中风和痴呆症。采用多变量Cox比例危害回归法获得MRI可见的PVS与发生痴呆症之间的危险比(HR)和95%置信区间(CI)。使用有效的方法对基底节(BG)和半卵圆中心(CSO)的PVS进行评级。结果包括全因性痴呆、阿尔茨海默氏痴呆(AD)和血管性痴呆。
1449名50岁或以上的参与者(46%为男性)被纳入。在8.3年的中位随访期内,全因性痴呆、阿尔茨海默病和血管性痴呆的发生率分别为15.8%、12.5%和2.5%。
在调整了血管危险因素和心血管疾病的模型中,痴呆的危险随着PVS负担的增加而稳步上升,与CSO的I级PVS相比,II级PVS的参与者上升了2倍(HR 2.44,95% CI 1.51 - 3.93),IV级参与者上升了5倍(HR 5.05,95% CI 2.75 - 9.26)。在BG中,与I级PVS相比,II级的危害增加了1.6倍(HR 1.62,95% CI 1.15 - 2.27),而IV级增加了2.6倍(HR 2.67,95% CI 1.04 - 6.88)。
在调整了白质高密度体积、隐蔽性梗死和总脑体积后,这种关联对CSO仍有意义,但对BG没有意义。
对AD也有类似的发现,但血管性痴呆因事件数量少而受到限制,没有统计学意义。
CSO中较高的PVS负担与发生痴呆的风险增加有关,与血管危险因素、总脑和白质高张力体积和隐蔽性梗死无关。这一发现支持PVS作为亚临床MRI标志物的作用,以识别处于亚临床阶段的高风险痴呆症患者,他们可能从早期干预中受益。
原文出处:
MRI Visible Perivascular Spaces and Risk of Incident Dementia: The Framingham Heart Study. Jose Rafael Romero, Adlin Pinheiro, Hugo J. Aparicio, Charles S.DeCarli, Serkalem Demissie, Sudha Seshadri; Neurology Sep 2022, 10.1212/WNL.0000000000201293; DOI:10.1212/WNL.0000000000201293
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言