Trastuzumab Deruxtecan治疗HER2阳性乳腺癌效果优于trastuzumab emtansine
2022-04-26 健康界 网络
尽管 HER2 靶向疗法改善了疾病预后,但它们不能治愈局部晚期或转移性疾病,并且大多数患者会出现疾病进展。
前言
乳腺癌(breast cancer,BC)是全世界女性中最常被诊断出和最致命的癌症,其中大约 20% 的女性患者为人表皮生长因子受体2(human epidermal growth factor receptor 2,HER2)阳性乳腺癌。尽管 HER2 靶向疗法改善了疾病预后,但它们不能治愈局部晚期或转移性疾病,并且大多数患者会出现疾病进展。对于治疗后疾病进展的患者,标准的二线治疗是T-DM1,是一种抗体-药物偶联物,结合了曲妥珠单抗的HER2靶向抗肿瘤特性和微管抑制剂 DM1的细胞毒活性。抗体和细胞毒剂通过稳定的接头缀合。T-DM1治疗的中位无进展生存期为9.6个月,中位总生存期为30.9个月。
而Trastuzumab Deruxtecan(T-DXd 和DS-8201)是一种新型ADC,是HER2靶向抗体和DNA拓扑异构酶Ⅰ抑制剂德卢替康(deruxtecan,DXd)的结合物。它设计独特,药物与抗体的比例高达大约8:1,并保持稳定,从而提供了强大的细胞毒性载荷,被癌细胞中过度表达的溶酶体内化并选择性地裂——这一过程可能会减少全身毒性作用。既往研究中表明,接受T-DXd的患者中有 60.9%[95% CI为(53.4,68.0)]总体缓解(完全或部分缓解),中位无进展生存期为 16.4 个月[95 % CI,(12.7,NE)]。这明显高于T-DM1。故近期NEJM上发表的一项研究比较了两个药物的治疗效果。
研究方法
该研究为一项3期、多中心、开放标签、随机对照实验。选择HER2阳性、先前接受过曲妥珠单抗联合紫杉醇治疗6个月内后疾病进展的BC患者参与研究,以1:1的比例随机接受T-DM1或T-DXd。2018 年 7 月 20 日-2020 年 6 月 23 日期间,共有 524 名 HER2 阳性转移性BC患者在 15 个国家的 169 个中心入组。总共有261名患者被随机分配到接受T-DXd,263名接受T-DM1给药疗程为:T-DXd每3周静脉注射一次,剂量为5.4mg/kg 体重,T-DM1每3周静脉注射一次,剂量为3.6mg/kg。使用T-DXd的中位随访时间为 16.2 个月(范围,0 ~32.7),使用曲妥珠单抗 emtansine 的中位随访时间为 15.3 个月(范围,0 ~ 31.3)。研究的主要终点为无进展生存期,次要终点包括总生存期、客观应答以及安全性。
研究结果
T-DM1
①T-DXd治疗在无进展生存期方面比T-DM1有优势。T-DXd组的无进展生存期中位数未达到(95%CI,18.5至无法估计),T-DM1组为6.8个月(95%CI,5.6~8.2)。T-DXd组12个月后无进展生存率为75.8%,而T-DM1组为34.1%(全因死亡或疾病进展风险为0.28),如图1A。亚组分析显示,在所有亚组中,T-DXd比T-DM1更有利于无进展生存期(由盲法独立中心审查评估),包括根据以前治疗的行数定义的亚组。在没有接受过任何治疗线或只接受过一个治疗线的患者中,疾病进展或因任何原因死亡的危险比为0.33,在接受过两个或更多治疗线的患者中为0.28(图1B)。
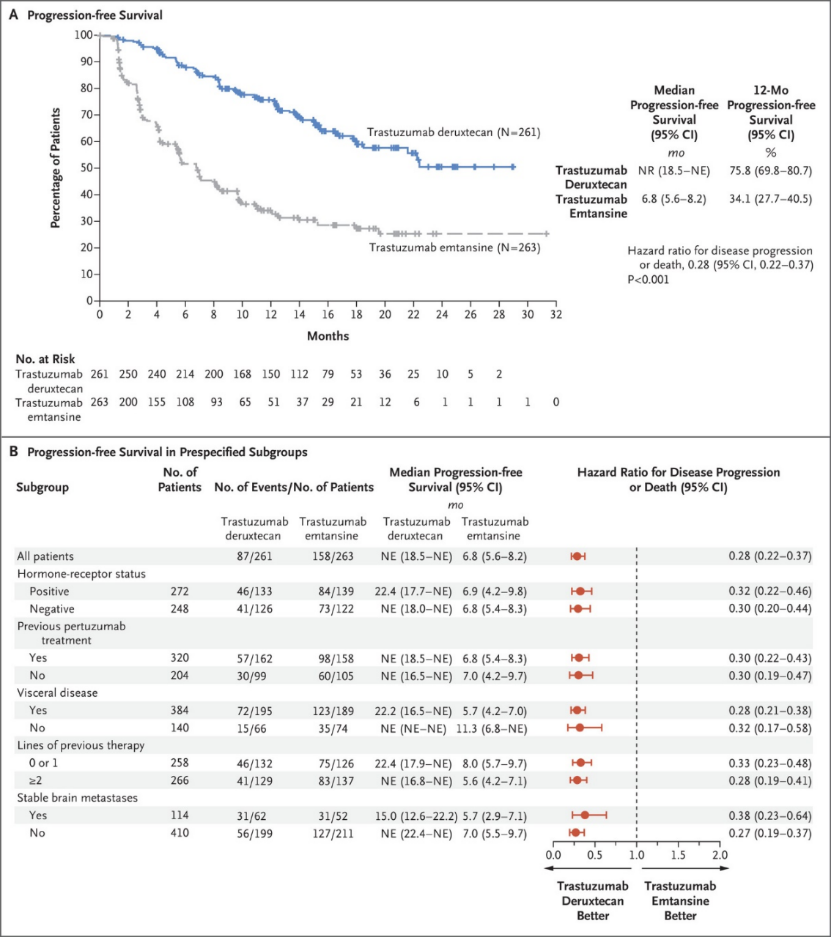
图1 无生存发展的 Kaplan-Meier 分析和亚组分析
图1A 显示了意向治疗人群(所有随机分配的患者)中的无进展生存期的 Kaplan-Meier 估计值;图1B 显示了根据激素受体状态、既往帕妥珠单抗治疗定义的亚组中无进展生存期的风险比和 95% 置信区间(CI)
②在中期分析的数据截止时,使用T-DXd的患者在12个月内存活的比例为94.1%[95%CI(90.3,96.4)],使用T-DM1的患者为85.9%(95%CI(80.9,89.7)](图2)。治疗组之间的差异没有达到预设的显著性界限(P<0.000265),死亡危险比[0.55;95%CI(0.36,0.86),P=0.007];P=0.007。截至数据截止日,T-DXd组261名患者中共有33人(12.6%)和T-DM1组263名患者中共有53人(20.2%)已经死亡。
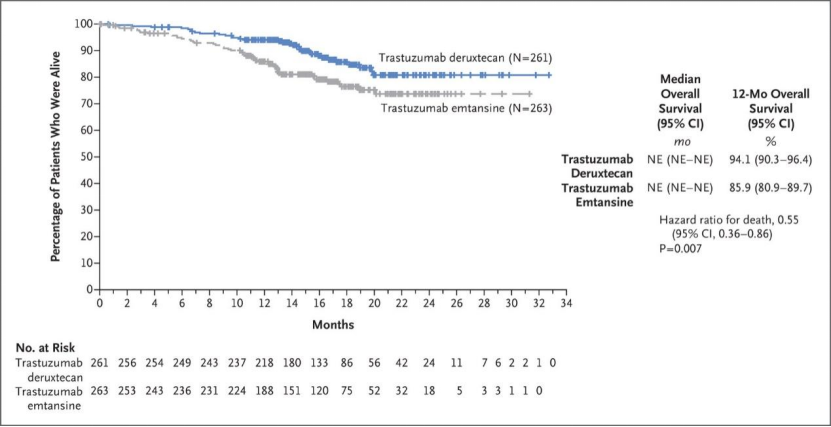
图2 受试者12 个月总生存期的 Kaplan-Meier 估计值
③图3显示的是患者中可测量肿瘤的最大直径总和相对于基线的最佳百分比变化:接受T-DXd 的 261 名患者中有 245 名(图 3A ) 和 263 名T-DM1的患者中的 228 名(图 3B)。上面的水平虚线表示疾病进展患者的肿瘤大小增加了 20%,下面的虚线表示肿瘤大小减少了 30%(部分反应)。T-DXd组治疗响应率为79.7%,T-DM1组为34.2%。T-DXd组的疾病控制(定义为完全反应、部分反应或疾病稳定)的患者比例为96.6%,T-DM1组为76.8%。
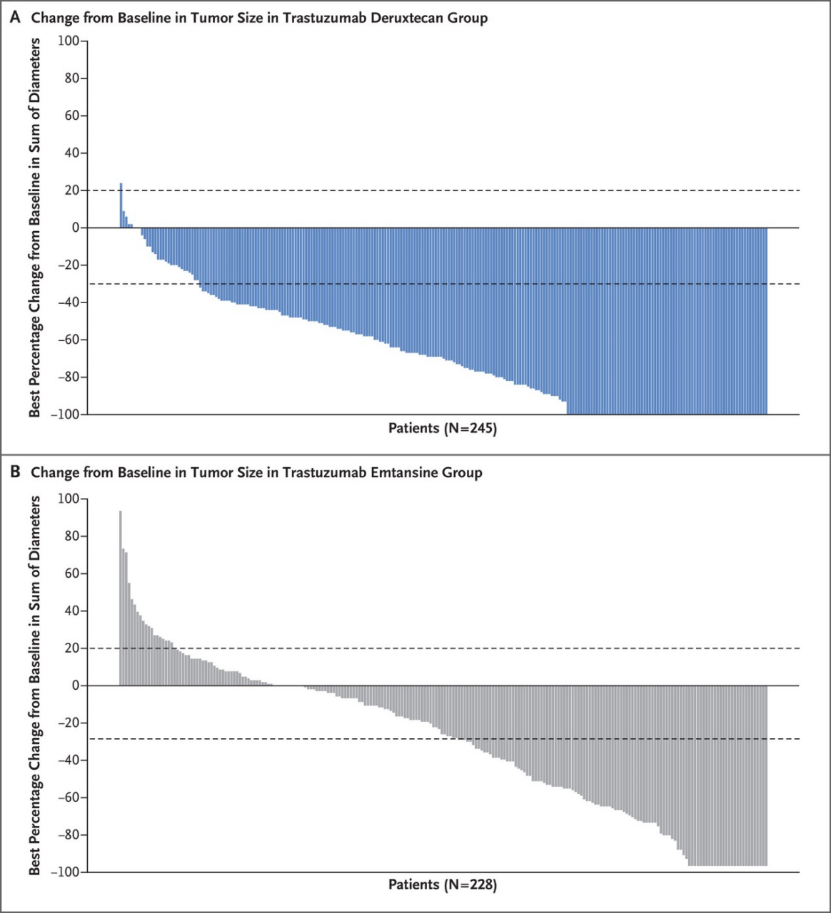
图3 药物抗肿瘤活性
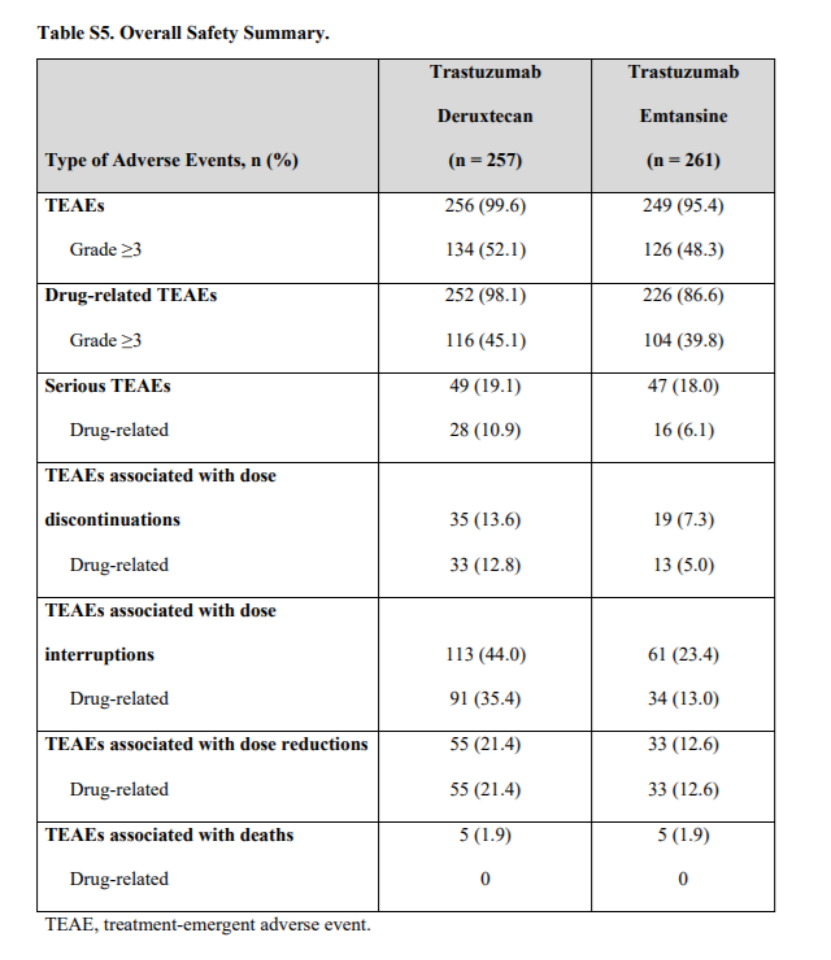
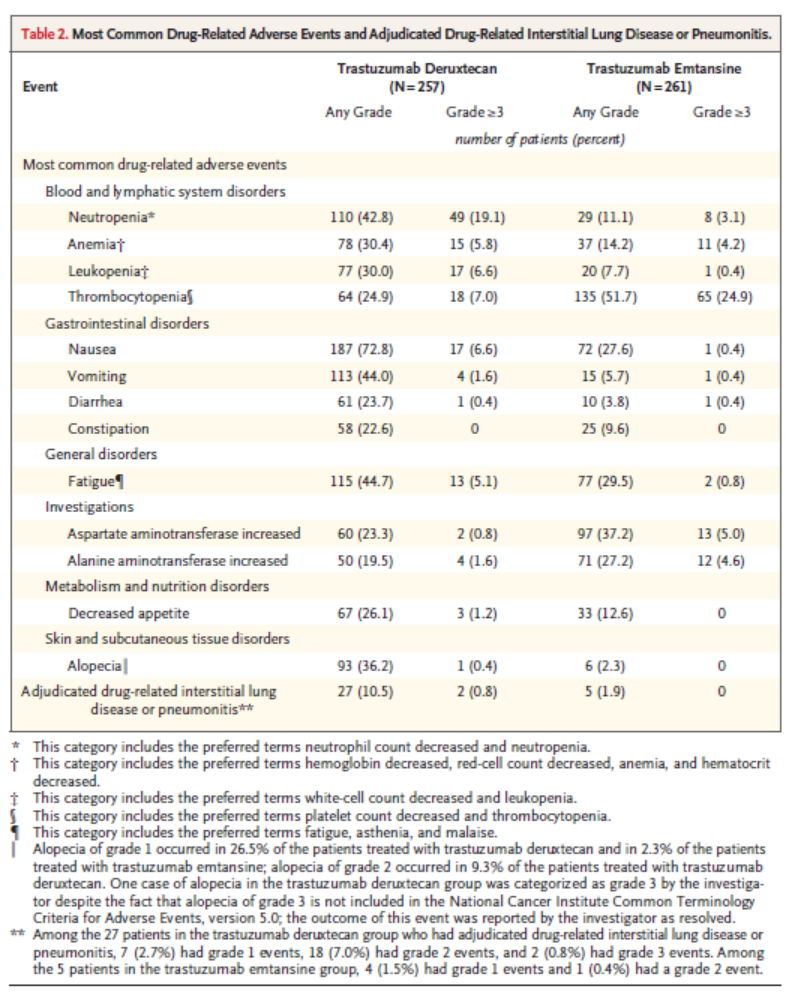
④安全性:T-DXd组的中位治疗时间为14.3个月(范围为0.7至29.8),T-DM1组为6.9个月(范围为0.7至25.1)。T-DXd组和T-DM1组在治疗开始后的不良事件发生率相似(分别为99.6%和95.4%)(表S5)。T-DXd组257名患者中有49名(19.1%)报告了严重不良事件,T-DM1组261名患者中有47名(18.0%)报告了严重不良事件。导致试验治疗中止的不良事件的发生率,T-DXd高于T-DM1(13.6%对7.3%)。具体不良反应如表2所示.T-DXd组报告的最常见的任何等级的药物相关不良事件是恶心(72.8%的患者)、疲劳(44.7%)和呕吐(44.0%);这些事件在T-DM1组的发生率都比较低(分别为27.6%、29.5%和5.7%)。见表2,T-DXd组有36.2%的患者发生任何等级的药物相关脱发,T-DM1组有2.3%。T-DXd组治疗开始后发生的最常见的3级或4级药物相关不良事件是中性粒细胞减少(19.1%)、血小板减少(7.0%)、白细胞减少(6.6%)和恶心(6.6%);T-DM1组的患者中分别有3.1%、24.9%、0.4%和0.4%报告了这些事件。两种治疗方法都没有报告5级的药物相关不良事件。
研究结果
研究结果表明,对于此前接受曲妥珠单抗和紫杉烷治疗的HER2阳性转移性乳腺癌患者,曲妥珠单抗-deruxtecan治疗与曲妥珠单抗-emtansine治疗相比,可显著降低患者的疾病进展或死亡风险。更多靶向HER2抗体药物偶联物(antibody-drug conjugate,ADC)治疗效果值得期待。
研究结论
对于接受过曲妥珠单抗联合紫杉醇治疗后出现疾病进展的HER2阳性转移性乳腺癌患者,接受T-DXd治疗在降低疾病进展或死亡风险方面优于T-DM1。
文献解读
该研究证明,T-DXd的无进展生存时间明显长于T-DM1,且进行疾病史,既往治疗方式,激素受体状态进行亚组分析后,T-DXd组依旧显示更低的疾病进展或死亡风险。T-DXd组死亡率也更低,从而证明排除一般混杂因素后T-DXd具有更好的治疗效果。但是两者同样存在较高不良反应风险。T-DXd等靶向HER2ADC也正在探索用于HER2低表达的疗效,目前不断涌现出新的HER2阳性乳腺癌靶向治疗药物及治疗方案。通过不同的用药方案、用药时长以及分层研究的对比,临床上进一步完善并细化了相关药物新兴治疗方案的制定与使用,更多的用药选择带来的积极影响也促进了相关靶向药物的新药研发。但是其用药后安全性仍需进一步的探讨,本文中两种药物都存在较高的不良事件报告率,说明在不断研发治疗药物和提高治疗方案的同时,需要更多关注如何降低不良事件发生。T-DXd有显著的抗肿瘤活性,临床试验数据提供了有效的证据支持,如何针对不同药物进行个体精准化的治疗是临床实践中的重点。
原文出处
Cortés J, Kim SB, Chung WP, et al. Trastuzumab Deruxtecan versus Trastuzumab Emtansine for Breast Cancer. N Engl J Med. 2022;386(12):1143-1154.
DOI:10.1056/NEJMoa2115022.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#mAb#
34
#TRA#
44
#AST#
31
#TEC#
43
#deruxtecan#
33
#emtansine#
27
#HER2阳性#
49
#MTA#
35
#EMT#
46