Cell :中风治疗新篇章-抑制细胞铁死亡
2019-05-31 佚名 转化医学网
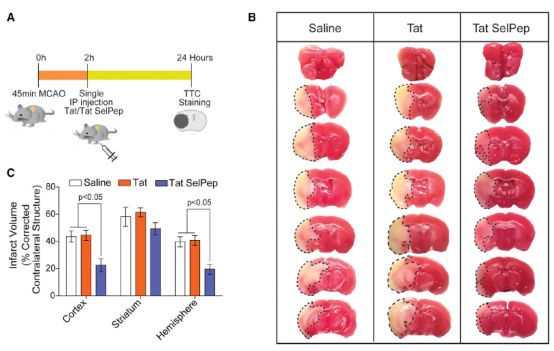
研究发现神经元通过诱导硒蛋白(包括谷胱甘肽过氧化物酶4(GPX4))对铁死亡相关刺激做出反应。硒(Se)可在铁死亡过程中增强GPX4和其它基因的转录,通过共激活转录因子TFAP2c和Sp1来保护神经元,在中风的营养和治疗中有重要意义。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






从坏调,到焦亡,再到铁死亡,会不会在发现更多的程序性死亡
101
#Cell#
35
#CEL#
38
#新篇章#
41
中风是俗称,应该称为缺血性卒中吧
54