2023年Q1 FDA批准了13款新药上市
每年FDA批准的新药,都是成为国际研发的风向标。在2023年Q1(至3月23日),FDA批准了哪些新药上市了呢?梅斯小编为您详细整理如下。初步看来涉及到肿瘤,阿尔茨海默病,罕见病,糖尿病,蛋白尿,偏头
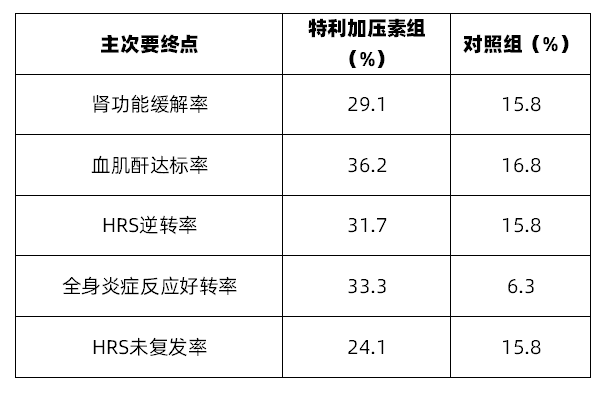
FDA批准达普司他(Daprodustat)上市用于慢性肾病贫血
据葛兰素史克2月1日公布,美国FDA已批准其口服缺氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI)Jesduvroq(daprodustat,中文译名:达普司他),用于每日一次治疗接受透析至少四个月的成
FDA批准仑卡奈单抗(Lecanemab)治疗阿尔茨海默病
FDA加速批准由卫材(Eisai)和渤健(Biogen)联合开发的仑卡奈单抗(Lecanemab)(商品名Leqembi)用以治疗阿尔茨海默病(AD)!Lecanemab是近年来靶向β淀粉样
梅斯盘点:FDA在2022年度批准的创新药(上)
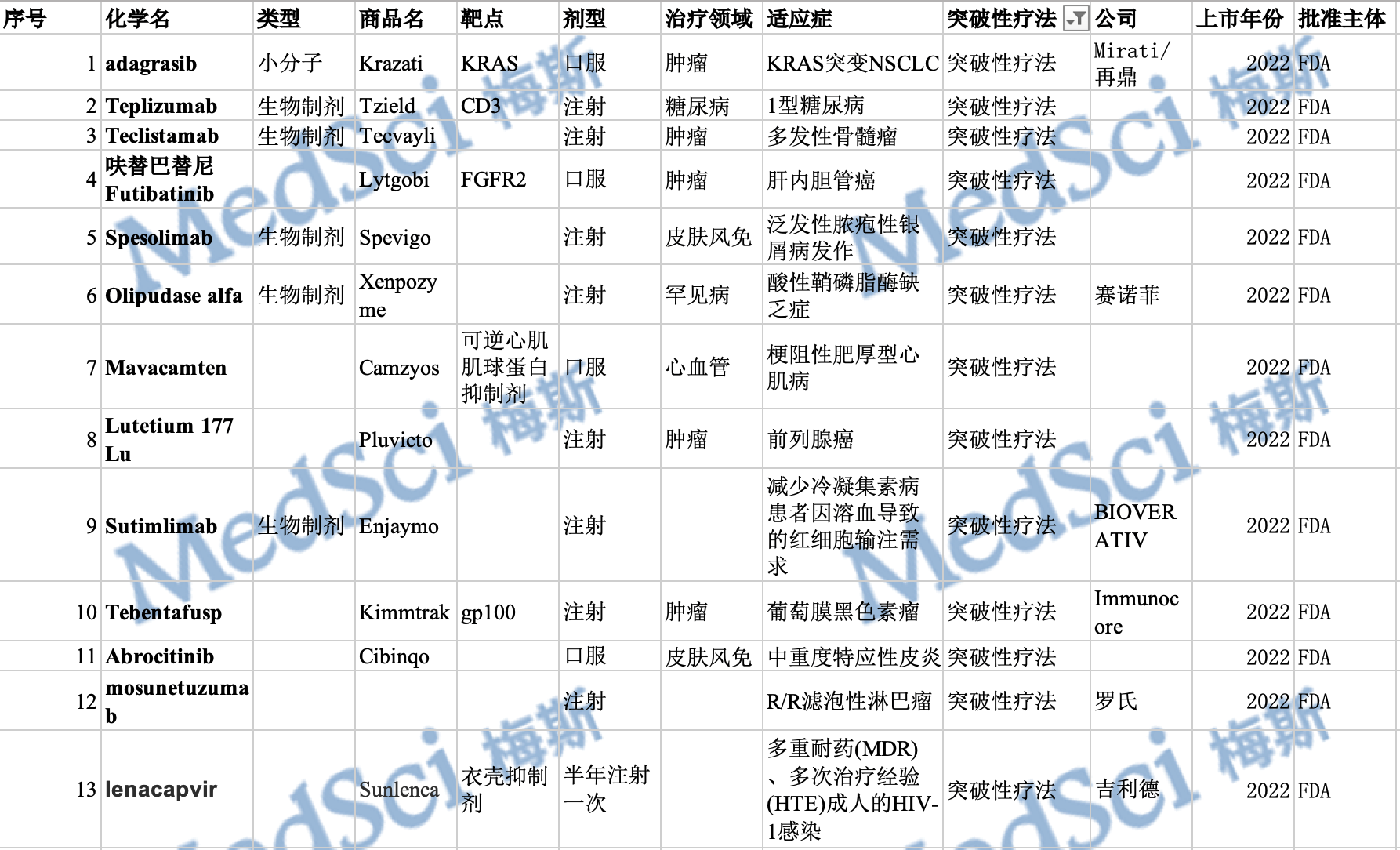
2022年即将结束,截至今年12月30日,美国FDA的药物评估和研究中心(CDER)已经批准了37款创新药。FDA的生物制品评估和研究中心(CBER)也批准了至少15项生物制品许可申请(BLA)。虽然
梅斯盘点:FDA在2022年度批准的创新药(下)
截至2022年12月30日,美国FDA的药物评估和研究中心(CDER)已经批准了37款创新药。FDA的生物制品评估和研究中心(CBER)也批准了至少15项生物制品许可申请(BLA)。虽然与往年相比,今
FDA批准lumasiran治疗原发性高草酸尿症1型,Alnylam的RNAi帝国再下一城!
近日,FDA批准了Alnylam的RNAi药物lumasiran的新适应症,通过降低血浆中的草酸盐水平来治疗原发性高草酸尿症1型(又称Ph1)这种罕见的遗传性疾病。主要基于一系列临床试验结果,见:NE
FDA现代化法案2.0:新药研发中减少动物实验是大趋势
9月29日,美国参议院在没有异议的情况下,通过FDA现代化法案2.0(FDA Modernization Act 2.0,S.5002),向制定一项政策迈出重要一步。法案链接:打开FDA现代化法案2.
PI3K抑制剂Duvelisib(度维利塞)或将遭FDA撤市
9月23日,据fiercepharma报道,FDA外部癌症专家组成的咨询会最终以8比4的投票结果反对PI3K抑制剂Copiktra(Duvelisib,度维利塞)三线治疗慢性淋巴细胞白血病(CLL)/
FDA上市前激活进口请求 (PLAIR)
本指南最终确定了 2013 年 7 月的上市前激活进口请求 (PLAIR) 指南草案,该指南描述了 FDA 关于根据预期批准准备在美国上市的产品的申请人进口未经批准的成品剂型药物产品的政策。 未决新药