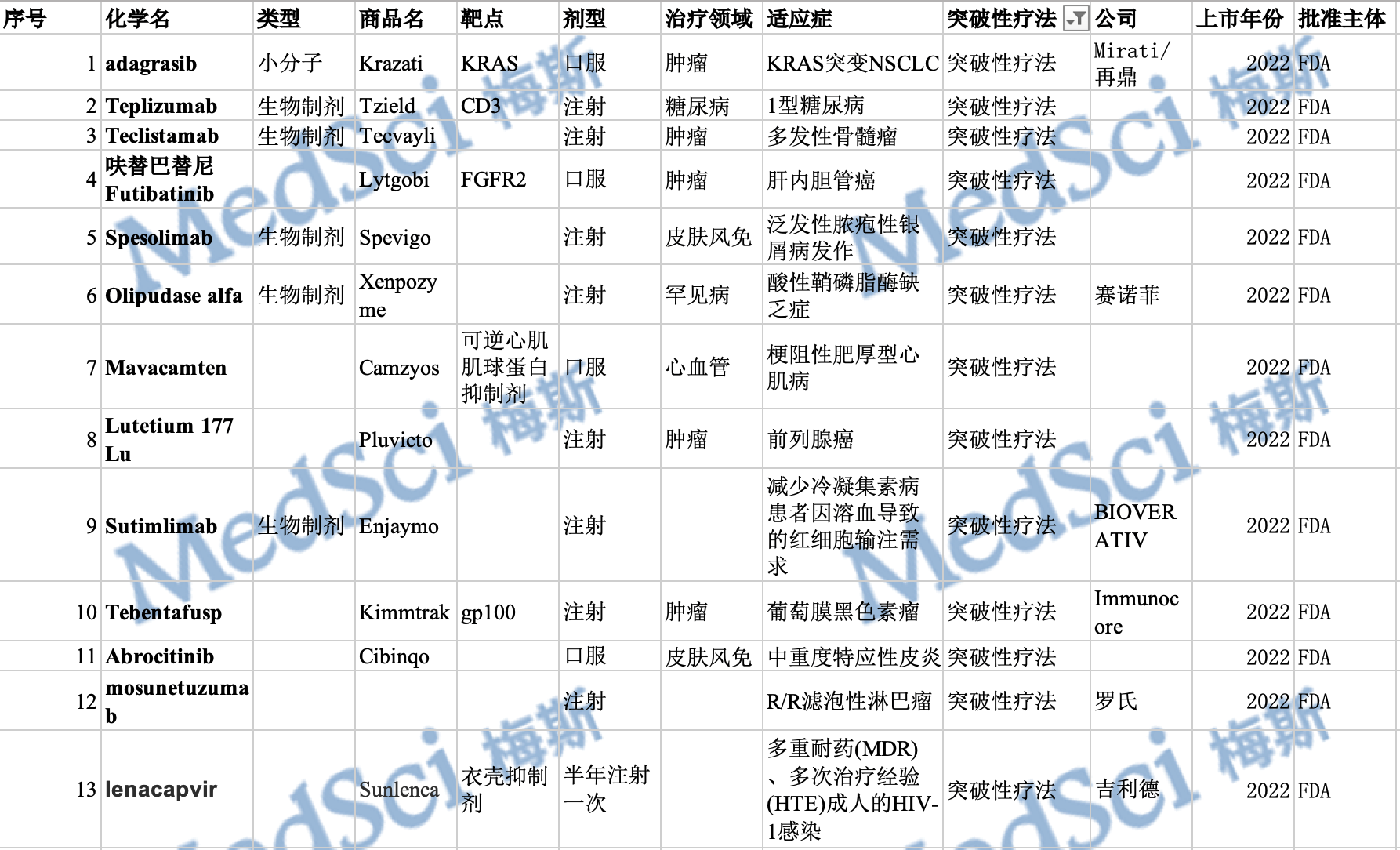
梅斯盘点:FDA在2022年度批准的创新药(下)
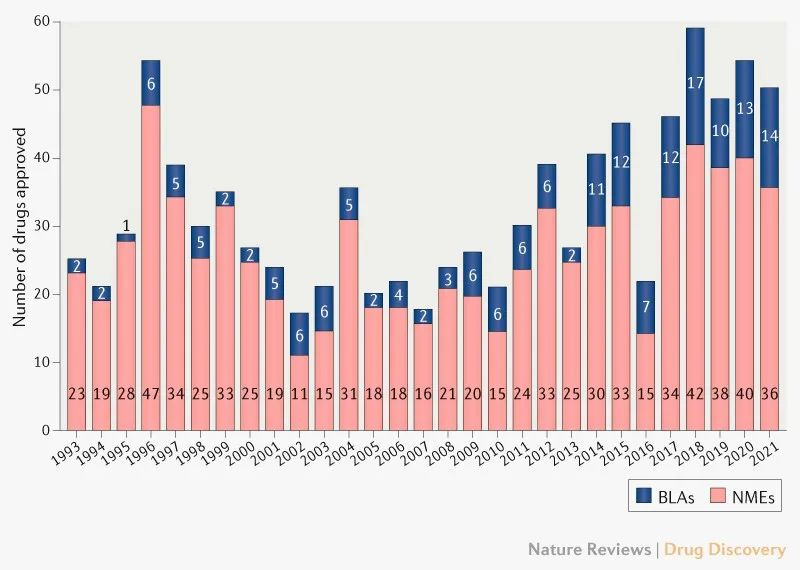
截至2022年12月30日,美国FDA的药物评估和研究中心(CDER)已经批准了37款创新药。FDA的生物制品评估和研究中心(CBER)也批准了至少15项生物制品许可申请(BLA)。虽然与往年相比,今
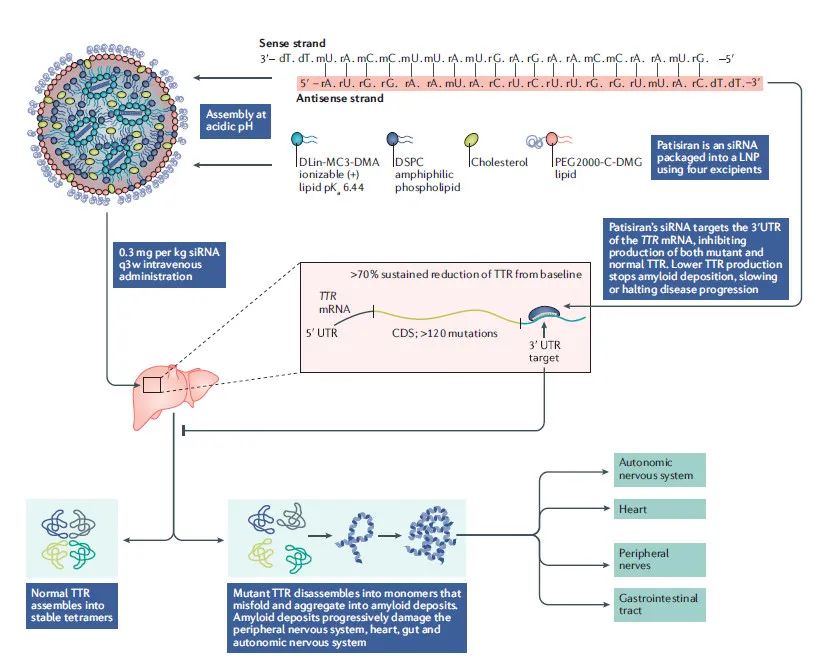
FDA批准lumasiran治疗原发性高草酸尿症1型,Alnylam的RNAi帝国再下一城!
近日,FDA批准了Alnylam的RNAi药物lumasiran的新适应症,通过降低血浆中的草酸盐水平来治疗原发性高草酸尿症1型(又称Ph1)这种罕见的遗传性疾病。主要基于一系列临床试验结果,见:NE
FDA现代化法案2.0:新药研发中减少动物实验是大趋势
9月29日,美国参议院在没有异议的情况下,通过FDA现代化法案2.0(FDA Modernization Act 2.0,S.5002),向制定一项政策迈出重要一步。法案链接:打开FDA现代化法案2.
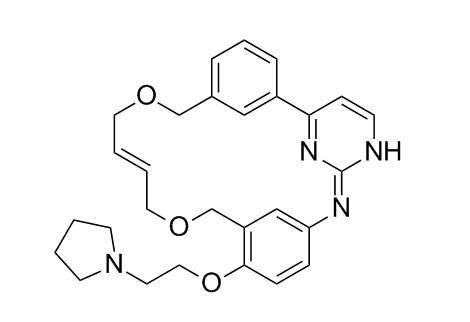
PI3K抑制剂Duvelisib(度维利塞)或将遭FDA撤市
9月23日,据fiercepharma报道,FDA外部癌症专家组成的咨询会最终以8比4的投票结果反对PI3K抑制剂Copiktra(Duvelisib,度维利塞)三线治疗慢性淋巴细胞白血病(CLL)/
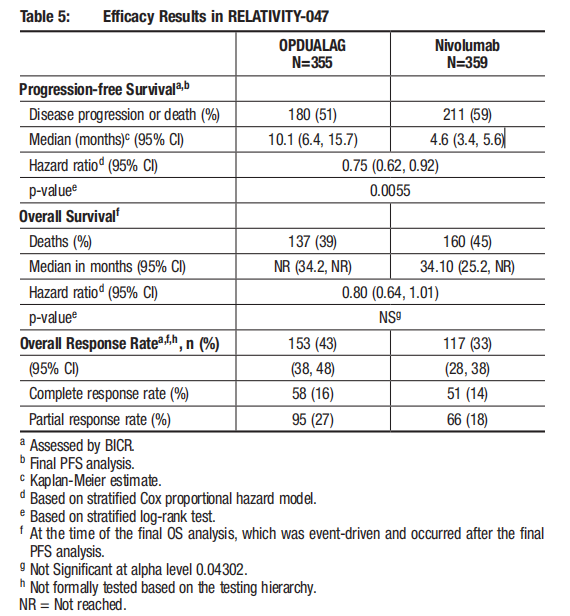
FDA批准LAG-3抗体Relatlimab联合Nivolumab用于不可切除或转移性黑色素瘤的儿童和成人患者
2022年3月18日,FDA正式批准百时施贵宝(BMS)公司LAG-3抗体Relatlimab联合PD-1抗体Nivolumab,用于治疗12岁或以上患有不可切除或转移性黑色素瘤的儿童和成人患者。这是
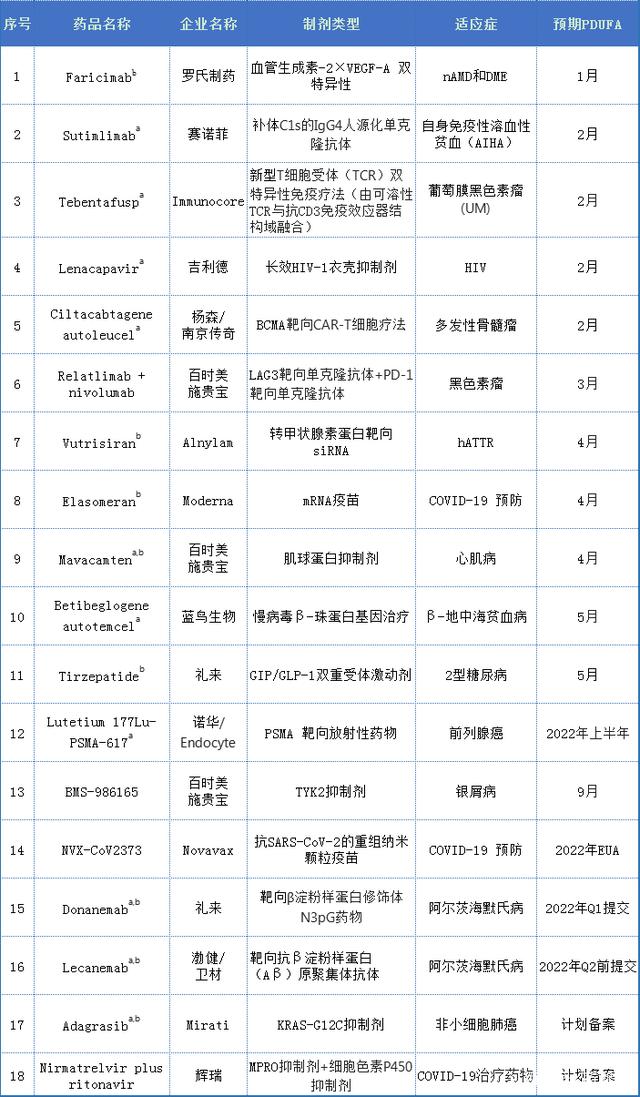
2022年FDA有望批准的18款创新疗法
近日,FDA发布2021年药物审评审批报告,获批50种新药,低于2020年53种,包括具有里程碑意义的mRNA疫苗与两款CAR-T细胞疗法、多款ACD新药、颇具有争议的阿兹海默症Aduhelm....