生物可吸收冠状动脉药物洗脱支架临床试验指导原则(2019年第8号)
为了进一步规范生物可吸收冠状动脉药物洗脱支架产品上市前的临床试验,并指导该类产品申请人在申请产品注册时临床试验资料的准备,制订本指导原则。
FDA研究数据技术一致性指南 v4.5.1(2020年7月更新)
本《研究数据技术一致性指南》提供了关于如何使用位于FDA数据标准目录(目录)中的FDA支持的数据标准提交标准化研究数据的规范、建议和一般考虑。该指南补充了《以电子格式提供监管报告》的行业指南,即:《标
最新版CIOMS伦理准则:适用于指导全球的健康研究
在国际医学科学组织理事会(Council for International Organizations of Medical Sciences,CIOMS)和上海医药临床研究中心的大力支持下,201
儿童临床试验伦理审查规范(重庆标准)
伦理委员会的审查监督是儿童受试者安全和权益的重要保障,为进一步加强儿童临床试验中受试者的保护,规范儿童临床试验伦理审查,在严格遵循国际准则及国内相关法律法规的基础上,建议加强以下各方面伦理考量,建立儿
HRPS/CR 01-2017 涉及人的生物医学研究伦理审查体系要求
世界中医药学会联合会于近日发布了关于执行新版本认证规则和技术规范的通知,现将新版技术规范《HRPS/CR 01-2017 涉及人的生物医学研究伦理审查体系要求》全文发布如下,供相关单位和技术人员参考。
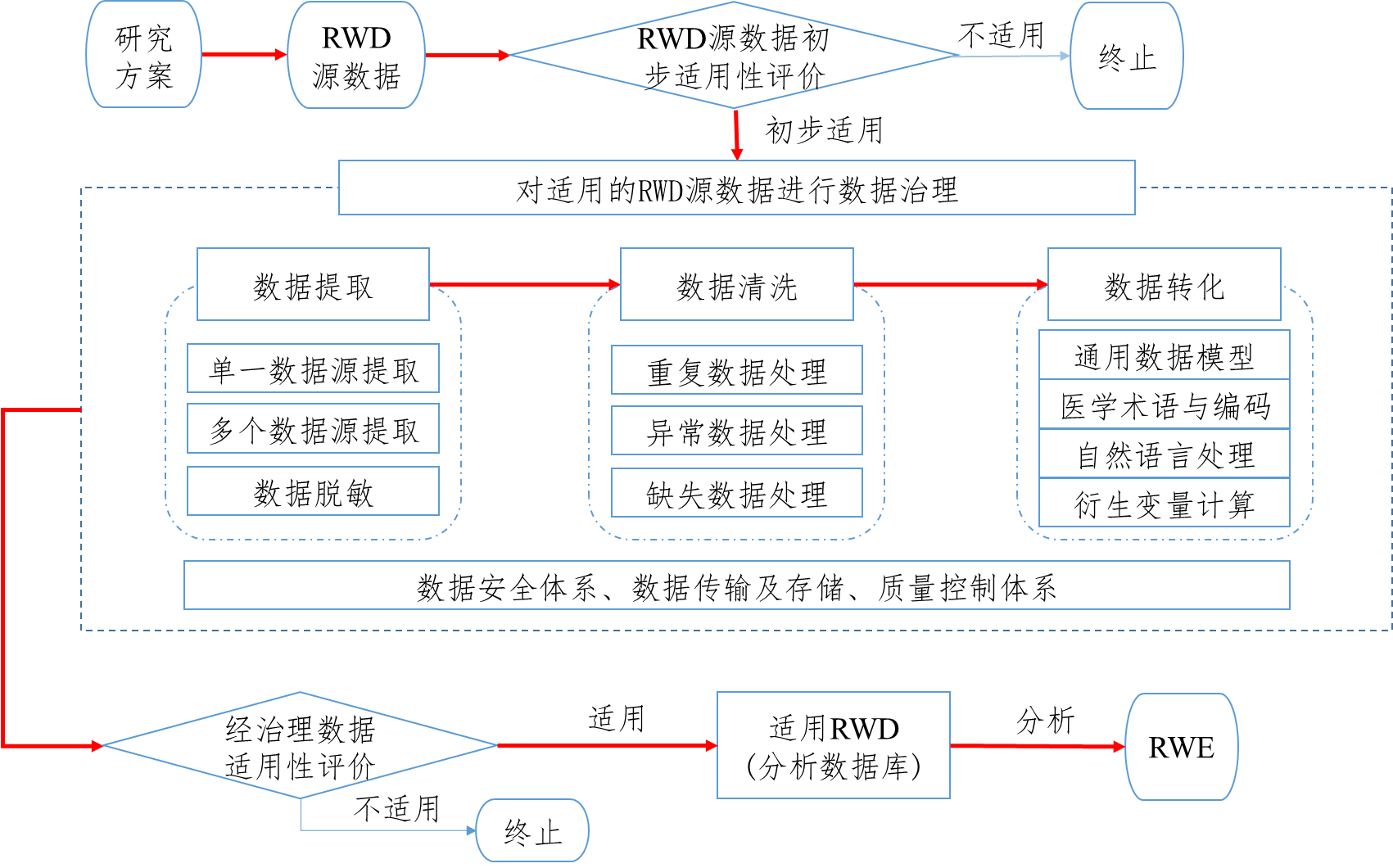
用于产生真实世界证据的真实世界数据指导原则(征求意见稿)
为进一步指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发,我中心组织起草了《用于产生真实世界证据的真实世界数据指导原则(征求意见稿)》,现在中心网站予以公示,以广泛听取各界意见和建议,欢迎