FDA批准Nivolumab,肝癌开启免疫治疗新时代
9月23日,FDA批准Nivolumab(纳武单抗,以下简称O药)用于接受过索拉非尼治疗后的肝细胞癌(HCC)患者,标志着肝癌治疗正式进入免疫时代。
癌度 - 肝癌,免疫治疗,纳武单抗,FDA - 2017-10-07
FDA批准百时美Opdivo(nivolumab)治疗经典型霍奇金淋巴瘤
FDA已加速批准百时美Opdivo(nivolumab)用于经典型霍奇金淋巴瘤(cHL)患者的治疗。
MedSci原创 - Opdivo,Nivolumab,霍奇金淋巴瘤,PD-1 - 2016-05-18
澳大利亚TGA批准OPDIVO(nivolumab)治疗肝癌
Bristol-Myers Squibb于2018年9月21日宣布,澳大利亚治疗用品管理局(TGA)已批准OPDIVO(nivolumab)用于治疗先前接受过索拉非尼治疗的肝癌患者。
MedSci原创 - TGA,澳大利亚,Nivolumab,肝癌 - 2018-09-24
FDA:PD-1免疫疗法Opdivo(nivolumab)再获批准——单药一线治疗BRAF野生型黑色素瘤
免疫治疗领域的王者——百时美施贵宝(BMS)近日宣布,FDA已批准PD-1免疫疗法Opdivo(nivolumab)作为一种单药疗法,用于BRAF V600野生型(wild-type,WT)不可切除性或转移性黑色素瘤患者的治疗此次批准,是Opdivo在过去一年(12个月)收获的第6个FDA批准,同时也标志着Opdivo成为PD-1/PD-L1领域首个也是唯一一个获批用于一线治疗BRAF野生型黑色
生物谷 - 基因治疗 - 2015-12-01
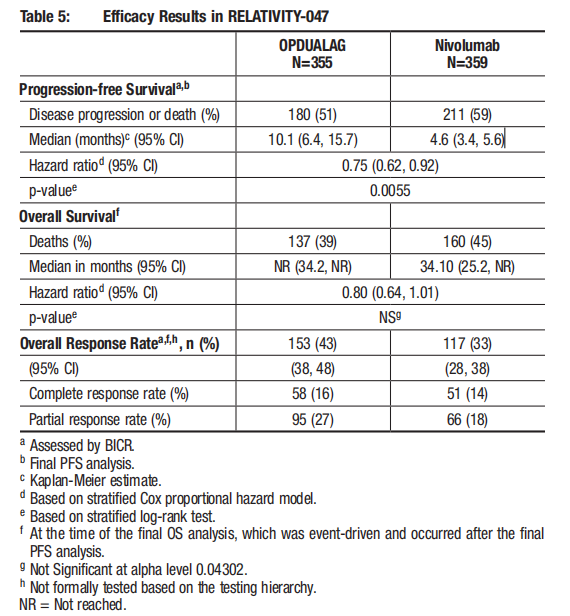
FDA批准LAG-3抗体Relatlimab联合Nivolumab用于不可切除或转移性黑色素瘤的儿童和成人患者
2022年3月18日,FDA正式批准百时施贵宝(BMS)公司LAG-3抗体Relatlimab联合PD-1抗体Nivolumab,用于治疗12岁或以上患有不可切除或转移性黑色素瘤的儿童和成人患者。这是
MedSci原创 - FDA,Relatlimab - 2022-03-19
SMC 批准首个针对罕见突变晚期肠癌患者的免疫治疗组合(Nivolumab联合ipilmumab)
Nivolumab联合ipilmumab已被苏格兰药物联盟 (SMC) 批准为成人患者的治疗选择,用于治疗以前基于氟嘧啶的化疗失败的患者。
MedSci原创 - Nivolumab,ipilmumab - 2021-12-19
FDA:强生Simponi Aria获FDA批准用于RA
强生(JNJ)旗下杨森(Janssen)19日宣布,FDA已批准将Simponi Aria(golimumab,戈利木单抗)静脉输液剂(for infusion)联合甲氨蝶呤(methotrexate
生物谷 - 新药,FDA - 2013-07-24
FDA批准Vaxchora霍乱疫苗上市
美国食品和药物管理局(FDA)批准Vaxchora作为预防旅客霍乱的疫苗。Vaxchora(单剂量活霍乱疫苗,PaxVax)是专门针对O1群霍乱的疫苗,该亚群也是造成霍乱的主要原因。Vaxchora曾经获得过快速疫苗接种和优先审查资格,是唯一一种被FDA批准用于预防霍乱的疫苗。此次FDA批
MedSci原创 - FDA,Vaxchora,霍乱,疫苗 - 2016-06-11
FDA批准Belviq用于体重控制
Arena制药公司和Eisai制药公司宣布FDA批准Belviq(lorcaserin HCl) 用于肥胖成年人的慢性体重管理圣地亚哥和新泽西克利夫湖,美通社2012年6月27日报道,Arena 制药有限公司和Eisai制药有限公司今天宣布美国食品药品监督管理局已经批准Belviq(由BEL-VEEK公司研制的)作为针对在肥胖成年患者当中低卡热量饮食和较多的增加运动的一种补充品。
丁香园 - FDA,Belviq,肥胖症 - 2012-08-09
美国FDA批准首个干眼症新药
Shire公司宣布美国FDA已经批准其新药Xiidra滴眼剂溶液(5%浓度的lifitegrast眼用溶液)上市,每日使用两次,治疗成人干眼症患者。
生物谷 - FDA,干眼症,新药 - 2016-07-13
Rigel的Tavalisse获得FDA批准
Rigel制药公司已获得FDA首次批准,将Tavalisse推向市场,用于治疗对先前治疗无效的成人慢性免疫性血小板减少症(ITP)。
MedSci原创 - Rigel,FDA批准 - 2018-04-18
FDA提前三个月批准施贵宝PD-1抑制剂Nivolumab(Opdivo),与Keytruda同价
今天FDA批准了施贵宝PD-1抑制剂Nivolumab(商品名Opdivo)作为末线药物治疗黑色素瘤。这比原计划的PDUFA时间(2015年3月) 提前三个多月,显示FDA对真正创新药物的友好态度。这是2011年以来批准的第七个黑色素瘤药物,而2011年以前转移黑色素瘤几乎没有治疗办法。这也是继默克Keytruda之后第二个在美国上市的PD-1抑制剂。免疫哨卡抑制剂的竞争全面展开。
美中药源 - PD-1抑制剂,FDA - 2014-12-24
FDA:安斯泰来新药获美国FDA批准
据医药网Pharmaceutical Business Review周一报道,美国安斯泰来制药称,美国食品药品监督管理局批准了公司新肾药。
大智慧 - FDA,新药 - 2013-07-23
FDA批准治疗热带疾病新药
FDA日前批准Impavido(米替福斯)治疗热带病利什曼病(leishmaniasis),该病是苍蝇叮咬引起,由寄生虫传染给人类。Impavido由加拿大Paladin公司生产,被批准用于治疗3种主要类型利什曼病。 Impavido获得FDA快速审批,优先审查和罕用药资格认定。
医药经济报 - 新药,FDA - 2014-04-04
FDA批准Breo Ellipta用于COPD
圣路易斯(MD Consult)——2013年5月10日,美国食品药品管理局(FDA0)和葛兰素史克公司宣布Breo Ellipta(糠酸氟替卡松/维兰特罗吸入性粉剂)获准用作慢性阻塞性肺病(COPD
MDC - COPD - 2013-05-15
为您找到相关结果约500个