CDE和注册司专家发文:基于风险的监查(RBM)应用和挑战
作者:苏娴a,崔孟珣b(国家食品药品监督管理总局 a.药品审评中心,b.药品化妆品注册管理司,北京 100038) 来源:中国新药与临床杂志 2018年6月 第37卷第6期 摘要:本文结合国际人用药品注册技术要求协调会
中国新药与临床杂志 - CDE,风险的监查 - 2018-08-16
CDE发布中国新药注册临床试验进展年度报告(2022年)
9月7日,CDE官方公告显示,国家药监局药审中心发布《中国新药注册临床试验进展年度报告(2022年)》。
药研网 - 临床试验,CDE - 2023-09-10
2019年6月CDE药品审评情况报告
摘要· 6月CDE共承办药品注册申请628件· 恒瑞医药提交马来酸吡咯替尼新适应症临床申请· 正大天晴首家提交甲磺酸仑伐替尼胶囊仿制申请· 9个品种通过仿制药一致性评价· 69个受理号获临床试验默示许可总体承办情况:药品注册申请628个据MED中国药品审评数据库2.0统计,2019年6月CDE共承办药品注册申请628个。
米内网 - CDE,药品审评 - 2019-07-04
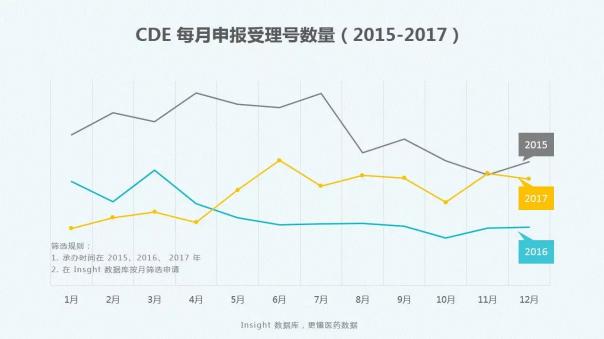
2017全年CDE药品审评报告
Insight数据库2017年终报告梳理了2017年CDE药品申报和审评的数据情况,让大数据来为你指路。
Insight数据库 - 药品审评,CDE,2017 - 2018-01-12
直播:从CDE新政看临床未满足需求
高博士, MedSci研究员/资深讲师, 拥有丰富的生物医药科研从业经历,对科研创新发现、基金申请与写作、研究设计等具有丰富的经验,对基金政策有较深的理解,培训和指导过大量年青专家
MedSci原创 - 2021-08-18
CDE发布征求CAR-T指导原则意见
嵌合抗原受体T细胞治疗产品具有新颖性、复杂性和技术特异性的特点,随着此类产品的研发进展和陆续申报上市,为促进企业及早发现此类产品的风险,提供有效地风险最小措施,确保上市后安全性风险可控,有必要对申报上
CDE - 2021-09-19
原料药、药用辅料和药包材注册申请不再单独受理,CDE建立登记平台
(厅字〔2017〕42号)与《国务院关于取消一批行政许可事项的决定》(国发〔2017〕46号),取消药用辅料与直接接触药品的包装材料和容器(以下简称药包材)审批,原料药、药用辅料和药包材在审批药品制剂注册申请时一并审评审批
中国食事药闻 - 关联审评,CFDA,注册申请 - 2017-12-03
2014年3月CDE受理药品简介
2014年3月,CDE共受理药品申请745件,较2月份增长近40%。其中,新药申请212件,仿制申请193件,进口申请68件,均较2月份有不同程度的增加。图2014年3月CDE受理药品申请类型分布 注册分类为1类的新药申报均为新药临床申请,共有16件,涉及7个品种,均为化学药品,其中有6个品种为1.1类,1个品种为1.6类。
中国医药工业信息中心 - CDE,药品 - 2014-05-13
中国CDE不良反应(ADR)因果关系判断法
不良反应 - 2024-02-04
注册收费
注册收费 收费标准 2008年9月1日前付费 2008年9月1日后付费 大会注册费包括参加峰会所有活动和领取论文集、秩序册等会议资料以及午餐、欢迎宴会等,交通
会议 - 2008-08-05
会议注册
会议注册 s 注册费:1500元/人(2009年2月28日前注册人员,享受8折优惠,即1200元/人) s 免费邀请跨国公司前十强、国际知名组织、中国种业公司前五十强和中国农业上市公司的总裁
会议 - 2009-01-13
为您找到相关结果约500个