新型抗肿瘤药物临床应用指导原则 (2018年版)
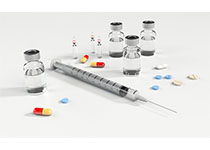
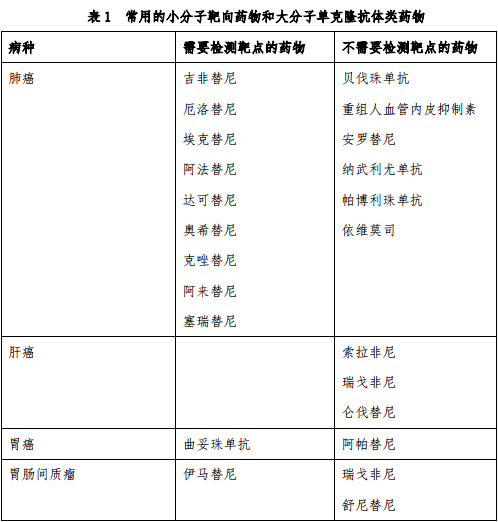
为规范新型抗肿瘤药物临床应用,提高肿瘤合理用药水平,保障医疗质量和医疗安全,维护肿瘤患者健康权益,特制定新型抗肿瘤药物临床应用指导原则。本指导原则涉及的新型抗肿瘤药物是指小分子靶向药物和大分子单克隆抗体类药物。
中华人民共和国国家卫生健康委员会官网 - 新型抗肿瘤药物,临床应用 - 2018-09-28
新型抗肿瘤药物临床应用指导原则(2019年版)
第一部分 新型抗肿瘤药物临床应用指导原则 为规范新型抗肿瘤药物临床应用,提高肿瘤合理用药水平,保障医疗质量和医疗安全,维护肿瘤患者健康权益,特制定新型抗肿瘤药物临床应用指导原则。本指导原则涉及的新型抗肿瘤药物是指小分子靶向药物和大分子单克隆抗体类药物。 抗肿瘤药物临床应用的基本原则 抗肿瘤药物的应用涉及临床多个学科,合理应用抗肿瘤药物是
网络 - 肿瘤 - 2019-12-21
新型抗肿瘤药物临床应用指导原则(2019版)
本指导原则涉及的新型抗肿瘤药物是指小分子靶向药物和大分子单克隆抗体类药物。基本原则为:病理组织学确诊后方可使用,靶点检测后方可使用。目前,根据是否需要做靶点检测,可以将常用的小分子靶向药物和大分子单克
MedSci原创 - 抗肿瘤药物 - 2020-03-16
新型抗肿瘤药物临床应用指导原则(2020年版),覆盖9大癌肿、83种药物
为进一步规范新型抗肿瘤药物临床应用,提高肿瘤合理用药水平,保障医疗质量和医疗安全,维护肿瘤患者健康权益,2020年12月29日,国家卫生健康委发布了《新型抗肿瘤药物临床应用指导原则(2020年版)》。
网络 - 肿瘤 - 2021-01-05
42种新型抗肿瘤药物临床应用指导原则进入“普法期”
近年来,抗癌新药在我国上市的脚步日益加快,且随着17种抗癌药纳入国家医保等惠民新政落地,患者对药物的可及性也越来越高。规范新抗癌药的应用,纳入国家监管部门的视野。
文汇报 - 新型抗肿瘤药物,临床应用 - 2019-04-16
《生物标志物在抗肿瘤药物临床研发中应用的技术指导原则》发布
为合理应用生物标志物指导抗肿瘤药物的临床研发提供可参考的技术规范,在国家药品监督管理局的部署下,药审中心组织制定了《生物标志物在抗肿瘤药物临床研发中应用的技术指导原则》(见附件)。根据《国家药监局综合
MedSci原创 - 生物标志物 - 2021-12-08
指南推荐:生物标志物在抗肿瘤药物临床研发中应用的技术指导原则
生物标志物不仅在临床实践中广泛运用,在抗肿瘤药物研发中的价值也日益凸显,已逐步成为抗肿瘤药物研发过程中极为重要的,甚至是必不可少的一种研发工具。目前已有多个基于生物标志物筛选患者人群的抗肿瘤药物获批上
CDE - 肿瘤,生物标志物,肿瘤药物 - 2021-12-09
当药品说明书遇上临床指南 该如何选择?
我国于 2018 年发布了《新型抗肿瘤药物临床应用指导原则( 2018 年版)》,文中指出:抗肿瘤药物的药品说明书是抗肿瘤药物临床应用的法定依据,其规定的适应证经过了国家药品监督管理部门批准。抗肿瘤药物临床应用须遵循药品说明书,不能随意超适应证使用。但是,随着癌症治疗临床实践的快速发展,目前上市的抗肿瘤药物尚不能完全满足肿瘤患者的用药需求,药品说明书也往往滞后于临床指南和实践,一些具有高级别循证医
肿瘤时间 - 医学人文 - 2019-03-17
42个新型抗肿瘤药物使用原则公布
1、国家卫健委权威发布 7大类肿瘤与42个新型抗肿瘤药物使用原则 近日,国家卫生健康委医政医管局对外发布了《新型抗肿瘤药物临床应用指导原则(2018年版)》(简称“《指导原则》”),对目前越来越多,越来越受关注的抗肿瘤药物使用给予了官方指导。该《指导原则》共涉及7大类肿瘤,42个治疗药物,为小分子靶向药物和大分子单克隆抗体类药物。抗肿瘤药物临床应用需考虑药物可及性和患者治疗价值两大要素。抗肿
医师报 - 基层机构,津贴,抗肿瘤药物 - 2018-09-26
国家卫健委:抗癌药降价保供进医院
国家卫生健康委员会1月10日在国家卫生健康委新闻发布厅召开2019年首场例行新闻发布会,介绍2018年度卫生健康工作进展成效及2019年度卫生健康工作重点任务。一是把临床急需的癌症防治用药纳入国家基本用药目录,以优先配备使用癌症防治药品需求为导向,2018版国家基本药物目录增加了12种抗肿瘤新药和丙肝的治疗药物。二是研究制定一系列癌症治疗的临床路径和用药指南,明确了对新型抗肿瘤药物在病理、特护用药
健康中国 - 卫健委,抗癌药,医院 - 2019-01-11
为您找到相关结果约500个