原研药和仿制药的临床评价
原研药是指原创性的新药,一般都有20年的专利保护期,要经过对成千上万种化合物进行层层筛选、严格的临床前和临床试验,才得以获准上市。一般情况下,原研药需要花费1 2 ~ 1 5 年左右的研发时间和1 0 ~ 2 0 亿美元的研发经费,目前只有大型跨国制药企业才有能力研制。仿制药是指与原研药具有相同的活性成分、剂量组成、给药途径,可以在形状、释放机制、赋形剂(非活性成分)、有效期和包装等方面有所不同,
中华医学信息导报 - 原研药,仿制药 - 2016-07-28
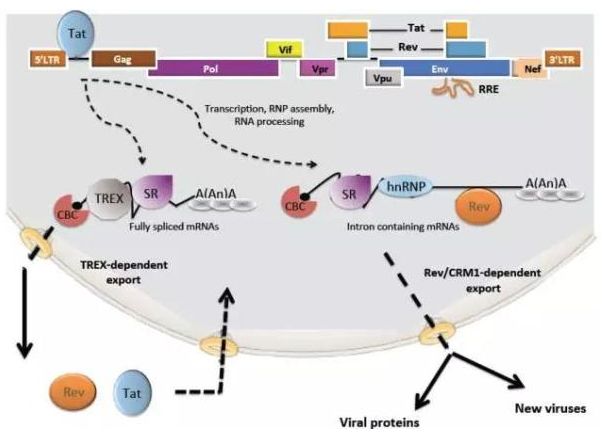
首个减少HIV 病毒载量在研新药初期临床成功
今天,创新生物技术公司 ABIVAX 宣布,接受了该公司先导新药候选物 ABX464 的慢性人类免疫缺陷病毒(HIV,俗称艾滋病病毒)感染者首次显示了体内病毒载量的减少,这是通过在外周血液单核细胞(PBMC)中的总 HIV 病毒 DNA 来测量的。ABX464 的分子结构(图片来源:ABIVAX 官网)ABX464 是一种通过全新作用机制来抑制 HIV 病毒复制的领域内首个(first-i
药明康德 - HIV - 2017-05-03
2014年度中国心脏外科白皮书:阜外领跑,广东心研所升至前三
传统格局被打破 2014年,心脏手术例数排名前十的单位是:心脏手术数排名前十的医院是:阜外医院(13025),安贞医院(10623),广东心研所(4896),武汉亚心(4429),西京医院(3950
中国循环杂志 - 中国心脏外科白皮书,阜外医院 - 2015-11-03
临床前研究验证性研究发表难题
临床前研究结果可重复性差,但是对这些研究进行重复似乎缺乏动力,只有一些比较重大的突破性研究,如那些发表在重要学术期刊上的,有潜在应用价值的研究,会受到医药公司的重视和重复。但是医学临床前研究的结果重复发表难问题已经
科学网博客园 - 临床研究 - 2016-02-05
抗肿瘤药物的非原研伴随诊断试剂临床试验注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《抗肿瘤药物的非原研伴随诊断试剂临床试验注册审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 抗肿瘤药物 - 2024-04-19
Neurology:临床前和前驱认知障碍阶段的临床相关变化
MCIDs可应用于临床实践或临床试验,以确定是否发生了临床相关的变化
MedSci原创 - 老年痴呆症,轻度认知障碍 - 2022-09-14
与抗肿瘤药物同步研发的原研伴随诊断试剂临床试验注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《与抗肿瘤药物同步研发的原研伴随诊断试剂临床试验注册审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 抗肿瘤药物 - 2024-03-29
Moderna正在临床前阶段研究mRNA猴痘疫苗
周一,又有五个国家报告了首例猴痘确诊病例,使今年报告猴痘疫情的国家总数达到17个。截至上周六,世界卫生组织(WHO)报告了12个国家5月13日至21日至少92例实验室确诊病例。另有28例疑似病例正在接
网络 - 猴痘疫苗 - 2022-05-25
2016 循证临床实践指南:前交叉韧带康复
2016年8月,荷兰皇家物理治疗学会(KNGF)指示前交叉韧带多学科专家组制订发布了前交叉韧带重建后康复共识,主要内容涉及前交叉韧带术前康复,术后康复,返回治疗标准。
Br J Sports Med. 2016 Aug 18. - 前交叉韧带,康复 - 2016-08-24
南开大学研创抗脑胶质瘤新药 已在澳洲临床试验
中国新闻网 - 南开大学,胶质瘤 - 2016-10-14
原研药与仿制药:创新与竞争的循环 – 生物谷专访Teva公司董事会顾问及前主席兼总裁
梯瓦制药公司(Teva Pharmaceutical Industries Ltd.) (简称Teva)是以色列最大的上市公司,全球最大的仿制药生产公司,市值大约为200亿美元,2007的总销售额超过70亿美元,它在全球的直属运营部门将遍及50多个国家,员工数量超过2.5万人。 2008年7月3日,生物谷(Bioon.com)在第七届日本国际生物论坛和博览会(7th Bio Forum &
会议 - 2008-07-17
2018 ASHM临床指南:HIV暴露前预防(更新版)
2018年4月,澳大利亚艾滋病医学会(ASHM)更新发布了HIV暴露前预防指南,HIV感染高危人群日常联合应用替诺福韦和恩曲他滨进行暴露前预防在美国,欧洲以及澳大利亚和WHO指南中均有推荐。本文是对2017版指南的更新,针对每日用药和按需用药进行HIV暴露前预防的建议进行修订。
J Virus Erad. 2018 Apr 1;4(2):143-159. - HIV暴露前预防 - 2018-04-30
为您找到相关结果约500个