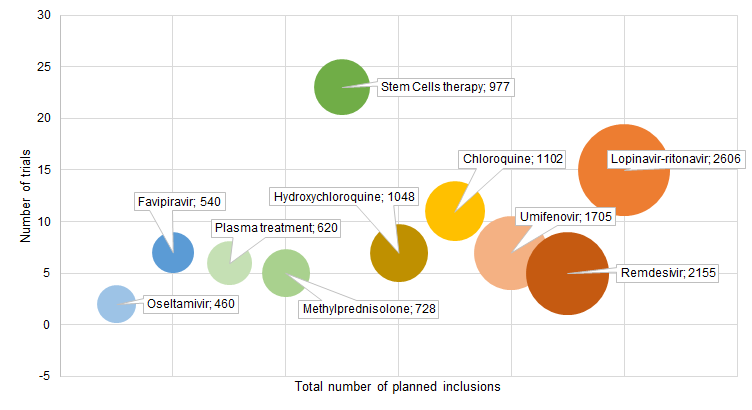
medRxiv: COVID-19注册临床试验概况如何?
在疾病流行的背景下,临床医生和研究人员获得世界各地不同团队正在建立的快速和高质量的临床试验信息是至关重要的,这些结果将告知使用的抗病毒药物、其剂量和持续时间、患者的纳入和排除标准、将要评估的结果以及临
生物探索 - Covid-19 - 2020-03-25
BMJ:临床试验注册对药物治疗系统评价的影响?
由此可见,试验注册是确定额外的随机对照试验的重要来源。如果进行检索,所有系统评价纳入的随机对照试验和患者数量对有所不同。
MedSci原创 - 临床试验注册,药物治疗,系统评价 - 2017-02-18
医疗器械临床试验数据递交要求注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《医疗器械临床试验数据递交要求注册审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 医疗器械 - 2024-04-19
注册类抗肿瘤药物临床试验延伸给药共识(2019版)
肿瘤新发患者逐年升高,注册类抗肿瘤药物临床试验日趋增多,监管部门审批流程的优化缩短了抗肿瘤药物上市时间,药物临床试验完成后或注册类药物上市后延伸给药是申办方、临床试验机构和伦理委员会共同面临的问题。为
中国新药杂志.2020,29 (9):1203-1206. - 抗肿瘤药物 - 2020-07-31
体外诊断试剂临床试验数据递交要求注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《体外诊断试剂临床试验数据递交要求注册审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 体外诊断试剂 - 2024-04-19
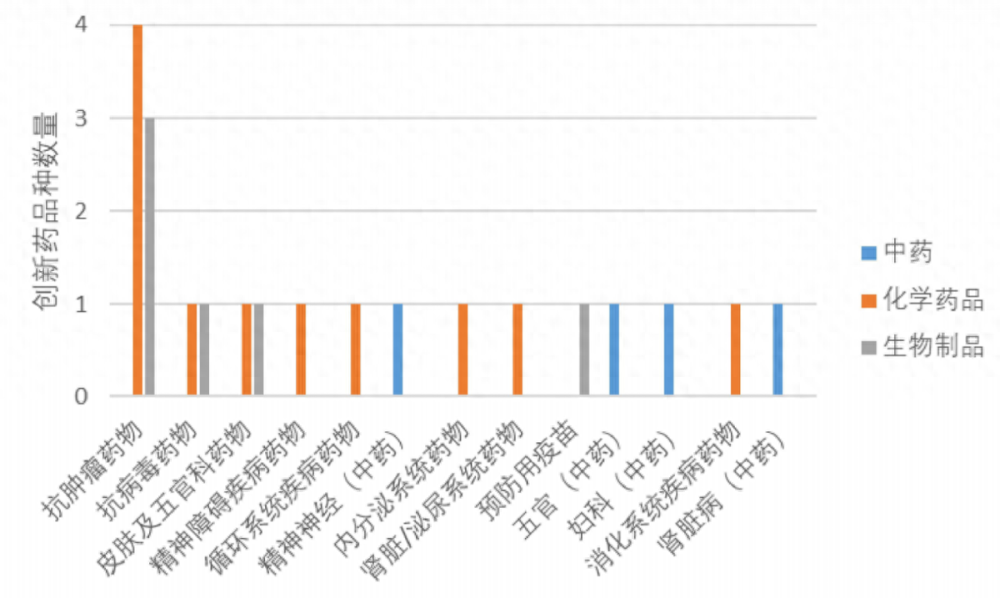
CDE发布中国新药注册临床试验进展年度报告(2022年)
9月7日,CDE官方公告显示,国家药监局药审中心发布《中国新药注册临床试验进展年度报告(2022年)》。
药研网 - 临床试验,CDE - 2023-09-10
使用体外诊断试剂境外临床试验数据的注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《使用体外诊断试剂境外临床试验数据的注册审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 体外诊断试剂 - 2024-04-20
自主研发 | 我国生物型接骨空心螺钉大规模注册临床试验正式启动
这款“生物型接骨空心螺钉”是我国完全自主研发的来源于传统蚕丝的高性能、低成本生物科技材料,突破了硬质蚕丝蛋白材料的技术壁垒。
网络 - 2023-12-25
抗肿瘤药物的非原研伴随诊断试剂临床试验注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《抗肿瘤药物的非原研伴随诊断试剂临床试验注册审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 抗肿瘤药物 - 2024-04-19
Iterum Therapeutics宣布完成口服Sulopenem治疗尿道感染的III期临床试验注册
Iterum Therapeutics是一家临床阶段的制药公司,致力于开发新型抗生素,以治疗社区和医院环境中由多重耐药性病原体引起的感染,Iterum Therapeutics近日宣布口服Sulopenem治疗尿道感染的III期临床试验已完成患者入组。
MedSci原创 - Sulopenem,尿道感染,Iterum,therapeutics - 2019-12-30
ClinicalTrials.gov网站临床试验注册指导
临床试验注册一直是医学文献、通俗媒体以及美国议会所关注的焦点问题。临床试验的注册库都属于网络数据库,收录临床试验的资料,兼有伦理和学术双重作用。这些注册库确保公众对目前正在开展或既往已开展项目的了解,从而发挥伦理作用;同时还可为研究人员、期刊编辑人员和审稿专家提供一些解读研究结果所需的背景资料;通过完整罗列各项临床试验的目录清单,还可提示研究人员对当前尚未
MedSci原创 - ClinicalTrials,临床研究,试验 - 2013-07-02
美国临床试验数据库(ClinicalTrials)注册流程与填写要求
临床试验注册制度,指在临床试验实施前就在公共数据库公开试验设计信息,并跟踪和报告试验结果。临床试验注册制度不仅有利于增加临床试验信息的 透明度、减少发表偏倚,更有利于保障临床试验质量、增加试验过程的规范性和试验结果的可信度,已成为当今临床试验发展的主流趋势[1-2]。 我国中医药领域对临床试验注册的重视程度和实践情况不容乐观,以美国临床试验数据库(ClinicalTrials.gov)
中国中医药信息杂志 - 临床试验,注册 - 2014-03-03
AHJ:注册研究和临床试验研究对比应校正基础风险指数
美国学者Steinberg等选择25个国家的3 726例ST段抬高型急性心肌梗死患者进行注册研究,并收集了人口统计学、住院治疗方案、住院发生的临床事件资料。这些医院同时参加了用依诺肝素和溶栓再灌注治疗急性心肌梗死(ExTRACT-TIMI)的随机化临床试验。结果显示,注册研究组的患者基础风险更大,未校正的住院死亡率在注册研究组比临床试验组更高。在校正了基础风险指数后,两者的死亡率接近,且注册研究组
MedSci原创 - 2013-11-18
BMJ: 期刊文章和临床试验注册中心报告漏报主要危害数据
为了测定临床试验方案、临床研究报告和主要的公开资源(期刊文章和试验注册)之间的数据在疗效和重大危害方面是否有矛盾的地方,以及临床研究报告本身是否矛盾,采用度洛西汀治疗重度抑郁症的研究作为研究对象。9个随机的度洛西汀安慰剂对照试验(共2878个病人)用于重度抑郁症提交给欧盟药品管理局(EMA)审批。研究者于2011年5月从EMA获得包含
MedSci原创 - 度洛西汀,数据来源 - 2014-11-03
FDA:增强临床试验人群的多样性 - 纳排标准、注册实践和行业试验设计指南
在过去的几十年里,FDA 主要通过扩大资格标准促进了注册实践,这将导致临床试验更好地反映最有可能使用该药物的人群,如果该药物获得批准。 尽管做出了这些努力,参与临床试验的挑战仍然存在,并且某些群体在许
FDA - 临床试验 - 2021-10-22
为您找到相关结果约500个