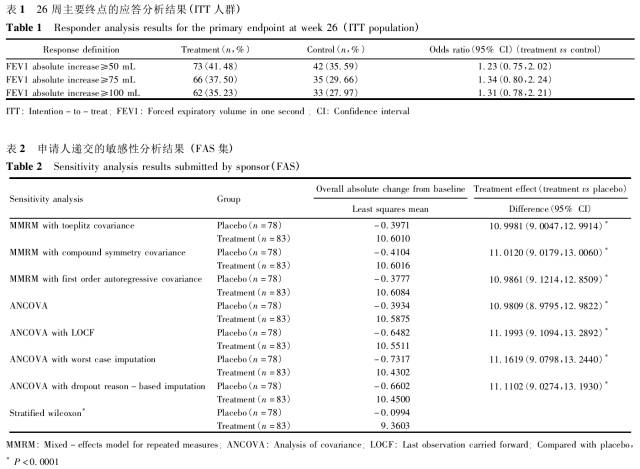
药审中心:临床试验缺失数据的统计学考量
缺失数据是临床试验中常见的重要问题,可能引起试验结果难于解释,甚至影响整个试验的推断和结论,但目前在国内临床研究中尚未引起足够的重视。实际应用中,申请人对待缺失数据的处理存在盲口应用统计学方法的现象,给新药安全有效性的评价和确证带来诸多困难。本文针对三个实际案例进行深入地阐述和分析,探讨对缺失数据的预防、估训一量的选择、缺失数据的统训一分析方法以及敏感性分析等,以期有助于申请人在临床试验中加强
中国临床药理学杂志 - 临床试验,缺失数据 - 2016-06-18
单组目标值(OPC)临床试验的统计学考虑
作者:中国临床试验生物统计学组(CCTS) 李卫,赵耐青(执笔) 来源:中国卫生统计 2017年6月 第34卷第3期 随机对照临床试验(randomized controlled trial,RCT)是临床研究的金标准,药物/医疗器械临床研究中,尤其是提供关键证据的临床研究中一般均采用RCT。在极少数的医疗器械临床试验中,如采用随机对照试验,会存在伦理学风险,致使临
中国卫生统计 - 单组目标值 - 2019-01-29
关于公开征求《疫苗临床试验的统计学指导原则(征求意见稿)》意见的通知
鉴于疫苗临床试验的特点,在药物研发过程中,需要选择合适的设计和分析方法以确保研究质量和结果的可靠性。我中心组织起草了《疫苗临床试验的统计学指导原则(征求意见稿)》,现公开征求意见。
国家药品监督管理局药品审评中心 - 疫苗临床试验 - 2023-11-07
ICH E9临床试验的统计学指导原则解析
ICH E9 Statistical principles for clinical trials (临床试验的统计学指导原则)可谓生物统计师的bible,目的在于协调欧洲、日本和美国在进行药品上市申请的临床试验时所应用的统计学方法的指导原则虽说中国是协调三方之外的国家,SFDA还为此另外制定了自己的《化学药物和生物制品临床试验的生物统计学技术指导原则》,但其内容基本还是照抄翻译了ICH E9的
MedSci原创 - ICH,E9,临床试验,统计 - 2012-05-28
我国临床试验生物统计学指导原则与国际ICH E9比较研究
《ICH Harmonised Tripartite Guideline Statistical Principles ClinicalTrails E9》(以下简称“ICH E9”)是在人用药品注册技术要求国际协调会议的赞助下制定,目的从统计学原理和方法出发,向申办者和专家提供建议,以便有助于为申请新药入市而作的临床 试验的分析和结论得到公认。现主要用于欧盟日本及美国管理当局的
中国卫生统计 - 生物统计,ICH,E9 - 2014-08-09
抗肿瘤药物临床试验统计学设计指导原则(试行)(2020年)
为建立抗肿瘤药物临床试验设计中统计学技术要求的统一尺度,鼓励和指导工业界进一步优化抗肿瘤药物临床试验中的统计学设计,以提高临床研发效率,药审中心组织制定了《抗肿瘤药物临床试验统计学设计指导原则(试行)
NMPA - 肿瘤 - 2021-02-09
抗肿瘤药物临床试验统计学设计指导原则(征求意见稿)
为了促进药物临床试验各相关方对抗肿瘤药物临床试验统计学设计的理解与合理应用,经广泛调研和讨论,我中心组织起草了《抗肿瘤药物临床试验统计学设计指导原则(征求意见稿)》。
CDE - 临床试验 - 2020-08-04
CCTS共识:临床试验中样本量确定的统计学考虑 2015
样本量 确定 (samplesizedetermination),又称样 本量估计 (samplesizeestimation),是指为满足统计 的 准确性和可靠性(I类错误 的控制和检验效能的保证) 计算 出所需的样本量 ,它是 临床试验设计 中一个极为 重要 的环节 ,直接关系到研究结论 的可靠性 、可重复 性 ,以及研究效率的高低。效果和检验效能 的权
CCTS,样本量 - 2016-06-17
多中心临床试验中中心校正的统计学实现(SPSS)
多中心临床试验可以在较短的时间内招募到足够多的病例数,同时,来自多中心的病例比来自单中心的病例更具有代表性,可以使所得结论的应用面更广泛。但由于各中心的试验条件不完全相同,所得结论也不尽相同。因此, 在评价疗效时, 必须考虑中心间效应的差别。当中心间差距较大时,如果直接合并各中心资料,可能会对总的结论有一定影响。这里涉及到两个问题,其一是评价中心效应是否存在,其二是如何扣除中心效应的影响对疗效进行
MedSci原创 - 中心校正,SPSS - 2013-11-19
CCTS 专家共识:非劣效临床试验的统计学考虑 2012
鉴于非劣效临床试验在 国内开展地 比较广泛,但 在研究设计和评价方面尚未形成相对统一 的认识 ,为 此中国临床试 验生 物统计学工作 小组 (CCTS),经充 分讨论 ,于 2011年 10月 30
统计,非劣效 - 2012-04-01
CCTS 专家共识:临床试验中多重性问题的统计学考虑 2012
临床试验根据研究目的不同可分为“探索性临床 试验”和“确证性临床试验”,而临床研究结论通常需 要根据确证性临床试验的统计推断结果得到。如果某 一确证性临床试验需要对多个检验假设做出统计学推 断,例如多个主要疗效指标的多重检验、多组间多重比 较、多个时间点的期中分析( interim analysis) 等情况 下,便会涉及多重性
CCTS,专家,统计 - 2012-06-17
适应性临床试验设计特点与介绍
众所周知,新药的研发是一个充满变数且不断做出复杂决断的过程,这就要求试验设计应该具备可变动性,以便于在试验过程中对其进行调整。在这种情况下,适应性设计(adaptive design)的提法也应运而生[1]。尽管适应性设计诞生之后受到了很多国家企业界和管理当局的关注,并且近年来也一直是统计学界、临床试验工作者和管理当局一直争议和探讨的热点问题,但到目前为止,适应性设计一直未能广泛应用。其主要原
MedSci原创 - 适应性临床试验,设计 - 2013-05-26
适应性临床试验设计相关问题的探讨
众所周知,新药的研发是一个充满变数且不断做出复杂决断的过程,这就要求试验设计应该具备可变动性,以便于在试验过程中对其进行调整。在这种情况下,适应性设计(adaptive design)的提法也应运而生[1]。 尽管适应性设计诞生之
MedSci原创 - 适应性设计,临床试验 - 2013-05-30
为您找到相关结果约500个