药审中心拟优先审评名单更新
4月17日,药审中心公示的拟优先审评的药品品种新增以岭万洲国际制药有限公司的非洛地平缓释片(规格为2.5mg、5mg、10mg),公示期间如有异议,可在药审中心网站“信息公开-->优先审评公示-->拟优先审评品种公示
中国药审 - 优先评审,药品注册 - 2019-04-22
抗疟疾新药获FDA优先审评资格
近日,60 Degrees Pharmaceuticals(60P)宣布,美国FDA授予其预防成人疟疾药物Tafenoquine (TQ)优先审评资格。2018年1月,该药物获得FDA的快速通道资格。
药明康德 - Tafenoquine,FDA,优先审评 - 2018-02-12
8款药品注册申请拟纳入优先审评
2019年3月29日,药审中心公示的拟优先审评的药品品种新增“盐酸安非他酮缓释片”等,公示期间如有异议,可在药审中心网站“信息公开-->优先审评公示-->拟优先审评品种公示”栏目下提出异议。
中国药审 - 药品,优先审评 - 2019-04-01
优先审评审批助力丙肝新药加快上市
随着我国药品审评审批制度改革的持续推进,广大丙肝患者的热切期盼成为现实——9月21日,国家食品药品监督管理总局同时批准吉利德公司(Gilead)的口服丙肝新药索磷布韦片,艾伯维公司(AbbVie)的奥比帕利片
中国医药报 - 优先评审,丙肝新药,上市 - 2017-09-25
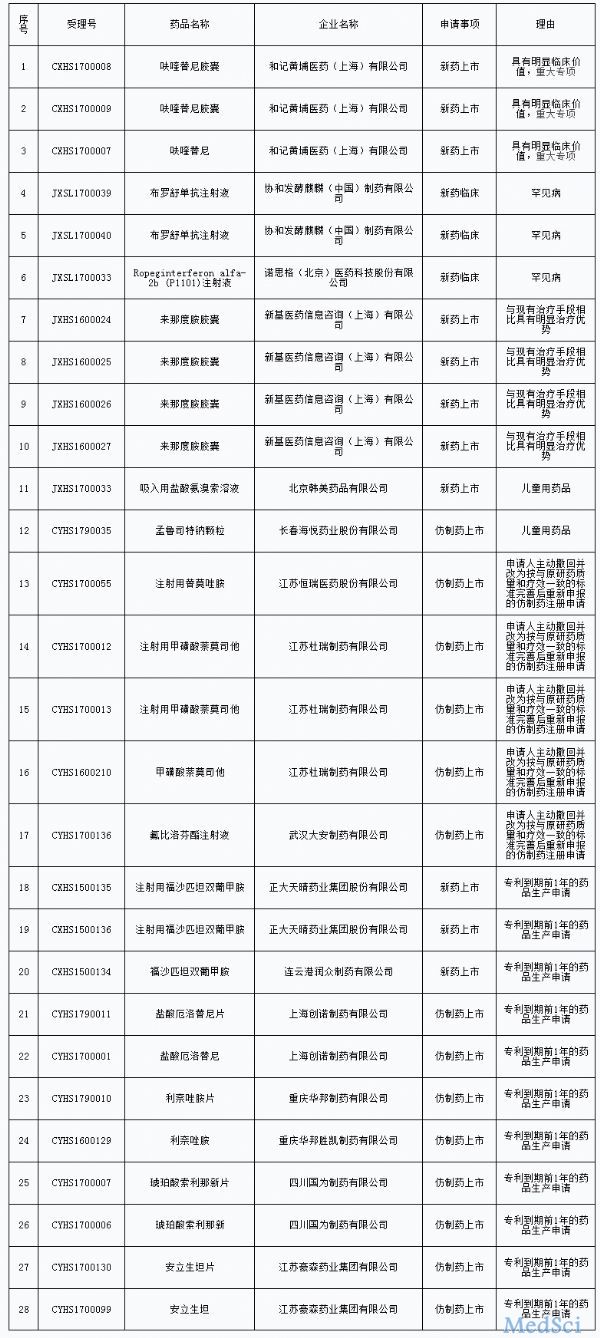
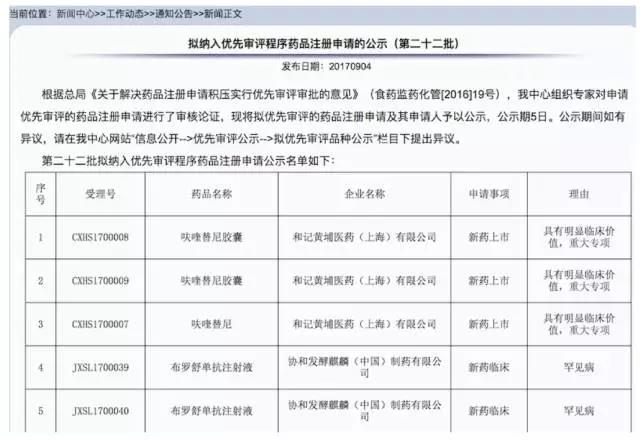
最新优先审评名单出炉,再添28个药品
今日(9月4日),国家食品药品监督管理总局药品审评中心(简称“CDE”)发布《拟纳入优先审评程序药品注册申请的公示(第二十二批)》,将拟优先审评的药品注册申请及其申请人予以公示,根据公示名单,此次入选的
医谷 - 药品,评审,药品注册申请 - 2017-09-04
9价HPV疫苗获优先审评 有望扩大适用年龄
FDA已经授予该sBLA优先审评资格,有望在2018年10月6日之前给出答复。在美国,大多数性活跃的男
药明康德 - 9价HPV疫苗 - 2018-06-20
新增15个品种拟被CDE纳入优先审评程序
8月19日至22日,CDE网站拟优先审评公示栏新增15个品种。拟同意纳入优先审评的理由分别是:注射用复方维生素(13)为仿制药上市;小儿钠钾镁钙葡萄糖注射液、小儿等渗电解质注射液为儿童药;曲美替尼片、达拉非尼胶囊、HSK3486乳状注射液、西妥昔单抗注射液、帕博利珠单抗注射液为具有明显治疗优势药品;阿卡波糖片则为符合117公告品种、申请人主动撤回的优先条件。
新浪医药新闻 - 优先审评,治疗优势 - 2019-08-25
卫计委:18个重大新药创制优先药品审评名单
为加快重大新药创制科技重大专项(以下简称“新药专项”)创新成果产出进程,根据有关文件规定和专家评审遴选建议,拟推荐法米替尼等18个专项支持的药物品种为优先审评品种。 现将拟推荐的品种予以公示。
国家卫生和计划生育委员会 - 新药,药品审评 - 2015-01-15
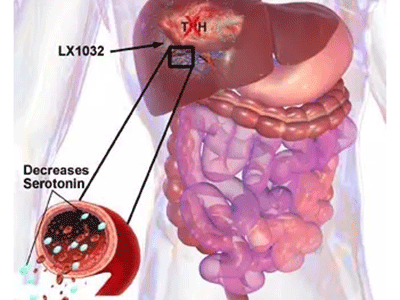
FDA将优先审评类癌综合症新药carcinoid syndrome
致力于研发精准新药用于治疗严重慢性疾病的生物制药公司Lexicon Pharmaceuticals宣布,美国FDA已接受了telotristat etiprate新药申请的优先审评。
MedSci原创 - 类癌综合症,FDA - 2016-06-04
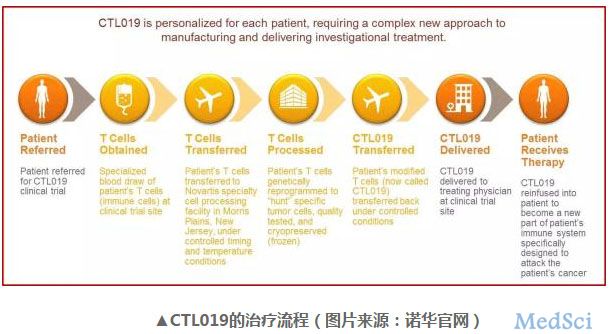
诺华CAR- T疗法今日获美国FDA优先审评资格
3月29日,诺华宣布美国 FDA 已为其 CAR- T 疗法 CTL019(tisagenlecleucel-T)的生物制剂许可申请颁发了优先审评资格。
药明康德 - 诺华,CAR-T疗法,癌症 - 2017-03-30
【喜讯】肠癌新药呋喹替尼进入CDE优先审评程序
9月4日,国家食品药品监督管理局药品评审中心(CDE)在官网上发布公告,包括我国原创小分子靶向药物呋喹替尼在内的多个药品进入优先审批程序。
肿瘤资讯 - 呋喹替尼,靶向药物,药品注册 - 2017-09-07
类癌综合症新药carcinoid syndrome获FDA优先审评资格
本周,致力于研发精准新药用于治疗严重慢性疾病的生物制药公司Lexicon Pharmaceuticals宣布,美国FDA已接受了telotristat etiprate新药申请的优先审评。
药明康德微信号:WuXiAppTecCh - 类癌综合症,类癌瘤,FDA - 2016-06-05
诺华ceritinib获FDA优先审评,有望一线用于肺癌治疗
今日,诺华(Novartis)宣布,美国FDA接受了该公司的补充新药申请(sNDA),并批准优先审评扩大使用Zykadia(ceritinib)一线治疗转移性非小细胞肺癌(NSCLC)患者,这些病人的肿瘤通过
MedSci原创 - ceritinib,Zykadia,诺华,优先审评 - 2017-02-24
FDA:儿科罕见病优先审评券计划(草案)
本指南提供了有关食品和药物管理局安全与创新法案 (FDASIA) 第 908 节的实施信息,该法案将第 529 节添加到《联邦食品、药品和化妆品法案》(FD&C 法案)中。 根据第 529 条
FDA - 罕见病 - 2021-10-25
为您找到相关结果约500个