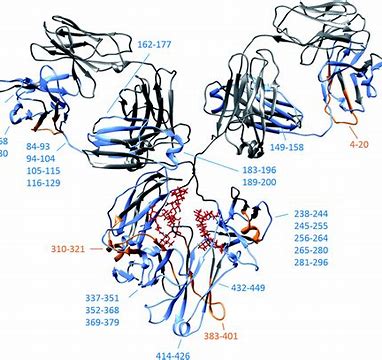
礼来公司的LY-CoV555无法帮助住院COVID-19的患者
礼来公司的单克隆抗体LY-CoV555对COVID-19住院患者没有显著的临床价值。
MedSci原创 - 礼来,Covid-19,COVID-19肺炎,LY-CoV555 - 2020-10-27
NEJM:中和抗体LY-CoV555治疗门诊轻中度新冠肺炎患者效果不显著
仅2800mg剂量下,中和抗体LY-CoV555可显著减少新冠肺炎门诊患者的病毒水平,其他2个剂量的效果不显著
MedSci原创 - 中和抗体,新冠肺炎,LY-CoV555 - 2020-10-29
NEJM:LY-CoV555联合瑞德西韦不能缩短新冠肺炎住院患者恢复期
LY-CoV555与瑞德西韦联合治疗不能加快新冠肺炎住院患者恢复时间
MedSci原创 - 新冠肺炎,瑞德西韦,LY-CoV555 - 2020-12-26
全球首款新冠病毒中和抗体LY-CoV555进入I期临床试验,首批患者给药完成
该试验的启动,比原定计划提前进行,标志着SARS-CoV-2反应的新阶段的开始,研究对象将接受专为该病毒设计的药物
MedSci - 中和抗体,新冠病毒 - 2020-06-04
礼来公司在新墨西哥州开始对COVID-19中和抗体bamlanivimab(LY-CoV555)进行研究
礼来公司今天宣布,通过与新墨西哥州的当地机构合作,已开始对COVID-19中和抗体bamlanivimab(LY-CoV555)进行研究。
MedSci原创 - 中和抗体,Covid-19,bamlanivimab(LY-CoV555) - 2020-12-19
礼来公布新冠病毒中和抗体II期概念验证数据:降低门诊COVID-19患者72%住院风险
9月16日,礼来宣布了BLAZE-1研究的中期分析结果,显示使用中和抗体LY-CoV555单药治疗COVID-19门诊患者可降低住院率。
医药魔方 - 新冠病毒 - 2020-09-17
礼来公布中和抗体联合疗法最新数据!向FDA提交紧急使用授权申请
10月7日,礼来宣布了其抗SARS-CoV-2病毒中和抗体开发项目的最新进展,包括两款中和抗体 LY-CoV555与LY-CoV016(从君实引进的JS016)的联合疗法用于新确诊轻至中度COVID-
医药魔方 - FDA,中和抗体,紧急使用 - 2020-10-08
芝加哥大学医学院:开始测试抗SARS-CoV-2抗体的疗效
美国芝加哥大学医学院(UChicago Medicine)正在开展一项临床试验(BLAZE-1试验),以检查抗SARS-CoV-2刺突蛋白的抗体治疗COVID-19(由新型冠状病毒引起的疾病)的潜力。
MedSci原创 - SARS-COV-2,SARS-CoV-2抗体,LY-CoV555,芝加哥大学 - 2020-09-04
礼来启动新冠病毒COVID-19抗体药物的全球首个临床试验
COVID-19抗体将在不适合使用疫苗的人群中进行评价。
MedSci原创 - 中和抗体,新冠病毒COVID-19 - 2020-06-07
近期多起新冠疗法试验暂停表明临床试验安全系统正常运行,公众不必担忧
礼来公司针对新冠病毒的ACTIV-3单克隆抗体治疗的三期试验由于潜在的安全隐患而被暂停。
MedSci原创 - 中和抗体,礼来,吉利德,瑞德西韦,瑞德西韦(Remdesivir) - 2020-10-15
美国国立卫生研究院(NIH)正在进行COVID-19预防性单克隆抗体的临床试验
目前,两项在健康成年人中进行的安慰剂对照双盲临床试验正在评估实验性单克隆抗体(mAb)是否可以预防SARS-CoV-2冠状病毒感染。
MedSci原创 - Covid-19,REGN-COV-2,LY-CoV555 - 2020-08-11
君实生物重组全人源抗SARS-CoV-2单克隆抗体注射液进展良好
君实生物公布其重组全人源抗SARS-CoV-2单克隆抗体注射液联合疗法的进展,在降低病毒载量、减轻症状及降低和冠状病毒相关的住院及急诊治疗方面均显示出良好疗效。
亿欧 - 单克隆抗体,注射液, 君实生物 - 2020-10-08
礼来宣布,美国政府将购买更多剂量的中和抗体疗法来治疗COVID-19
礼来公司近日宣布,美国政府已同意一起购买至少100,000剂700毫克的Bamlanivimab(LY-CoV555)和1400毫克的etesevimab(LY-CoV016)。
MedSci原创 - Covid-19,bamlanivimab(LY-CoV555),Bamlanivimab,etesevimab - 2021-02-27
FDA扩大君实/礼来新冠中和抗体紧急授权
9月16日,礼来宣布,美国FDA已经扩大其与君实合作的新冠中和抗体bamlanivimab(700mg)和etesevimab(1400mg)紧急使用授权 (EUA),用于个体暴露后预防 (PEP)。
医药魔方 - FDA,礼来,免疫应答,鸡尾酒疗法,新冠中和抗体 - 2021-09-18
礼来的中和抗体bamlanivimab获得FDA紧急使用授权,用于治疗轻中度新冠COVID-19感染患者
Bamlanivimab是靶向新冠病毒SARS-CoV-2的spike蛋白的中和抗体。
MedSci原创 - 中和抗体,COVID-19新冠病毒,bamlanivimab(LY-CoV555),FDA的紧急使用授权(EUA) - 2020-11-10
为您找到相关结果约152个