国家药品审评中心发布药物非临床安全性研究技术指导原则
作为药审中心承担的十二五重大专项课题之法规科学的部分内容,2013年3月28日至29日,中心组织召开了药物非临床安全性研究技术指导原则合并修订/ 起草专题讨论会。
MedSci原创 - 药品审评中心,CDE - 2013-07-06
国家药监局药品、器械审评检查长三角分中心在上海正式挂牌
国家药品监督管理局药品审评检查长三角分中心、医疗器械技术审评检查长三角分中心正式挂牌。
医谷网 - 上海,器械审评,正式挂牌 - 2021-01-07
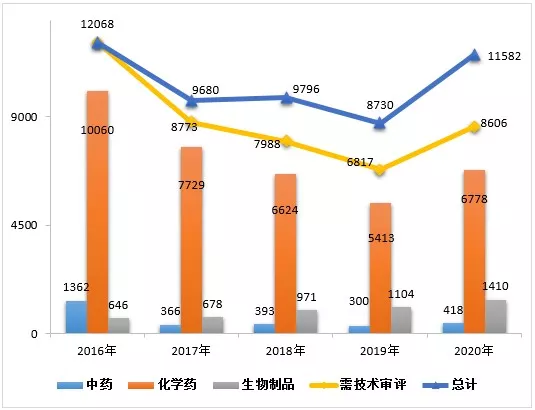
2020年度药品审评报告
2020年是极不平凡的一年,面对突如其来的新冠肺炎疫情,中国国家药品监督管理局药品审评中心(以下简称药审中心)在中国国家药品监督管理局(以下简称国家药监局)的坚强领导下,贯彻《药品管理法》《疫苗管理法
CDE - 药品审评报告 - 2021-06-23
药审中心拟优先审评名单更新
4月17日,药审中心公示的拟优先审评的药品品种新增以岭万洲国际制药有限公司的非洛地平缓释片(规格为2.5mg、5mg、10mg),公示期间如有异议,可在药审中心网站“信息公开-->优先审评公示-->拟优先审评品种公示
中国药审 - 优先评审,药品注册 - 2019-04-22
国家药品监督管理局药品审评过程中审评计时中止与恢复管理规范(试行)
为加强药品监督管理,国家药品监督管理局发布了《国家药品监督管理局药品审评过程中审评计时中止与恢复管理规范(试行)》,本文为其具体文件内容。
国家药品监督管理局官网 - 药品审评 - 2023-08-17
药品审评中心药物临床试验期间安全信息评估与风险管理工作程序(试行)
本文为国家药品监督管理局药品评审中心发布的《药品审评中心药物临床试验期间安全信息评估与风险管理工作程序(试行)》。
国家药品监督管理局药品评审中心 - 临床试验 - 2023-11-10
药品注册申请审评期间变更工作程序(试行)
为配合《药品注册管理办法》的贯彻实施,药审中心组织制定了《药品注册申请审评期间变更工作程序(试行)》。
国家药品监督管理局药品审评中心 - 药品注册 - 2023-07-18
8款药品注册申请拟纳入优先审评
2019年3月29日,药审中心公示的拟优先审评的药品品种新增“盐酸安非他酮缓释片”等,公示期间如有异议,可在药审中心网站“信息公开-->优先审评公示-->拟优先审评品种公示”栏目下提出异议。
中国药审 - 药品,优先审评 - 2019-04-01
《药品审评中心药物临床试验期间安全信息评估与风险管理工作程序(试行)》修订说明
我们对《药品审评中心药物临床试验期间安全信息评估与风险管理工作程序(试行)》工作程序进行了修订,现面向社会征求意见。
国家药品监督管理局药品审评中心 - 临床试验 - 2023-07-10
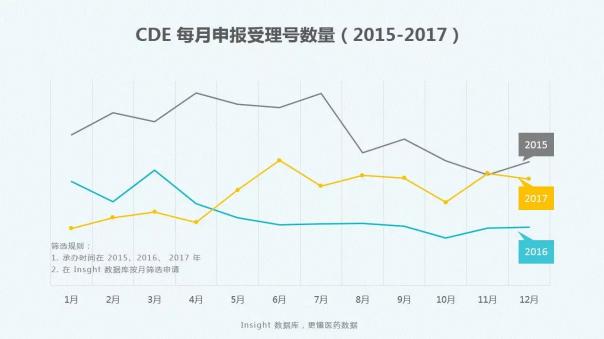
2017全年CDE药品审评报告
Insight数据库2017年终报告梳理了2017年CDE药品申报和审评的数据情况,让大数据来为你指路。
Insight数据库 - 药品审评,CDE,2017 - 2018-01-12
药品审评中心补充资料工作程序(试行)
为配合《药品注册管理办法》的贯彻实施,进一步规范药品注册审评补充资料管理工作,结合药品审评以流程为导向的科学管理体系的研究成果和审评工作实际,药审中心研究制定了《药品审评中心补充资料工作程序(试行)》
CDE - 药品审评中心 - 2020-12-07
国家药品监督管理局药品审评过程中审评计时中止与恢复管理规范(试行)(征求意见稿)
为落实《药品注册管理办法》(国家市场监督管理总局令第27号)相关要求,我中心组织起草了《国家药品监督管理局药品审评过程中审评计时中止与恢复管理规范(试行)》,现在中心网站予以公示,以广泛听
CDE - 药品审评 - 2021-11-19
为您找到相关结果约500个