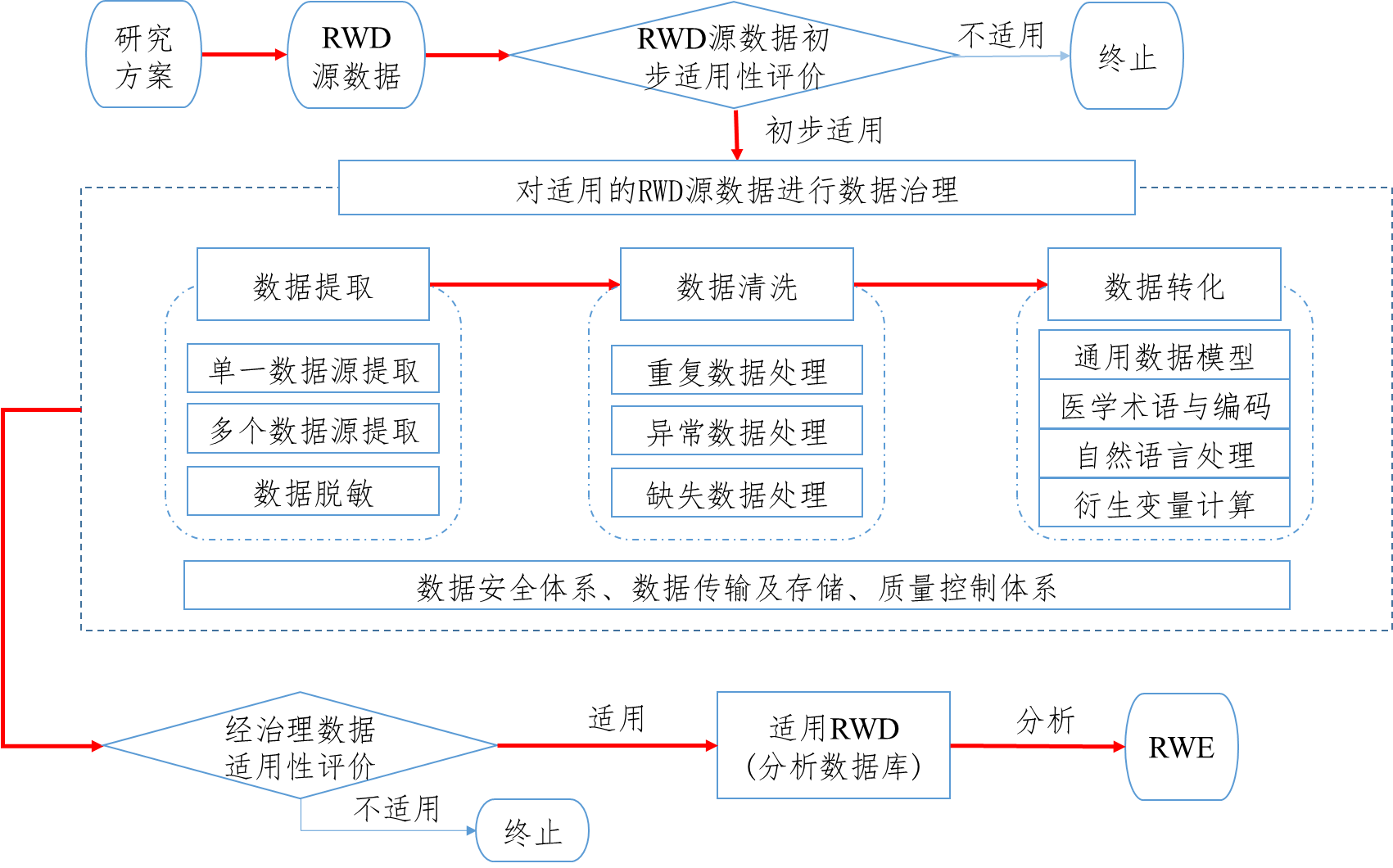
用于产生真实世界证据的真实世界数据指导原则(征求意见稿)
为进一步指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发,我中心组织起草了《用于产生真实世界证据的真实世界数据指导原则(征求意见稿)》,现在中心网站予以公示,以广泛听取各界意见和建议,欢迎
CDE - 真实世界证据,真实世界研究 - 2020-08-03
利用真实世界数据做好研究:关键的数据质量问题
本文我们来聊一聊真实世界数据质量的相关问题。原始数据的质量在使用RWD的研究中,原始数据的质量取决于数据完整性和准确性。一个关键问题在于数据随机缺失(missing at random)的程度:随机缺失数据会减低测量的准确性,而非随机缺失会导致结果偏倚。因此,研究者需要仔细判断数据的真实性(即该数据是否可以反映真实的情况)和可靠性(即收集的数据是否具有一致性)。除了数据质量,还需要考虑数据的全
医咖会 - 真实世界数据 - 2019-03-12
FDA 指导文件:使用真实世界数据和真实世界证据向 FDA 提交药品和生物制品文件
为了便于 FDA 对提交给 FDA 的包括真实世界数据 (RWD) 和真实世界证据 (RWE) 的提交进行内部跟踪,本指南鼓励申办者和申请人在提交的求职信中指明 RWD/RWE 的某些用途。本指南不涉
FDA - 真实世界证据,真实世界数据 - 2022-09-10
2017 DIA | 真实世界研究需要大数据的支持
真实世界研究(real world research, RWR)起源于实用性临床试验,最早应用于药物流行病学范围。指在较大的样本量(覆盖具有代表性的更广大受试人群)的基础上,在真实医疗过程中,根据患者的实际病情和意愿非随机选择治疗措施,开展长期评价,并注重有意义的结局治疗,在广泛真实医疗过程中评价干预措施的外部有效性和安全性与传统临床试验不同的是,真实世界的研究不会基于特定的患者群和特定的研究环
MedSci原创 - 真实世界,大数据 - 2017-05-23
国家药监局药审中心关于发布《用于产生真实世界证据的真实世界数据指导原则(试行)》
为进一步指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发,药审中心组织制定了《用于产生真实世界证据的真实世界数据指导原则(试行)》(见附件)。
国家药品监督管理局药品审评中心 - 2021-04-15
利用真实世界数据做好研究,来看诸多经典研究实例
近年来,研究者们对真实世界研究的关注度越来越高,希望通过真实世界数据解决临床试验数据无法回答的临床和政策问题。
医咖会 - 真实世界数据 - 2019-03-12
Vertex显示了CF药物Kalydeco益处的真实世界数据
Vertex提供了长期的观察数据,强调了Kalydeco对囊性纤维化患者的益处。使用来自两个大型独立囊性纤维化(CF)的真实世界数据,将用该药物(一种囊性纤维化跨膜(CFTR)调节剂)治疗的患者与从未接受过这种治疗的匹配患者的比较组进行比较。
MedSci原创 - Kalydeco,真实世界 - 2018-06-10
真实世界数据:诺华Entresto®可改善心衰患者生存质量
11月12日,诺华制药公布了一项来自德国的真实世界研究数据,数据来自射血分数下降的心衰(HFrEF)患者接受了Entresto® (sacubitril/valsartan)治疗。研究数据进一步支持了Entrest
新浪医药 - Entresto,诺华,真实世界数据 - 2017-11-23
《用于产生真实世界证据的真实世界数据指导原则(试行)》
为进一步指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发,药审中心组织制定了《用于产生真实世界证据的真实世界数据指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品
国家药品监督管理局药品审评中心 - 真实世界数据,真实世界研究 - 2021-04-15
用于产生真实世界证据的真实世界数据指导原则(征求意见稿)
为进一步指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发,我中心组织起草了《用于产生真实世界证据的真实世界数据指导原则(征求意见稿)》,现在中心网站予以公示,以广泛听取各界意见和建议,欢迎
CDE - 指导原则 - 2020-09-01
FDA:CVM GFI #266 使用真实世界数据和真实世界证据来支持新动物药物的有效性
本指南描述了 CVM 打算如何评估提交给 CVM 的真实世界数据和真实世界证据,以证明新动物药物申请的有效性的实质性证据或新动物药物有条件批准申请的有效性的合理预期。 它还提供有关申办者如何在提交申请
FDA - 真实世界数据 - 2021-10-24
如何高效收集真实世界数据(RWD)杏树林有良方
美通社 - 2017-07-10
FDA指导原则:包含真实世界数据的药品和生物制品提交数据标准
《21 世纪治愈法案》于 2016 年 12 月 13 日签署成为法律,旨在加速医疗产品开发,并更快、更有效地为有需要的患者带来创新。 除其他规定外,《21 世纪治愈法案》在《联邦食品、药品和化妆品法
FDA - 真实世界,真实世界数据 - 2021-10-24
为您找到相关结果约500个