辉瑞的美罗华(利妥昔单抗)仿制药Ruxience,获得欧盟批准
Ruxience被批准用于治疗非霍奇金淋巴瘤(NHL)、慢性淋巴细胞性白血病(CLL)、类风湿性关节炎(RA)、肉芽肿伴多血管炎(GPA)和显微多血管炎(MPA)和寻常型天疱疮(PV)。
MedSci原创 - 利妥昔单抗,生物仿制药,欧盟批准,RUXIENCE - 2020-04-04
辉瑞的美罗华仿制药RUXIENCE的营销申请,获得欧盟人用药物委员会的积极评价
辉瑞公司宣布,其美罗华(利妥昔单抗)的潜在的生物仿制药RUXIENCE的营销授权申请,获得欧洲药品管理局(EMA)的人用药品管理委员会(CHMP)的积极意见。
MedSci原创 - 辉瑞,美罗华,仿制药,RUXIENCE,欧盟,人用药物委员会,积极评价 - 2020-02-02
美罗华再迎新对手,第二款国产利妥昔单抗上市
昨日(10月9日),据国家药监局官网数据显示,信达生物的利妥昔单抗注射液(商品民:达伯华)获批上市,根据信达生物发布的公告,该药将用于治疗弥漫性大B细胞淋巴瘤、滤泡性淋巴瘤及慢性淋巴细胞性白血病,这也
医谷网 - 美罗华,利妥昔,考核制度 - 2020-10-10
FDA对抗体生物仿制药产品批准在2019年明显增加
抗体协会的调查结果显示,美国食品和药物管理局(FDA)对生物仿制药抗体治疗药物的批准在2019年显着增加。今年前七个月共批准了六种抗体产品。
MedSci原创 - FDA,抗体生物仿制药,批准增加 - 2019-08-10
2019 FDA:批准42款新药9款生物类似药 3款在路上
截止到2019年11月29日,今年FDA共批准42款新药、9款生物类似药,另外还有3款新药的PDUFA时间在12月,预计2019年将有45款新药获得FDA批准。相较于2017年和2018年,2019年会是FDA批准新药数量最低的一年,但质量不差,比如Skyrizi、Zolgensma、Rozlytrek和Brukinsa。本文总结了2019年FDA批准的42款新药、9款生物类似药,以及12月份面临
CPHI制药在线 - FDA,药品审批,生物类似药 - 2019-12-02
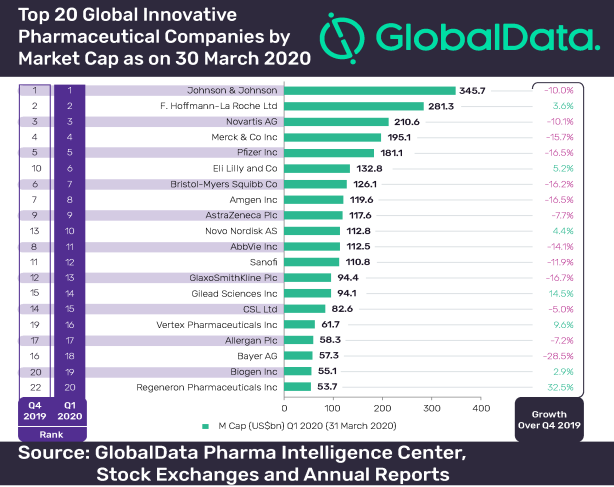
2020 Q1各大药企收入排名,强生,罗氏,诺华,默沙东,辉瑞,礼来,阿斯利康......
4月份,强生,礼来,GSK,辉瑞、诺华、默沙东相继发布了2020年第一季度财报。在疫情的笼罩之下,今年注定是不平凡的一年。而对于跨国药企而言,其开年业绩就上演了“王座更迭”的戏
MedSci原创 - 辉瑞,罗氏,药企,阿斯利康,强生,诺华 - 2020-05-03
为您找到相关结果约6个