APL Bioengineering:深圳实验室侯尚国团开发利用光学显微研究液体-液相分离的方法综述
2023-05-18 iNature iNature 发表于上海
该综述总归结了各种光学形成方法在研究LLPS中的优点。最后,讨论了适用于LLPS 研究的潜在未来形成工具和方法。
细胞内液-液相分离(Liquid–liquid phase separation,LLPS)是生物分子动态结合和无细胞器(Membraneless organelles,MLOs)形成的关键过程,在调节生物分子相交互作用和精细肌肉功能方法起着至关重要的作用。在分水平上对细节细胞LLPS机制的全面理解是至关重要的,LLPS已被证明与多种疾病的发病机制密切相关,包例如神经退行性病,如肌萎缩性侧索硬化症( ALS)【1】、额增叶痴呆(FTD)【2】、阿尔茨海默病(AD)【3】、和帕金森病(PD)【4】,它还与实体瘤相关,包括乳腺【5】、结肠白(CC)【6】等。
2023年5月,深圳湾实验室侯尚国家队和合作团队在APL Bioengineering 上发表题目为“ Study liquid–liquid phase separation with optical microscopy: A methodology review ”的综述文章介绍了用LLPS研究的光学成像方法。综述首先简要介绍了LLPS的分机制造,然后回顾了LLPS研究中使用的光学合成方法和光探针。而且,该综述总归结了各种光学形成方法在研究LLPS中的优点。最后,讨论了适用于LLPS 研究的潜在未来形成工具和方法。
总的来说,综上所述在为LLPS研究选择合适的光学合成方法提供参考,LLPS研究的合成方法的选择取决定于各种原因,可能有必须使用多种技术来全面了解LLPS。LLPS的深入研究有帮助我们更好地理解生物成分的相互作用和无细胞器的功能,并希望为相关疾病的治疗和预防提供新的思路和策略。

与LLPS的蛋白质历史单一分解状态和液体状态之间的转变,受到各种环境因素的影响,如盐、温度、CO 2 /O 2 水平、光照、吸附剂、pH和ATP等(图1 ) 。小的相分离液体通过融合或奥斯特瓦德熟化形成大的液体【7】。随着液体滴的老化,它们转变成凝胶状态。结构或麦克斯韦眼镜【8】。LLPS的主要驱动力包包括静电和疏水相互作用,如cation-anion、cation-p、p-p、dipole-dipole、helix-helix、coiled-coil、steric zipper和oligomerization。
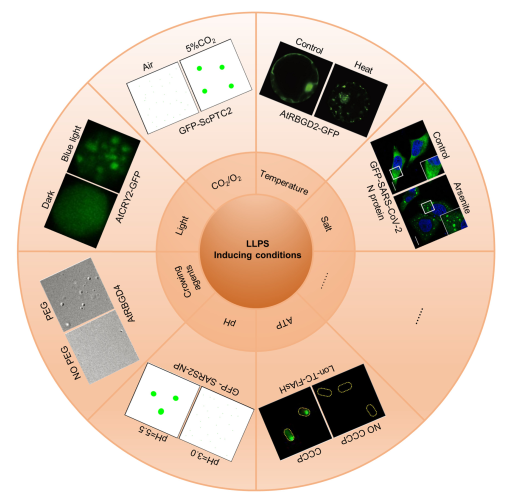
LLPS诱导条(图源自Applied Physics Letters Bioengineering)
光学显微镜作为观察LLPS的主要技术,在LLPS中发着着不可或缺的作用。目前通过微分干触比显微镜(DIC)、宽视场视野显微镜(Wide-field)、共聚焦显微镜(Confocal)、全内镜反射橄榄光显微镜(TIRF)、超分光率显微镜(SMLM和SIM)、橄榄光相关光谱(FCS)、橄榄光修复(FREP)和Capflex在体内外观察或表格征相分离。从观察效率、分离率、灵敏度、形成速度、光毒性和光效白效应等方面总归结了各种光学形成方法在研究LLPS中的优点。通过对这些方法的评价,可以为研究人员选择合适的光学合成方法提供参考。
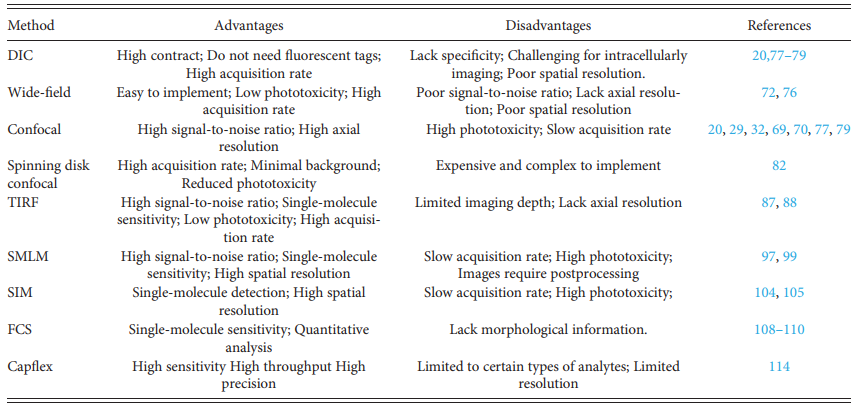
LLPS研究中光学成像方法的比较(图源自Applied Physics Letters Bioengineering)
未来,具备高时空精度、高灵敏度和大成影像野外等优点的三维单元跟踪技术将在LLPS研究中发展越来越重要的作用【9-15】。另一种方便,镜片显微镜头配件高速成像和低剂量等优势【16-18】,使之可能长期观察LLPS,通过连续观察样品,在不同时间点上获取图像数据,可以显示LLPS动力学的变化和演化过程。另外,随着机器学习在图像数据处理领域的快速发展,它也在LLPS研究中发挥着越来越重要的角度【19,20】。机器人学习的方法,可以从大量的图像数据中提取有关系LLPS的成分信息,帮助我们更好地理解LLPS的形状制作和交互作用过程。综合而言,未来的LLPS研究将有助于三维单分子跟踪技术、光学片显微镜和机器学习等方法的发展并得到了一步推动。这些新技术的应用将加深我们对LLPS的认识,促进对相关疾病发生机制的理解,并为治疗和预防提供新的策略和方法。
侯尚国课题组致力于高时空分辩三维光学成象方向研究,为新兴前沿研究领域;研究方向为开发超时空间分离三维成像技术并将其应用于相关动态生物系统研究。因课题组科研工作需要,招收光学、生物学、化学等相关背景的博士后(2名)、研究助理(3名)。欢迎优秀青年联盟,在这里你可以获得玩乐高积木和专辑商业摄影的快乐,满足你探索精细肌肉运动的奥秘的好奇心。
课题组主页:http://houlab.szbl.ac.cn/
1 D. Pakravan、G. Orlando、V. Bercier 和 L. Van Den Bosch,“液-液相分离在肌萎缩侧索硬化症中的作用和治疗潜力”,J. Mol。细胞生物学。13(1), 15 (2021).https://doi.org/10.1093/jmcb/mjaa049
2 T. Murakami、S. Qamar、JQ Lin、GS Schierle、E. Rees、A. Miyashita、AR Costa、RB Dodd、FT Chan、CH Michel、D. Kronenberg-Versteeg、Y. Li、SP Yang、Y. Wakutani、W. Meadows、RR Ferry、L. Dong、GG Tartaglia、G. Favrin、WL Lin、DW Dickson、M. Zhen、D. Ron、G. Schmitt-Ulms、PE Fraser、NA Shneider、C. Holt、 M. Vendruscolo、CF Kaminski 和 P. St George-Hyslop,“ALS/FTD 突变诱导的 FUS 液滴和可逆水凝胶向不可逆水凝胶的相变会损害 RNP 颗粒功能,”Neuron 88(4), 678 (2015) .https://doi.org/10.1016/j.neuron.2015.10.030
3 S. Boyko、K. Surewicz 和 WK Surewicz,“液-液相分离条件下 tau 蛋白原纤维化的调控机制”,Proc。国家队。学院。科学。美国 117(50), 31882 (2020).https://doi.org/10.1073/pnas.2012460117
4 S. Mukherjee、A. Sakunthala、L. Gadhe、M. Poudyal、AS Sawner、P. Kadu 和 SK Maji,“α-突触核蛋白的液-液相分离:α-突触核蛋白聚集的新机制洞察帕金森病的发病机制,”J. Mol。生物学。435, 167713 (2022).https://doi.org/10.1016/j.jmb.2022.167713
5 Y. Huang , P. Li , K. Sun , K. Yin , W. Zhang , and Z. Wang ,“液-液相分离相关基因综合分析预测乳腺癌预后”,Front Genet。13, 834471 (2022). https://doi.org/10.3389/fgene.2022.834471
6 D. Qin、R. Wei、S. Zhu、L. Min 和 S. Zhang,“MiR-490-3p 通过 LLPS 依赖性 miRISC 系统沉默 CDK1 并抑制结肠癌的增殖”,Front。摩尔。生物科学。8, 561678 (2021).https://doi.org/10.3389/fmolb.2021.561678
7 CP Brangwynne,“无膜细胞器的相变和尺寸缩放”,J. Cell Biol。203(6), 875 (2013).https://doi.org/10.1083/jcb.201308087
8 S. Boeynaems、S. Alberti、NL Fawzi、T. Mittag、M. Polymenidou、F. Rousseau、J. Schymkowitz、J. Shorter、B. Wolozin、L. Van Den Bosch、P. Tompa 和 M. Fuxreiter ,“蛋白质相分离:细胞生物学的新阶段,”Trends Cell Biol。28(6), 420 (2018).https://doi.org/10.1016/j.tcb.2018.02.004
9 H. Cang、CM Wong、CS Xu、AH Rizvi 和 H. Yang,“具有并发光谱读数的单个纳米粒子的共聚焦三维跟踪”,Appl。物理。莱特。88(22), 223901 (2006).https://doi.org/10.1063/1.2204652
10 S. Hou、J. Exell 和 K. Welsher,“实时 3D 单分子跟踪”,Nat。公社。11(1), 3607 (2020).https://doi.org/10.1038/s41467-020-17444-6
11 S. Hou、C. Johnson 和 K. Welsher,“实时 3D 单粒子跟踪:迈向活细胞中的主动反馈单分子光谱学”,分子 24,2826(2019 年)
12 S. Hou、X. Lang 和 K. Welsher,“使用动态移动激光点进行稳健的实时 3D 单粒子跟踪”,选择。莱特。42(12),2390(2017)。
13 S. Hou 和 K. Welsher,“实时 3D 单粒子跟踪协议”,J. Visualized Exp。131, 56711 (2018).https://doi.org/10.3791/56711
14 S. Hou 和 K. Welsher,“一种用于监测病毒首次接触的自适应实时 3D 单粒子跟踪方法”,Small 15(44),e1903039 (2019)。
15 MF Juette 和 J. Bewersdorf,“具有亚毫秒时间分辨率的单个荧光粒子的三维跟踪”,Nano Lett。10(11), 4657 (2010)。
16 EMC Hillman、V. Voleti、W. Li 和 H. Yu,“神经科学中的光片显微术”,Annu。神经科学牧师。42, 295 (2019).https://doi.org/10.1146/annurev-neuro-070918-050357
17 E. Sapoznik、BJ Chang、J. Huh、RJ Ju、EV Azarova、T. Pohlkamp、ES Welf、D. Broadbent、AF Carisey、SJ Stehbens、KM Lee、A. Marin、AB Hanker、JC Schmidt、CL Arteaga , B. Yang , Y. Kobayashi , PR Tata , R. Kruithoff , K. Doubrovinski , DP Shepherd , A. Millett-Sikking , AG York , KM Dean , 和 RP Fiolka ,“用于大尺度和亚细胞动力学的高分辨率成像”,eLife 9,
18 EHK Stelzer、F. Strobl、B.-J。Chang、F. Preusser、S. Preibisch、K. McDole 和 R. Fiolka,“光片荧光显微镜”,Nat。Rev. Methods Primers 1(1), 73 (2021). https://doi.org/10.1038/s43586-021-00069-4
19 MS Durkee、R. Abraham、MR Clark 和 ML Giger,“组织显微镜图像中的人工智能和细胞分割”,Am。J.帕索尔。191(10), 1693 (2021).https://doi.org/10.1016/j.ajpath.2021.05.022
20 X. Fuyong、X. Yuanpu、S. Hai、L. Fujun 和 Y. Lin,“显微镜图像分析中的深度学习:一项调查”,IEEE Trans。神经网络学习。系统。29(10), 4550 (2018).https://doi.org/10.1109/TNNLS.2017.2766168
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







