D-VMP对比VMP治疗不适合移植亚洲NDMM的3期OCTANS研究结果
2023-04-23 聊聊血液 网络 发表于上海
与全球 ALCYONE 研究的结果相比,D-VMP在亚洲患者中表现出一致的疗效和安全性。
在 III 期 ALCYONE 研究中(中位随访16.5个月),与 VMP 单独治疗相比,达雷妥尤单抗联合 VMP (D-VMP) 可显著延长不适合移植的 NDMM 患者的无进展生存期 (PFS)(中位PFS未达到vs. 18.1个月;风险比 [HR]=50;P<0.001)。在 ALCYONE 的更新分析中(中位随访40.1个月),D-VMP继续显示显著的 PFS 获益(中位PFS 36.4个月vs. 19.3个月;HR=42; P<0.0001),并显著延长总生存期(中位OS均未达到,HR=0.60;P=0.0003)
为了确认 D-VMP 在亚洲患者中的疗效和安全性,中韩等国血液科专家共同开展了一项III期 OCTANS 研究,近日《Clinical Lymphoma Myeloma & Leukemia》报道了预先设定的主要分析结果,通讯作者为侯健教授和王建祥教授,第一作者为傅卫军教授。

OCTANS研究是一项多中心、随机、开放标签、活性对照III期研究,在中国、香港特别行政区、中国台湾、韩国和马来西亚39家研究中心入组患者,主要入组条件包括≥18岁、新诊断MM、因年龄(≥65岁)或合并症而不适合ASCT,以2:1的比例随机接受 D-VMP 或 VMP 治疗。OCTANS研究方案与ALCYONE研究基本一致。
所有患者均接受最多9个周期(42天/周期)的硼替佐米(1.3 mg/m2皮下注射,第1周期第1、2、4和5周每周两次,第2-9周期第1、2、4和5周每周一次)、美法仑(9 mg/m2口服,每个周期第1-4天每天一次)和泼尼松(每周期第1-4天口服60 mg/m2,每日1次)。D-VMP 组患者在第1周期每周一次接受达雷妥尤单抗 16 mg/kg 静脉给药,第2-9周期每3周一次,此后(第10+周期)每4周一次直至疾病进展或出现不可接受的毒性。在2020年06月24日发布方案修正案后,接受达雷妥尤单抗静脉给药的患者可以选择换用达雷妥尤单抗皮下给药。达雷妥尤单抗以固定剂量 1800 mg 通过手动注射至腹部皮下组织中,注射时间约为3-5 min,每4周一次。在每个 D-VMP 周期的第1天,用地塞米松 20 mg 替代泼尼松作为输注前治疗。
主要疗效终点为≥VGPR率。
患者和治疗
分别有220例患者随机分配至 D-VMP 组 (n=146) 和VMP 组(n=74;图1)。

大多数患者(167例 [75.9%] 患者)来自中国。治疗组之间的人口统计学和基线特征大体平衡(表1)。中位年龄为69岁,21.9%的患者有高危细胞遗传学异常。

临床截止日期时(2020年07月02日),在接受≥1次研究治疗的215例(D-VMP组n=144;VMP组n=71)患者中,D-VMP组31例 (21.5%) 患者和 VMP 组26例 (36.6%) 患者在第1-9周期停止治疗(图1),最常见的停药原因为疾病进展(第1-9周期内,D-VMP组和 VMP 组分别有14例 [9.7%] 和15例 [21.1%] 患者),接受的中位治疗周期分别为8.0和7.0,中位治疗持续时间为11.0个月和9.9个月。第1周期、第2-9周期和第10 + 周期达雷妥尤单抗的中位相对剂量强度分别为100%、97.7%和98.8%。两组之间硼替佐米、美法仑和泼尼松当量的中位相对剂量强度相似(硼替佐米分别为87.4%和88.7%;美法仑分别为93.1%和94.4%;泼尼松当量分别为98.9%和99.3%)。
疗效
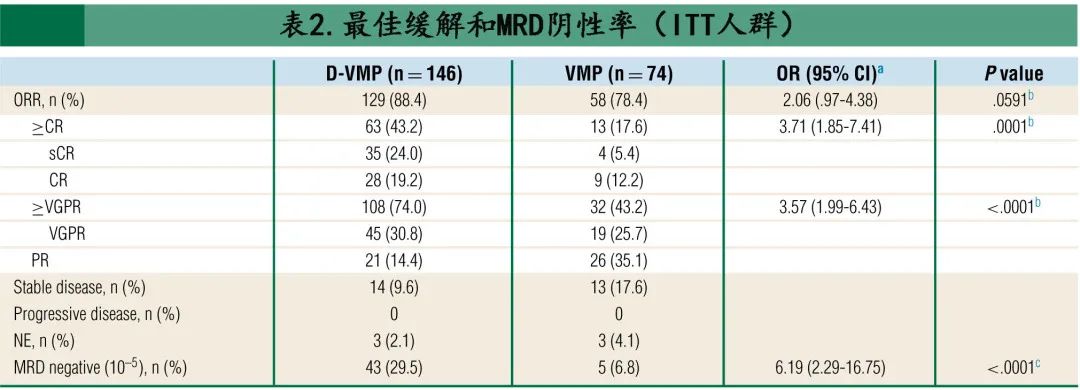
在 ITT 人群(D-VMP组n=146;VMP组n=74)中,D-VMP组≥VGPR率较 VMP 组显著改善(74.0% vs. 43.2%;OR=3.57;95%CI,1.99-6.43;P<0.0001;表2)。此外D-VMP 组的 ORR 为88.4%,VMP组为78.4%(OR=2.06;95%CI,97-4.38; P=0.0591),≥CR率也更高(43.2% vs. 17.6%;0R=3.71;95%CI,1.85-7.41;P=0.0001;表2)。至首次缓解的中位时间为0.79个月和0.82个月,至≥VGPR的中位时间为2.2个月和1.8个月,至≥CR中位时间分别为5.8个月和6.1个月。两组的中位缓解持续时间均无法估计。D-VMP 组在10-5灵敏度阈值下的 MRD 阴性率高于 VMP 组(29.5% vs. 6.8%;OR=6.19;95%CI,2.29-16.75;P<0.0001)。
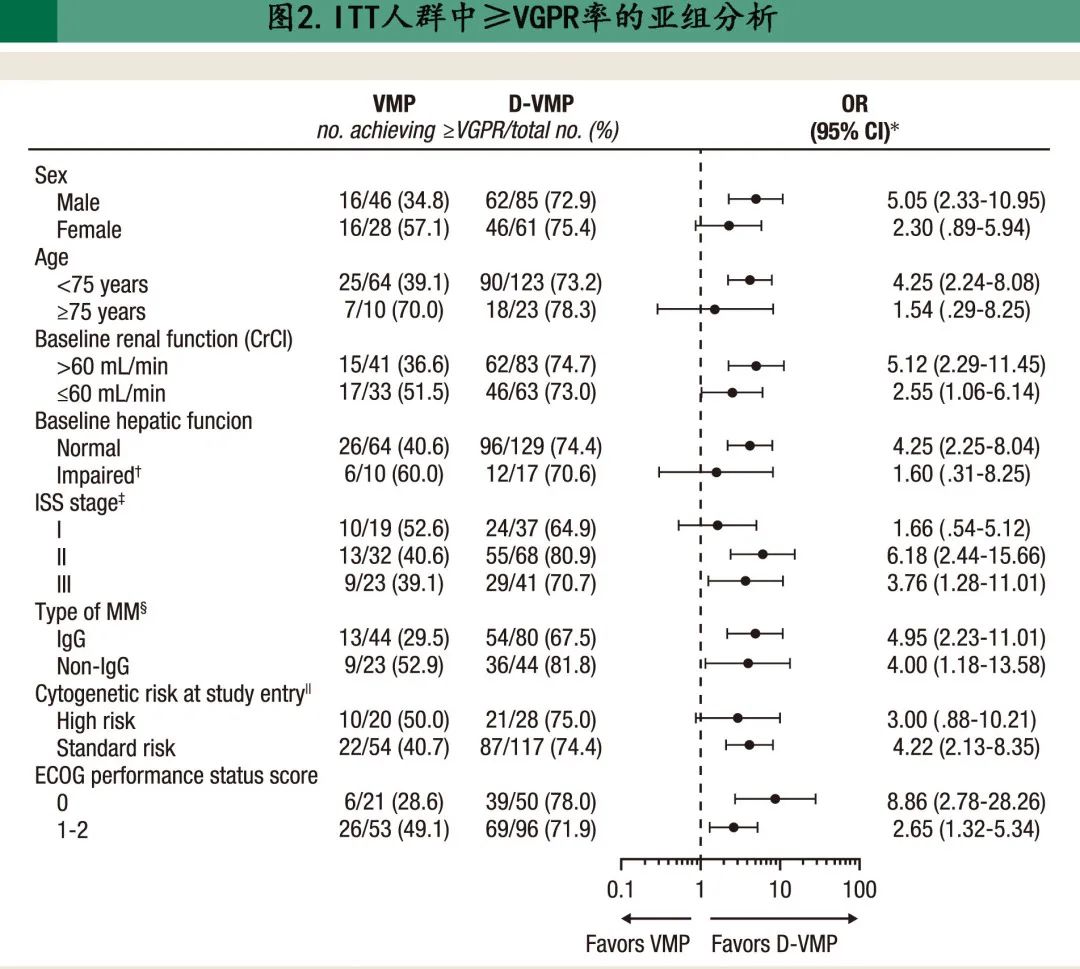
预先设定的≥VGPR率亚组分析证明,在 ITT 人群中观察到的 D-VMP 优于 VMP 的结果在各亚组(包括肾损害、ISS III期和高危细胞遗传学异常患者)中基本一致(图2)。
中位随访12.3个月,D-VMP组较VMP组显著延长了PFS(中位PFS未达到 vs. 18.2个月;HR=0.43; 95% CI, .24-.77; P=0.0033;图3)。D-VMP 组估计的12个月 PFS 率为84.2%,VMP组为64.6%。在许多预先规定的亚组中进一步观察到 D-VMP 与 VMP 相比的 PFS 获益。D-VMP 组至下次治疗或因疾病进展死亡的中位时间未达到,VMP组为16.7个月(HR=0.26; P<0.0001)。本分析时D-VMP组和 VMP 组分别共有15例 (10.3%) 和7例 (9.5%) 死亡;OS随访正在进行中。

安全性
最常见(任一组中≥20%的患者)和最常见(任一组中≥5%的患者)的任何级别治疗中出现的不良事件 (TEAE) 总结见表3。在第1-9周期内,两个治疗组的所有治疗患者均发生任何级别TEAE;D-VMP组128例 (88.9%) 患者和 VMP 组59例 (83.1%) 患者发生3/4级TEAE。第1-9周期任一治疗组中≥10%的患者发生的3/4级 TEAE 为血小板减少症(D-VMP组46.5%;VMP组45.1%)、中性粒细胞减少症 (39.6%,50.7%)、白细胞减少症 (31.3%,36.6%)、淋巴细胞减少症 (30.6%,22.5%)、贫血 (24.3%,26.8%)、感染性肺炎 (27.8%,14.1%) 和低钾血症 (13.2%,2.8%)。第1-9周期内,D-VMP组 (66.7%) 的感染发生率高于 VMP 组 (50.7%),主要是任何级别和3/4级感染性肺炎(任何级别35.4% vs. 18.3%;3/4级27.8% vs. 14.1%)以及上呼吸道感染(任何级别27.1% vs. 15.5%;3/4级7.6% vs. 1.4%)。D-VMP 组1例患者在第2-9周期发生最大级别为2级的乙型肝炎病毒再激活;VMP组无患者发生乙型肝炎病毒再激活。在第1-9周期内,D-VMP组和 VMP 组分别有3例 (2.1%) 和1例 (1.4%) 患者因感染终止治疗。2例患者在周期1-9期间因感染死亡:D-VMP组1例(7%)患者死于感染性肺炎,VMP组1例 (1.4%) 患者死于脓毒性休克。
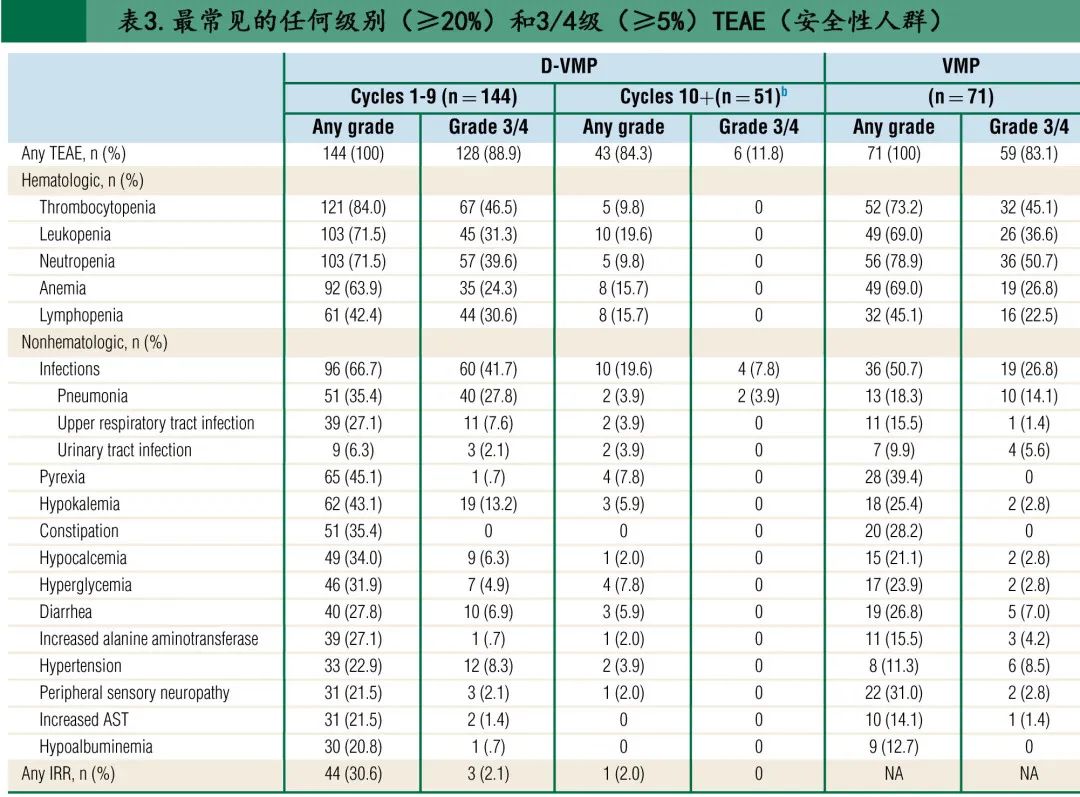
在第1-9周期,D-VMP组和 VMP 组分别有63例 (43.8%) 和25例 (35.2%) 患者发生严重不良事件 (SAE)。最常见(任一组中≥5%的患者)的 SAE 为感染性肺炎(D-VMP组18.1%;VMP组4.2%)和血小板减少症 (6.9%;7.0%)。总体而言,D-VMP组 (82.6%) 中导致任何研究治疗周期延迟或剂量调整的 TEAE 发生率高于 VMP 组 (69.0%),两个治疗组中导致治疗终止的 TEAE 发生率均较低且相同(均为4.2%)。在第1-9周期内,D-VMP组和 VMP 组分别有4例 (2.8%) 和3例 (4.2%) 患者发生导致死亡的TEAE。总体而言,D-VMP组仅1例(7%)发生第二原发恶性肿瘤(8个治疗周期后发生的胰腺癌,研究者评估后认为与达雷妥尤单抗无关),而VMP组为0例患者;无患者发生肿瘤溶解综合征。
在 D-VMP 组接受达雷妥尤单抗单药治疗(第10+周期)的患者中,43例 (84.3%) 患者在第10+周期发生任何级别TEAE(表3)。6例 (11.8%) 患者在第10+周期发生3/4级TEAE:肺炎和 C 反应蛋白升高(各2例 [3.9%] 患者)最常见。第10+周期感染的发生率为19.6%;肺炎、上呼吸道感染和尿路感染(各2例 [3.9%] 患者)最常见。第10+周期无患者发生乙型肝炎复发,无患者因 TEAE 而中止治疗。5例 (9.8%) 患者在第10+周期发生SAE;肺炎(2例 [3.9%] 患者)最常见。1例 (2.0%) 患者在第10+周期死于TEAE(肺炎和呼吸衰竭)
在 OCTANS 研究中,不适合移植的亚洲 NDMM 患者D-VMP治疗的≥VGPR率显著高于 VMP 单独治疗组(74% vs. 43%;OR=3.57;95%CI,1.99-6.43;P<0.0001),≥CR率和 MRD 阴性率也显著高于后者。此外中位随访12.3个月,与 VMP 相比D-VMP可显著改善PFS(HR=43; 95% CI, 0.24-0.77; P=0.0033)。预先设定的≥VGPR率亚组分析显示,在各亚组(包括肾损害患者、ISS III期疾病患者和细胞遗传学异常高危患者)中,D-VMP均优于VMP。此外两个治疗组中均观察到患者报告的总体健康状况改善,在第9个月时 D-VMP 组相比 VMP 组具有显著差异,而在其余的评估时间点,使用和不使用达雷妥尤单抗时总体健康状况的改善相当。
总的来说,与全球 ALCYONE 研究的结果相比,D-VMP在亚洲患者中表现出一致的疗效和安全性,支持使用 D-VMP 治疗不适合移植的亚洲 NDMM 患者,也提供了关于四联 D-VMP 方案治疗亚洲患者获益的疗效和安全性数据。
参考文献
Weijun Fu, Soo-Mee Bang, Honghui Huang,et al. Bortezomib, Melphalan, and Prednisone With or Without Daratumumab in Transplant-ineligible Asian Patients With Newly Diagnosed Multiple Myeloma: The Phase 3 OCTANS Study.Clin Lymphoma Myeloma Leuk . 2023 Mar 4;S2152-2650(23)00073-3. doi: 10.1016/j.clml.2023.02.009.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言