PFS 翻倍!tipifarnib获FDA突破性疗法资格
2021-02-26 医药魔方 医药魔方
2月24日,Kura宣布,tipifarnib已被FDA授予突破性疗法认定,用于治疗铂类化疗后疾病进展、等位基因变异频率≥20%,复发或转移性HRAS突变型头颈部鳞状细胞癌(HNSCC)。
2月24日,Kura宣布,tipifarnib已被FDA授予突破性疗法认定,用于治疗铂类化疗后疾病进展、等位基因变异频率≥20%,复发或转移性HRAS突变型头颈部鳞状细胞癌(HNSCC)。 头颈部鳞状细胞癌是世界上第七大最常见癌症,每年有超过88.5万的新发病例。尽管近年治疗取得了进展,但患者预后仍然很差,5年生存率低于40%。二线治疗对许多患者的临床获益有限,客观缓解率(ORR)仅为6-16%,中位无进展生存期(PFS)为2-3个月,中位总生存期(OS)为5-8个月。尽管HRAS早在40多年前就被发现了,但目前还没有针对这种蛋白突变形式的肿瘤的特定治疗方法。
HRAS是原癌基因,是一种正常基因,通过编码蛋白质,帮助调节细胞生长和分化。但可因突变或表达增加而成为癌基因。4-8%的头颈鳞状细胞癌患者存在HRAS突变。tipifarnib是一种有效的、高选择性的法尼酰基转移酶抑制剂,法尼酰基转移酶是HRAS活性的关键酶。

tipifarnib分子结构式
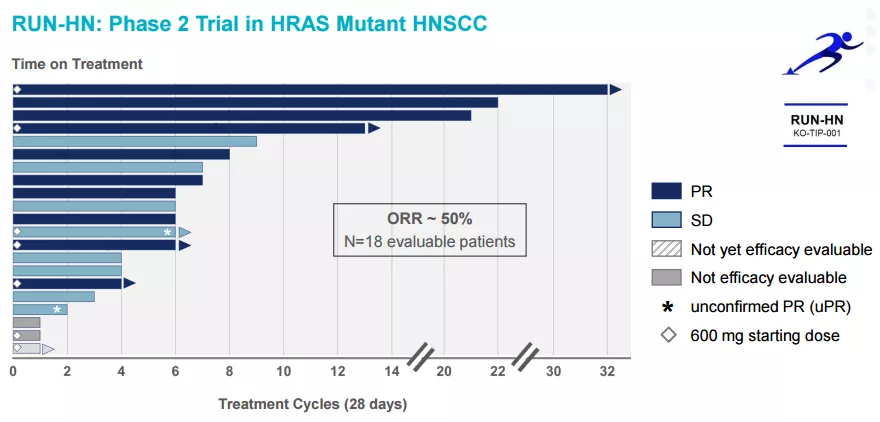
Tipifarnib突破性疗法认定是基于一项II期RUN-HN研究数据,该研究评估了tipifarnib在复发或转移性HRAS突变型头颈部鳞状细胞癌患者中的疗效。试验数据已于2020年5月在美国临床肿瘤学会上公布,18例疗效可评估患者的ORR为50%,中位PFS为5.9个月,中位OS为15.4个月。tipifarnib目前正在进行一项注册性临床研究(AIM-HN)。
Kura总裁兼首席执行官Troy Wilson博士说:“我们很高兴FDA授予tipifarnib突破性疗法称号,这是FDA对其治疗这种毁灭性疾病潜力的肯定。”我们将继续专注于AIM-HN注册性试验,并期待与FDA紧密合作,尽快将这种疗法应用于患者。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#PFS#
52
#突破性疗法#
30
#ARNI#
44