最新Nature Immunology:老年人的肿瘤微环境可能限制T细胞对癌症的控制
2024-05-16 BioMed科技 BioMed科技 发表于上海
研究员发现在老年肿瘤微环境(TME)中CD8+T细胞的有限启动在控制肿瘤方面的重要性超过了细胞固有缺陷。衰老中肿瘤生长的增加与CD8+T细胞浸润和功能的减少有关。
在癌症中,年龄相关免疫功能障碍的病因和影响尚不完全清楚。而在本研究中,麻省总医院Debattama R. Sen等人发现在老年肿瘤微环境(TME)中CD8+T细胞的有限启动在控制肿瘤方面的重要性超过了细胞固有缺陷。衰老中肿瘤生长的增加与CD8+T细胞浸润和功能的减少有关。由于T细胞功能障碍,从年轻小鼠转移T细胞也不能恢复老年小鼠对肿瘤的控制。至关重要的是,骨髓靶向治疗可以重振传统的1型树突状细胞,从而改善肿瘤控制,恢复衰老过程中的CD8+T细胞免疫。相关工作以“The aged tumor microenvironment limits T cell control of cancer”为题发表在Nature Immunology。

【文章要点】
目前,迫切需要消除衰老/衰老和衰竭在介导肿瘤内CD8+T细胞功能障碍中的影响,以改善癌症老年患者的预后。为此,还必须了解老年TME对CD8+T细胞分化和功能的广泛影响。在该研究中,作者发现衰老通过损害抗原特异性CD8+T细胞的持久性和增殖来损害对肿瘤的控制。研究发现,衰老的CD8+T细胞的增殖能力本质上是有限的,并且特别容易受到基因毒性应激的影响,这使它们容易在肿瘤中衰竭。相反,来自老年TME的信号改变独立地影响CD8+T细胞的分化,使其远离典型的T细胞耗竭(图1)。
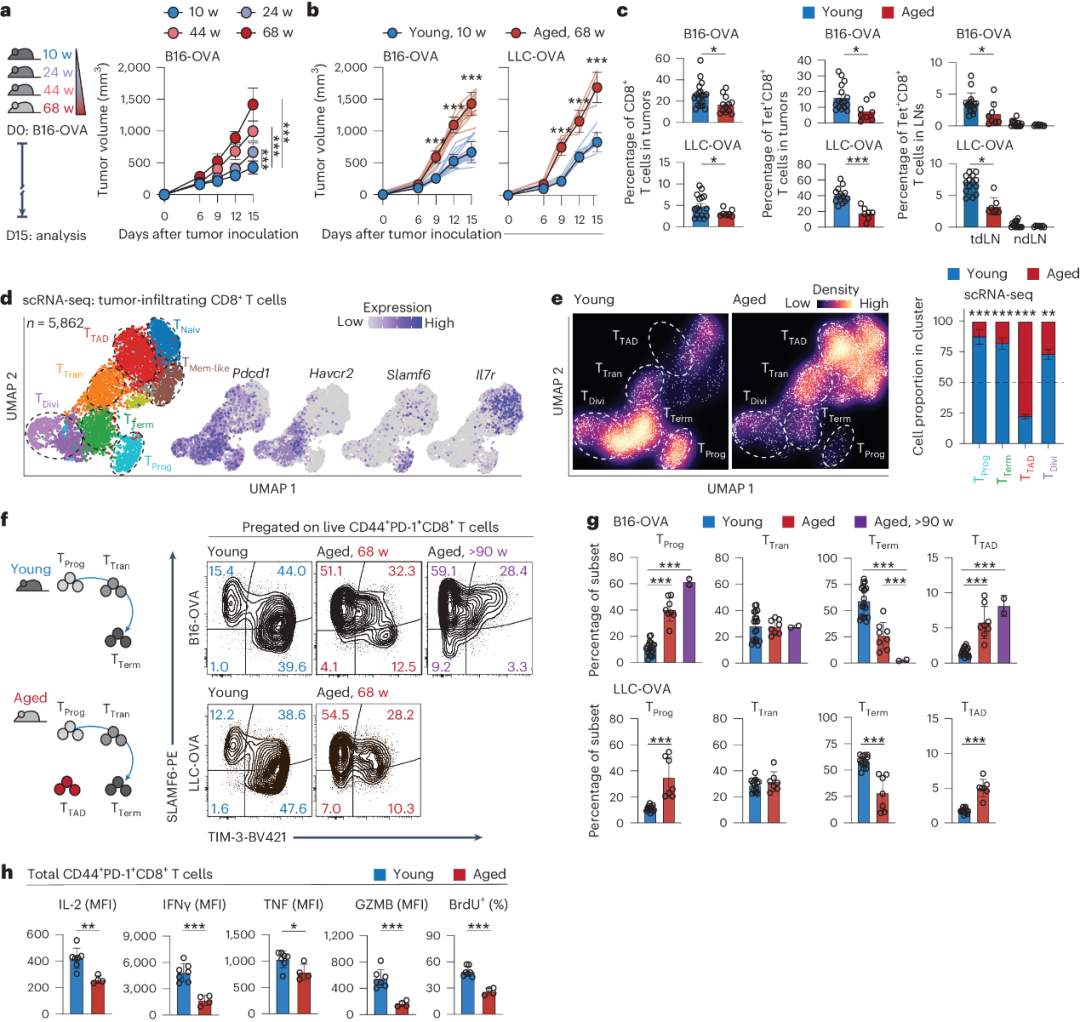
图1 衰老促进肿瘤生长、改变CD8+ T细胞的命运和效应功能
为此,作者在小鼠和人类肿瘤中鉴定了一个先前未知的功能失调的CD8+T细胞亚群,该亚群与衰老的TME特异性相关,在功能、转录和表观遗传学上与典型的耗尽CD8+T淋巴细胞不同。即老年TME中的细胞外源性信号驱动肿瘤浸润性年龄相关功能障碍(TTAD)细胞状态。至关重要的是,研究发现即使在转移的年轻CD8+T细胞中,衰老样细胞命运可以由来自衰老TME的细胞外源性信号诱导。因此,衰老的CD8+T细胞代表了一种独特的CD8+TT细胞谱系。最后,研究还发现,老年肿瘤中自然杀伤细胞-树突状细胞-CD8+T细胞串扰的改变削弱了传统1型树突状细胞(cDC1s)对T细胞的启动,并促进了TTAD细胞的形成。因此,老年小鼠不能从治疗性肿瘤疫苗接种中获益(图2)。最后,研究表明,骨髓靶向免疫疗法可以重振cDC1s,改善肿瘤控制,增强老年小鼠的CD8+T细胞免疫。
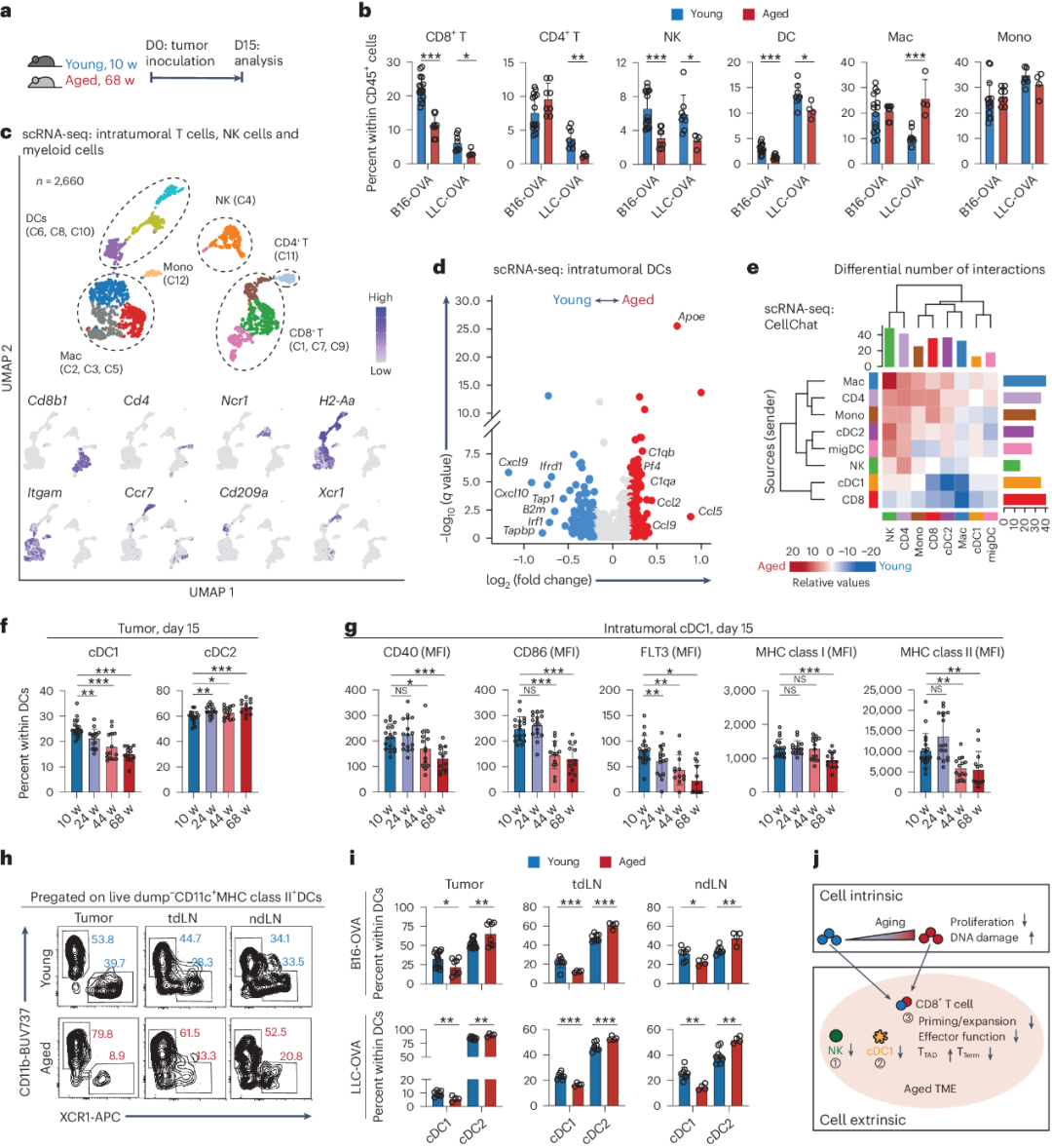
图2 老年TME侵蚀自然杀伤细胞-树突状细胞-CD8+T细胞串扰并损害-CD8+T细胞的启动和扩增
原文链接:
https://www.nature.com/articles/s41590-024-01828-7
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#癌症# #T细胞# #肿瘤微环境#
8