Cancer Discov:第四代EGFR抑制剂,突破点在哪?
2019-05-23 医药魔方 医药魔方Pro
EGFR,即表皮生长因子受体(epidermal growth factor receptor),也叫HER1或ErbB1,是人表皮生长因子受体(HER)家族成员之一。除了HER1(ErbB1,EGFR)之外,HER家族还包括HER2(ErbB2,neu)、HER3(ErbB3)及HER4(ErbB4)。
EGFR,即表皮生长因子受体(epidermal growth factor receptor),也叫HER1或ErbB1,是人表皮生长因子受体(HER)家族成员之一。除了HER1(ErbB1,EGFR)之外,HER家族还包括HER2(ErbB2,neu)、HER3(ErbB3)及HER4(ErbB4)。
EGFR广泛分布于哺乳动物上皮细胞、成纤维细胞、胶质细胞等细胞表面。EGFR信号通路对细胞的生长、增殖和分化等生理过程发挥重要的作用。EGFR突变也是非小细胞肺癌患者中最常见的一种突变类型,尤其是在亚洲人群中可以占到40%~50%,因此EGFR一直是制药产业研究的最热门靶点之一。
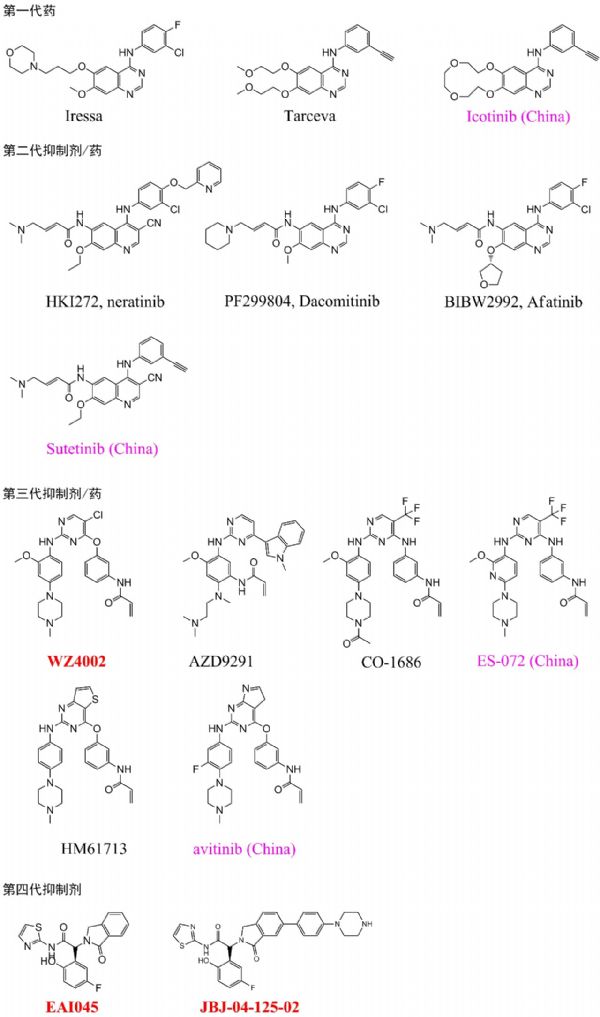
第一代EGFR抑制剂吉非替尼、厄洛替尼的上市显着改善了NSCLC患者的临床治疗结局,但是几乎不可避免的耐药问题迫使科学家们不断去开发探索新一代的EGFR抑制剂,专门针对T790M突变耐药的第三代EGFR抑制剂奥希替尼正是由此而生,解决了大约50%的EGFR抑制剂耐药问题。不过肿瘤细胞在药物压力下仍在不断变异,新的耐药问题随之而来,第四代EGFR抑制剂成为产业界和医生、患者的新期待。
5月15日,癌症领域顶级期刊《Cancer Discovery》(IF=24.37)发表了美国哈佛大学医学院丹娜法伯癌症研究所Michael Eck教授、Nathanael Gray教授和Pasi Janne教授团队的最新合作成果,报道了在首个第四代EGFR抑制剂EAI045基础上开发的小分子变构抑制剂JBJ-04-125-02,再次引起业内极大关注。
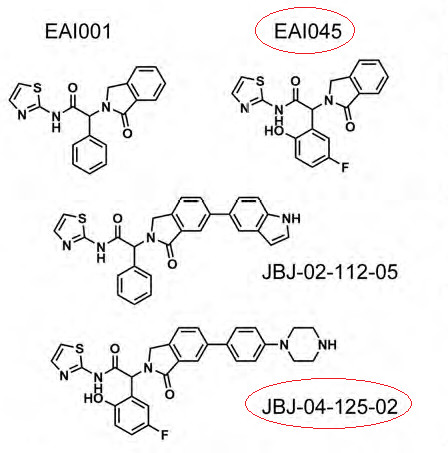
JBJ-04-125-02相比EAI045有何改进?能否成为四代EGFR抑制剂中的新星?第四代EGFR抑制剂的未来突破点在哪?我们为此特别采访了全球首个第四代EGFR抑制剂EAI045的共同研发人、曾在Michael Eck教授团队担任研究科学家并专职负责EGFR靶向药研发的云彩红教授。
云彩红教授
问:哈佛大学医学院近日在《Cancer Discov》上发表了第四代EGFR抑制剂JBJ-04-125-02的文章,您在哈佛大学工作期间也从事了第四代EGFR抑制剂的研发。对于他们的研究成果,您有何评价?
云彩红:首先我想对我的老师、长期密切合作的同事及朋友Michael Eck教授、Nathanael Gray教授和Pasi Janne教授表示衷心祝贺,也对参与这项研究的一线人员,其中有一些是我的老朋友或工作继任者,表示由衷的祝贺!
Cancer Discov杂志上这篇关于JBJ-04-125-02的论文是最近3年以来EGFR药物研发领域最令人激动的进展之一,该化合物以新的作用方式在动物模型上显示了令人振奋的效果。
JBJ-04-125-02实际上是我们2016年在Nature杂志上发表的全球首个EGFR异位型的、“第四代”抑制剂EAI045的“升级版”。EAI045是由哈佛大学与诺华制药这两大巨头合作研发。当时我是代表哈佛方面的核心人员,在概念提出、方案设计、结构药理学研究和初步药效研究等方面均做了比较多的关键工作。EAI045就好比我们共同的“孩子”一样。现在在EAI045的基础上进一步改进了这个化合物,得到了更好的JBJ-04-125-02,这个“孩子”终于长大了,所以我是非常高兴的。
问:您提到JBJ-04-125-02是EAI045的“升级版”,能否先给我们介绍一下EAI045的故事?
云彩红:这个故事就说来话长了,我可以大致介绍一下。大家知道EGFR突变型非小细胞肺癌中的主要类型(尤其是L858R和Del-19)对第一代EGRF抑制剂(易瑞沙、特罗凯、凯美纳)是敏感的,但用药过程中会产生耐药性,一半左右的耐药性是由于T790M突变所导致的。2008年我在美国科学院院报(PNAS)上发表了一篇专门研究T790M为什么会耐药的论文[2],这篇论文在阐明T790M耐药的机理的基础上实际上提示了克服T790M耐药的三种策略,因此这实际上是一项比较重要的工作。如今已经过去11年,这篇论文每年被引用次数超过100次,而且这个数字还在上升。
在PNAS论文的基础上,我们提出的三大新药研发策略已经有两个得到实现。
第一个策略是不可逆抑制。基于这一策略我们于2009年在Nature杂志发表了全球第一个EGFR“第三代”抑制剂WZ4002[3],尽管后来因为专利权益纠纷中止了研发,但WZ4002开创了两件事:一个是开创了用共价抑制策略能选择性抑制EGFR T790M耐药性突变,在动物模型中显示显着疗效和极低毒性;另一个是在EGFR抑制剂领域开创了使用氨基嘧啶这个新内核骨架,与第一代药基于4-苯氨基喹唑啉是完全不同的骨架。到了2013年前后公开发表的AZD9291、CO-1686等第三代抑制剂也全部都沿袭了WZ4002的这两个设计要点。众所周知,AZD9291后来脱颖而出成功上市,开始拯救千千万万的病人。
第二个策略就是非ATP竞争性抑制,即异位抑制策略。在我们之前,曾有人在其他激酶(比如Abl)上实现了异位抑制,但从来没有人知道EGFR激酶会存在异位抑制位点,我们开始时也不知道,仅仅是基于2008年 PNAS论文所发现的EGFRT 790M耐药原理坚信如果能实现对EGFR激酶的异位抑制,就有希望克服T790M耐药,所以当时仅仅是抱着试一试的态度来做这一尝试的,结果我们很幸运地发现了EAI001。EAI001经过初步改进设计以后就得到了EAI045,于2016年发表于Nature[4]。由于EAI045联用Cetuximab是第一个对EGFR新一代耐药突变L858R/T790M/C797S具备明确药效的抑制剂,且其骨架类型也与第一代药和第三代药完全不同,所以被誉为全球第一个EGFR“第四代”抑制剂,也是全球第一个EGFR异位型抑制剂。
但EAI045独立使用效果不佳,必须与Cetuximab抗体联用,而且仅仅对L858R/T790M/C797S有效,而对Del-19/T790M/C797S效果不佳,所以很显然需要进一步改进。JBJ-04-125-02就是在EAI045的基础上改进而来的,其核心骨架与EAI045完全相同。
问:JBJ-04-125-02相比EAI045主要有哪些改进?又有哪些不足?可能的应用范围是什么?
云彩红:JBJ-04-125-02的最主要改进是抑制EGFR L858R/T790M的能力比EAI045显着增强,使得原来必须与Cetuximab联用的异位抑制剂,现在即使单独使用都能显示比较好的抑制效果了。另外一个重要突破是JBJ-04-125-02可以与AZD9291联合使用,大大增强彼此药效。可能具备比较重要的临床应用价值(尽管这一联用只能解决L858R类型EGFR突变的问题):
第一,现有实验数据表明,JBJ-04-125-02联用AZD9291能显着增强彼此的药效。由于AZD9291对L858R/T790M的药效原本就没有对Del-19/T790M的药效那么好,JBJ-04-125-02对于L858R/T790M类型的病人来说可能会是一个很好的消息,可以弥补AZD9291对此类病人的作用不足;
第二,细胞水平的研究初步证明,当JBJ-04-125-02联用AZD9291时,新一代耐药性突变明显更加难以发生。如果将来在临床应用中也证明这一点,那么L858R/T790M类型的病人采用JBJ-04-125-02联用AZD9291疗法,不仅效果可能会更好,更重要的是可能不容易再耐药,这无疑是一个非常利好的消息。
所以,在我看来JBJ-04-125-02或许是第三代药的帮助者,可能能帮助AZD9291更好地完成作为第三代药的任务。这些数据带给了我们新的希望,但还没有经过临床的充分验证,其内在原因也不清楚,所以如果是患者朋友还是要慎重对待。
JBJ-04-125-02最大的不足是仍然不能很好的抑制Del-19、Del-19/T790M或Del-19/T790M/C797S。由于第三代药AZD9291使用以后病人发生新一代耐药情况中Del-19/T790M/C797S比较常见,而JBJ-04-125-02不能很好抑制Del-19/T790M/C797S,所以这一新药研发成果对大多数即将或已经产生耐药性的病人来说还是没有能解决燃眉之急。
第二点不足,它仍然会有一些“惧怕”EGFR二聚体化。根据现有数据来看,如果EGFR表达量较高,或者病人体内EGF浓度较高,从而导致EGFR形成二聚体较多,超过某个“阈值”的话,那么JBJ-04-125-02就会像EAI045一样单药变得不那么有效。但好在这个情况比EAI045改善了不少,而且如果与AZD9291联用,则能更好地克服这个问题。AZD9291不仅比Cetuximab便宜,而且与异位抑制剂联用时的叠加毒性可能也比后者小。
鉴于以上观点,我想JBJ-04-125-02也许还比较难以完成大家所期待的“第四代药”的任务。因为L858R/T790M/C797S发生几率较低,而JBJ-04-125-02对Del-19/T790M/C797S又不太有效。
问:既然JBJ-04-125-02还不够完美,那么您认为下一步研发工作的重点和突破点是什么呢?
云彩红:这个非常清楚,毫无疑问就是要抓紧研发能克服Del-19/T790M/C797S的“第四代药”,这一点也是JBJ-04-125-02这篇论文里明确提出的观点。由于目前所发现的EGFR异位抑制位点与Del-19类型的突变不兼容,所以研发克服Del-19/T790M/C797S的“第四代药”可能得采取其他策略,异位抑制策略不一定行得通。或者如果能发现EAI045/JBJ-04-125-02作用位点之外的、全新的异位作用位点,则也有可能能解决这个问题。
问:您认为EAI045和JBJ-04-125-02的案例能给我们国内的新药研发带来哪些启发?
云彩红:在EAI045和JBJ-04-125-02的研发过程中,结构药理学研究在里边起到了非常重要的作用。从2008年PNAS论文的结构药理学工作阐明T790M耐药机理,启发WZ4002和EAI045的研发,一直到JBJ-04-125-02的成功研发,结构药理学家从战略高度、方案设计、具体实施直至新抑制剂的正确用法等各个层面都发挥了关键性作用。如果没有结构药理学的指引,我们根本想不到要做这样一类抑制剂,更想不到怎样去使用这类抑制剂。
事实上,我与国际顶级制药公司合作的时间超过了15年,从我的个人经验看,国际大型药企是非常重视、而且越来越重视结构药理学在新药研发工作中的作用。药物化学专家、药效研究专家和结构药理学家一样,都是新药源头研发最核心的人员。如果新药研发好比盖一座新房子,患者是需要买房子住的人,那么药物化学专家非常像建筑公司。房子建得多了,即使没有专门设计公司设计,建筑公司也能盖出可以住人的房子来的,但也许就不一定那么高效、那么符合用户的需要。而结构药理学也许有点像设计公司,可以帮助建筑公司高效而且精准地把房子盖好,而像贝聿铭先生这样的建筑设计大师则可以设计出符合极端严苛要求的艺术品。
因此,我的最主要的建议是国内的药物化学专家们能更多地和生物学、医学领域的专家合作,尤其是希望他们能更多地重视结构药理学这个领域的发展!
原始出处:To C, Jang J, Chen T, et al. Single and dual targeting of mutant EGFR with an allosteric inhibitor. Cancer Discov. 2019 May 15.
小提示:本篇资讯需要登录阅读,点击跳转登录
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#抑制剂#
32
#Dis#
32
#GFR#
24
#ISC#
24