一个高速发展而充满了“重磅炸弹”的领域
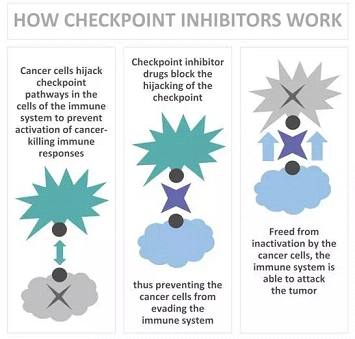
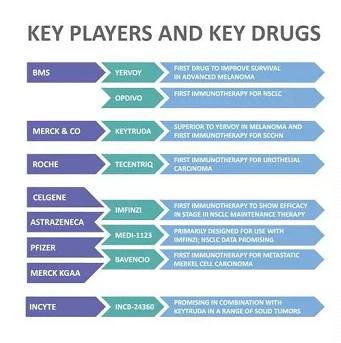
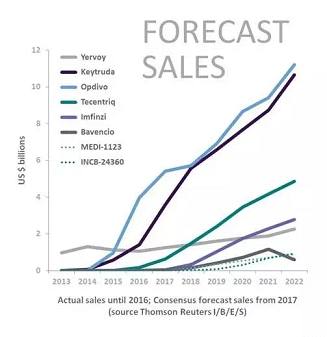
免疫检查点抑制剂疗法旨在阻断癌细胞逃避免疫系统破坏的通路,随着新产品不断地进入开发和现有药品新适应症的获批上市,该领域的进展持续高速推进,其中最成功的产品通常在获批后很短的时间内就能达到“重磅炸弹”级别。Opdivo 和 Keytruda 于2014年获批上市,2016年就成为了“重磅炸弹”(年销售额突破10亿美元),Tecentriq 于2016年获批,有望在2018年冲击“重磅炸弹”的门槛,而2017年获批上市的Imfinzi 和 Bavencio,预计分别在2019年和2021年可成为“重磅炸弹”,我们预测下表中8个免疫检查点抑制剂在2022年的销售总额最高可达340亿美元。
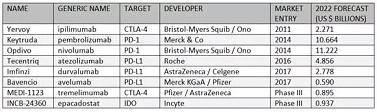
2022年的销售额预测值超过100亿美元的Keytruda 和 Opdivo,均在我们的《2015最值得关注的新药预测》报告中进行了探讨,而Imfinzi 和 Bavencio 也名列2017年最值得关注的8个新药之中。自该报告发布以来的数个月里,免疫检查点抑制剂领域又产生多个非常具有价值的进展,这足以证明该领域发展的神速。仅2017年5月,这些药物就获批了5个新的适应症,此外还有2个新适应症的上市申请获受理。以上申请的审批包括首次开创性地批准(基于肿瘤基因的特征而非肿瘤类型批准某个药物用于实体瘤治疗)和批准某种新药进入该领域。
Keytruda:首次按基因特征而不考虑肿瘤部位的适应症获批
在此开创性的批准以前,抗癌药的适应症都是基于肿瘤的所在部位,例如肺、胰腺或直肠等。2017年5月FDA首次批准一个新药用于基因类型为微卫星高度不稳定(microsatelliteinstability-high,MSI-H)或错配修复缺陷(mismatch repair deficient,dMMR)的所有实体瘤治疗,而拥有这些生物学标记的肿瘤包括直肠癌、子宫内膜癌、胰腺癌和胃肠道癌症。
Keytruda 还在不考虑PD-L1表达的条件下,获批用于非小细胞肺癌一线治疗
2015年10月,Keytruda获批用于有PD-L1生物标记的转移性非小细胞肺癌(NSCLC)治疗标志着该产品正式进军非小细胞肺癌市场,一年以后,获批拓展用于PD-L1高表达的转移性非小细胞肺癌一线治疗,2017年5月,该产品又进一步获批拓展至无需考虑PD-L1的表达,与化疗联合用于所有转移性非小细胞肺癌的一线治疗。时至今日,Keytruda是唯一一个获批的此项疗法的PD-1/PD-L1免疫检查点抑制剂。
Imfinzi、Keytruda 和 Bavencio 加入 Tecentriq 和 Opdivo 的膀胱癌市场争夺战
同样出现在2017年5月的,还包括三个免疫检查点抑制剂获批用于尿路上皮癌,加入了以前两款获批该适应症药物间的市场争夺战。Imfinzi获批用于尿路上皮癌的二线治疗,这也是该产品首次获得批准上市。Keytruda 和 Bavencio 同样是获批二线治疗,而且Keytruda 在原有的基础上获批了一线治疗。膀胱癌是美国的第五大癌症,2016年有7.7万人被新确诊为膀胱癌,而尿路上皮癌占确诊人数的90%。这些新进入该领域的产品,将与Tecentriq 争夺膀胱癌市场。而2016年5月获批的Tecentriq 是FDA 30余年来首个批准用于该类型膀胱癌治疗的药物,并且于2017年4月,Tecentriq 成为本领域首个获批一线治疗的免疫疗法。对于Opdivo,该产品也在2017年2月获批了二线疗法。
Opdivo二线治疗肝细胞癌的美国上市申请被受理
此前,Opdivo 已经有多个肿瘤适应症获批上市销售,2017年5月,Opdivo二线治疗肝细胞癌(HCC)的上市申请又被FDA受理,其审批意见有望在2017年9月揭晓。肝细胞癌是一种极为常见的癌症,全球每年超过70万人受此病困扰,是致死率第二高的癌症。此外, Opdivo 的肝细胞癌一线疗法还在开发中。
Keytruda 用于胃癌、胃食管交界处腺癌的美国上市申请获受理
Keytruda 在2017年二季度获得的巨大成就不仅是上述疗法的获批,还包括用于胃癌、胃食管交界处腺癌的上市申请获得受理,而且FDA的审批决定有望在2017年9月公开。在全球范围内,胃癌是第五大癌症,每年大约有95万人被诊断为胃癌,每年全球报告的致死人数大约72万人,是第三大癌症死因。
对于Keytruda而言,并非所有的消息都是好消息—多发性骨髓瘤出现了死亡病例
尽管 Keytruda 已获得不少令人振奋的消息,但最近并非所有的消息都令人满意。在2017年6月,在收到 Keytruda 治疗组患者死亡更多的报告后,默沙东宣布停止了两项有关多发性骨髓瘤三期临床试验的招募。其中,KEYNOTE-183是一项评估 Keytruda 联合 Pomalyst (泊马度胺) 和地塞米松三线治疗多发性骨髓瘤的临床试验,而 KEYNOTE-185 是一项评估Keytruda 联合 Revlimid (来那度胺) 和地塞米松一线治疗多发性骨髓瘤的临床试验。具体情况有待更深层次的数据统计分析公开后进一步观察。
ASCO 公开了 Opdivo 和 Yervoy 治疗间皮瘤的积极性数据
2017年6月初,Opdivo 和 Yervoy 为胸膜间皮瘤治疗带来了希望,胸膜间皮瘤是一种无法治愈的癌症,初始化疗复发率达100%,平均预后寿命只有13至15个月。在美国临床肿瘤协会(ASCO)第53届会议上公开了一项名为 MAPS2 的二期临床试数据,该数据显示二线或三线治疗胸膜间皮瘤,Opdivo 治疗组的12周疾病控制率为44%,Opdivo 联合 Yervoy 治疗组为50%,而相比之下,此前的各种治疗方案,疾病控制率均未超过30%。截止目前,该临床试验还在进行中,有望在2018年12月前完成。此外,一项名为CheckMate743,用于评估 Opdivo 联合 Yervoy 一线治疗间皮瘤的三期临床试验已经在2016年10月开启,预计在2021年8月完成。
INCB-24360 喜忧参半的临床数据在ASCO上公开
今年ASCO会议上,Incyte 公司公开了其 IDO 免疫检查点抑制剂 INCB-24360 的临床试验数据,结果为喜忧参半。尽管该产品对某些类型的实体瘤效果有限,但二线治疗非小细胞肺癌是非常有前途的。虽然在一项名为 ECHO-202 的 I/II临床试验的数据显示,INCB-24360联合Keytruda治疗乳腺癌和卵巢癌的收效甚微(目前这些适应症已经停止开发),但是非小细胞肺癌治疗的总应答率达35%,在同等条件下相比Keytruda 单药治疗有显着的改善,并且联合疗法在不考虑PD-L1表达的条件下表现出良好的疗效和耐受性。此外,该产品在黑色素瘤和肾细胞癌上也表现出了积极的疗效。
这些数据彰显了PD-1/IDO 抑制剂组合疗法取代耐受性较差的 PD-1/CTLA-4 抑制剂组合疗法的可能性,而 PD-1/CTLA-4 抑制剂是目前唯一获批的肿瘤免疫组合疗法(即 Opdivo 联合 Yervoy 用于转移性黑色素瘤治疗)。INCB-24360 联合 Keytruda 的三期临床征程于2016年由一项针对黑色素瘤、名为 ECHO-301的临床试验而开启,而且更多的三期临床试验正在计划招募中,如 INCB-24360 联合 Keytruda 用于非小细胞肺癌的一线治疗,膀胱癌的一线、二线治疗,肾细胞癌的一线治疗和头颈部鳞状细胞癌癌的一线治疗,以及联合 Opdivo 用于非小细胞肺癌、头颈癌的一线治疗等。
小结
免疫检查点抑制剂领域,乃至整个肿瘤免疫治疗领域的进展都是极为神速、引人瞩目的,而且这些进展都具有巨大的临床和商业价值。未来几年的挑战将是确定最佳的免疫疗法类型和组合,以及找到最佳的目标人群接受它。Keytruda 开创性地基于生物标记物类型而非肿瘤部位的获批,意味着它朝此方向已经迈出坚定的一步,以后其它基于生物标记物类型的获批也极有可能再次出现。跟我们今天看到的一样,随着这一领域的发展与进步,肿瘤免疫治疗有望持续不断地为患者预后提供显着的改善。

小提示:本篇资讯需要登录阅读,点击跳转登录
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#抑制剂#
29
学习了,谢谢分享
92
#免疫检查点#
26
学习了谢谢分享
76
好文,值得点赞!认真学习了,把经验应用于实践,为患者解除病痛。
85