自2007年11月索拉非尼被美国食品药品监督管理局批准用于晚期肝癌治疗以来,国际上已有5个靶向药物获批肝癌适应症。随着对肝癌分子信号通路和肿瘤微环境研究的不断深入,靶向免疫治疗在晚期肝癌治疗中表现出明显优势。
免疫治疗的实现和应用,无疑是人类抗击癌症历史上十分关键的一步。其卓越的有效性和持久性,都让人对免疫疗法的未来充满期待。那么,在靶向免疫治疗时代,肝癌放疗是否会被取代?
9月27日,在全国临床肿瘤学大会(CSCO)学术年会上,来自复旦大学附属中山医院主任医师曾昭冲教授分享了题为“靶向免疫治疗时代,肝癌放疗新思考”的精彩报告。
靶向免疫治疗原发性肝癌的疗效
放疗是一种局部治疗手段,通过直接或间接地损伤 肿瘤细胞 DNA 来起到杀伤肿瘤的作用。传统上认为, 由于免疫细胞对放疗敏感,放疗具有免疫抑制性,但越来越多的证据显示,局部放疗可产生“远隔效应”,促进机体产生免疫应答,与免疫治疗联合甚至有协同作用, 成为肿瘤治疗领域中极有前景的治疗模式。
2020年我国发布的《肝癌靶向药物治疗专家共识》推荐:
1,对于不适合局部处理的局部晚期和晚期肝细胞癌,可选择索拉非尼(1级推荐,1类证据)、仑伐替尼(1级推荐,1类证据),也可考虑多纳非尼(2级推荐,1类证据,药品未上市);慎重选择阿帕替尼(3级推荐,2类证据)、安罗替尼(3级推荐,3类证据);
2,对于不适合局部处理的局部晚期和晚期HCC的二线治疗,可选瑞戈非尼(1级推荐,1类证据),也可考虑阿帕替尼(2级推荐,1类证据,未获得适应证)、卡博替尼(2级推荐,1类证据,国内未上市)、雷莫芦单抗(2级推荐,1类证据,国内未上市);慎选安罗替尼(3级推荐,3类证据)。
3,对于不适合局部处理的局部晚期和转移性HCC且肝功能 Child-Pugh A级患者,一线治疗可选择贝伐珠单抗联合阿替利珠单抗(1级推荐,1类证据);也可以谨償选择抗血管生成靶向药物(贝伐珠单抗、小分子络氨酸激酶抑制剂)联合免疫检查点抑制剂的其他组合方案(2级推荐,3类证据)。
原发性肝癌放疗的效果
自2013年到2019年美国NCCN肝胆肿瘤诊治指南均推荐,无论肿瘤位于何处都适合放疗。2018年美国NCCN肝胆肿瘤诊治指南新增推荐,放疗时使用影像引导,即IGRT。

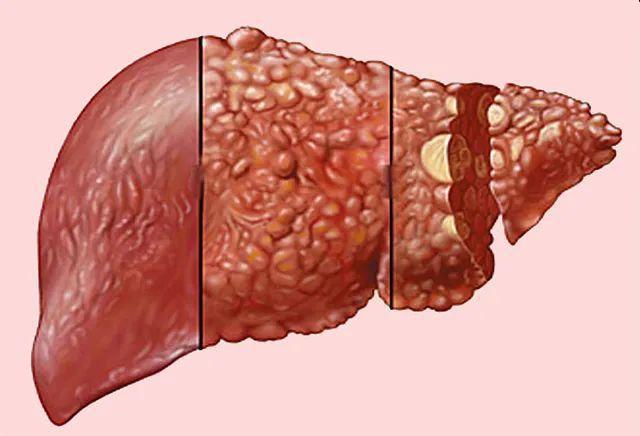
这些HCC都可以局部放疗,不应马上用靶向治疗
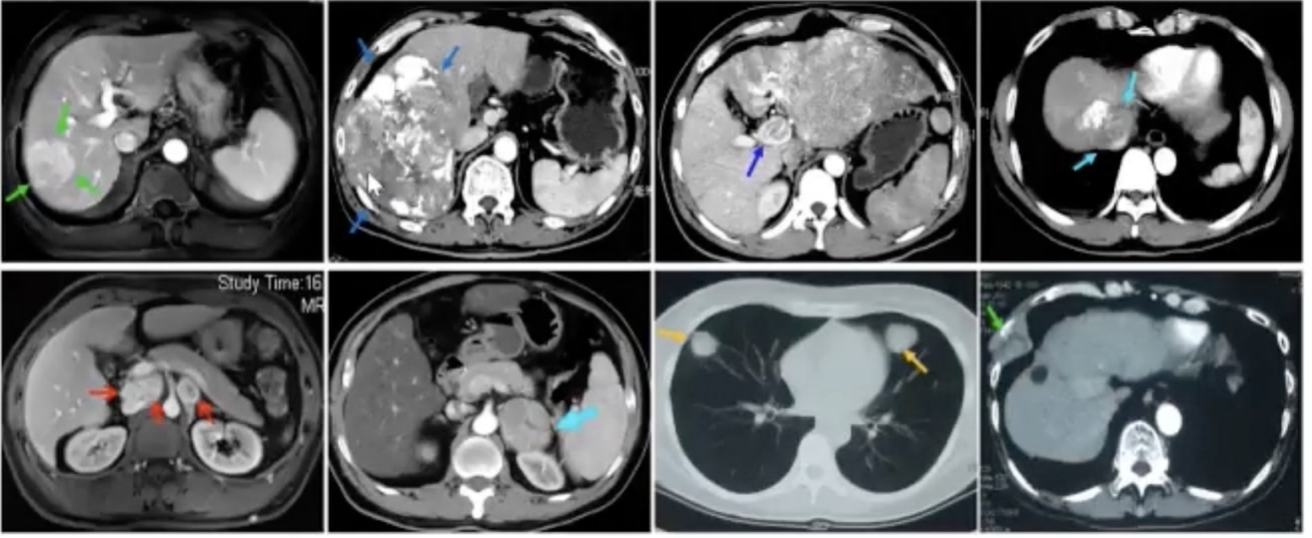
图:不同HCC影像图
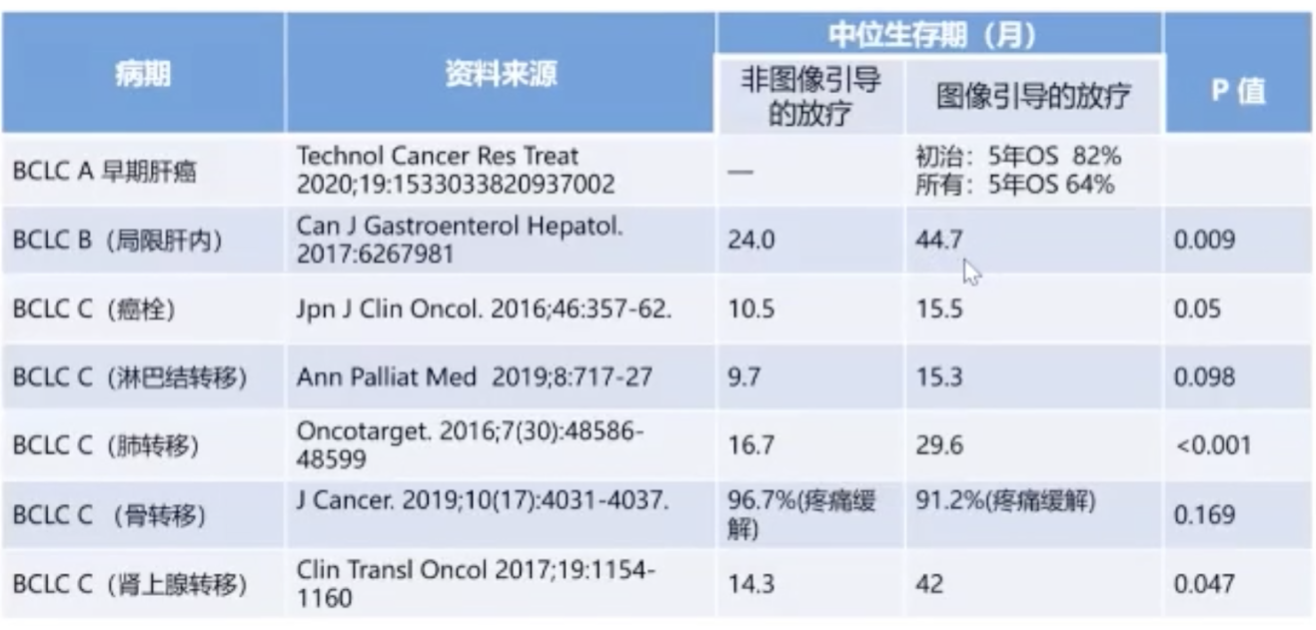
图:IGRT与非IGRT治疗不同病期原发性肝癌OS比较
放疗改变原发性肝癌免疫微环境
众所周知,肿瘤微环境是肿瘤发生、发展所处的内外环境,在肿瘤进程、免疫逃逸和治疗抵抗中发挥重要作用。有研究显示,放疗诱导PD-1和PD-L1表达,促进免疫逃避。然而,放疗激活cGAS-STING通路,促进抗肿瘤免疫。
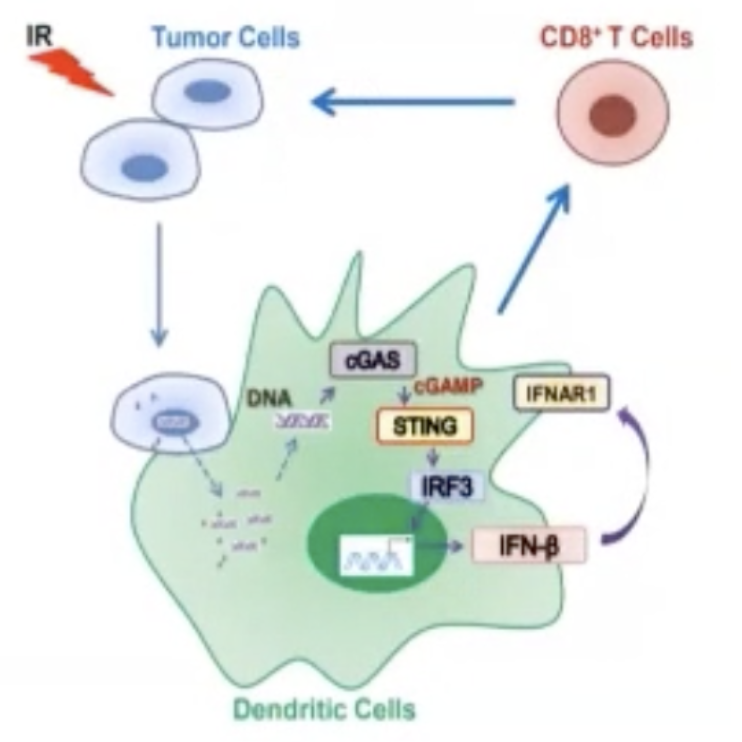
图:cGAS-STING通路
放疗剂量对远隔效应的影响
在肿瘤放疗分割剂量中,单次大剂量放射照射通过STING信号通路增加放疗后免疫效应。单次大剂量放射照射通过促进周围巨噬细胞向抑肿瘤的M1型极化,进而增加放疗后免疫效应。
肝癌细胞LM3,Huh7受不同放射剂量照射72小时后,取其上清液刺激THP-1巨噬细胞,检测巨噬细胞M1型marker表达变化。其中,单次10Gy M1型marker表达最高,说明单次10Gy照射时巨噬细胞向抑瘤的M1型极化最明显。
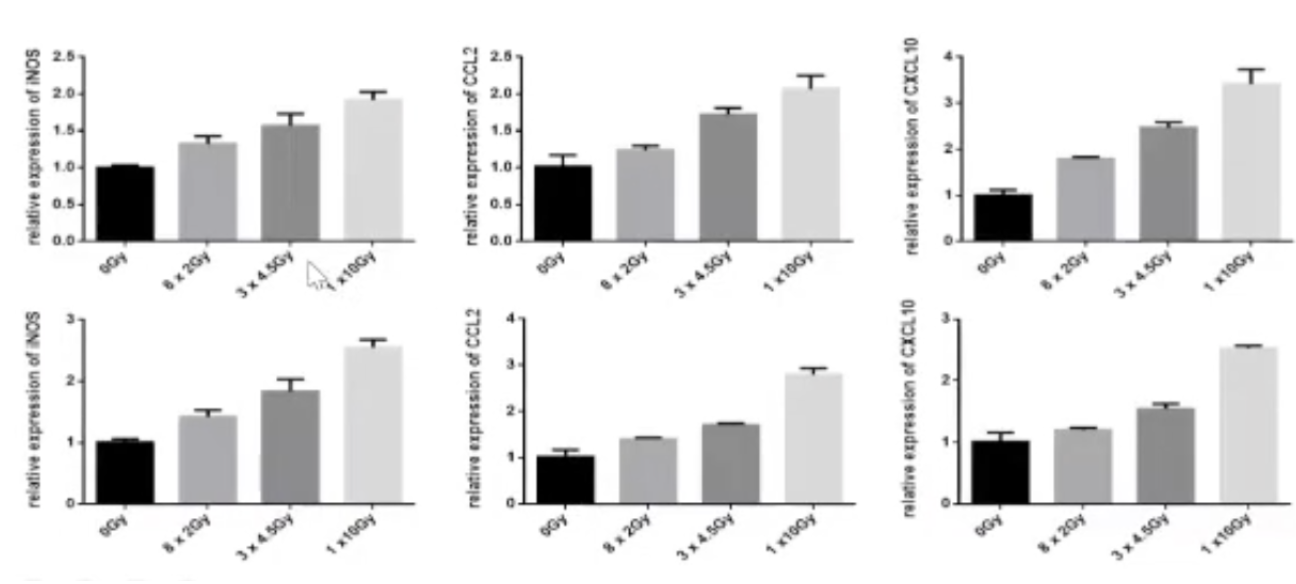
图:不同放射分割方法影响巨噬细胞极化表型
当前,放疗联合免疫治疗的这种治疗模式尚处于起 步阶段,对于放疗方案、免疫治疗的剂量、介入时机、 药物种类以及目标人群尚未达成一致。放疗联合免疫治疗在肝癌治疗中的价值值得进一步地探究。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









学习了
55
学习学习
65
学习了。感谢分享
62