再延期!“复必泰”临床试验延长至10月30日
2022-05-08 健识局 健识局
5月5日,有媒体报道称,复星医药从BioNTech公司引进的mRNA新冠疫苗“复必泰”在中国的Ⅱ期临床试验结束日期将延长至今年10月30日。
5月5日,有媒体报道称,复星医药从BioNTech公司引进的mRNA新冠疫苗“复必泰”在中国的Ⅱ期临床试验结束日期将延长至今年10月30日。
全球权威的临床试验登记网站ClinicalTrials.gov看到:5月3日时,“复必泰”中国Ⅱ期临床试验的预计完成日期已修改为今年10月30日。
ClinicalTrial网站显示,这项临床试验由BioNTech公司登记,2020年12月启动,原计划于2021年12月结束,后延期至今年4月30日,如今再次延后。
“复必泰”的Ⅱ期临床主要是研究这款疫苗在中国健康人群中的安全性。试验总共入组950人,每个参与者的试验持续13个月左右。去年7月,复星医药董事长吴以芳曾表示,疫苗的“审定工作基本完成,正在加紧进行行政审批”。这一度被业内视为复必泰即将上市的信号。
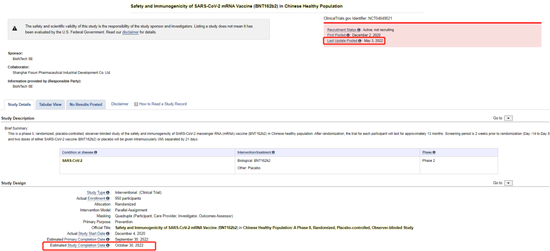
图源:ClinicalTrials.gov网站
然而,一再传出的临床延期消息,让“复必泰”在大陆地区上市蒙上阴影。今年3月,吴以芳再度回应复必泰的上市进展时,态度变得保守了许多:“还在审批,没有更多的消息。”
复星医药2021年年报显示,这款疫苗在港澳台三地的累计供应量已超2000万剂,销售额达10亿元。
相关报道:尴尬的中国mRNA疫苗,还有好日子吗?
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








