Cell discovery:北京大学杭婧/乔杰/魏瑗揭示金属蛋白酶妊娠相关血浆蛋白A的结构及调节机制
2022-12-25 iNature iNature 发表于上海
金属蛋白酶妊娠相关血浆蛋白A(PAPP-A)最初作为胎盘滋养层分泌的蛋白质在孕妇循环中发现。
金属蛋白酶妊娠相关血浆蛋白A(PAPP-A)最初作为胎盘滋养层分泌的蛋白质在孕妇循环中发现。虽然妊娠期绝大多数循环PAPP-A由于嗜酸性粒细胞主要碱性蛋白(proMBP)的共价抑制而蛋白水解无活性,但 PAPP-A 的活性也可以被另一种特征较少的调节剂STC2共价抑制。然而,PAPP-A蛋白水解的结构基础以及这两种调节剂之间的机理差异知之甚少。
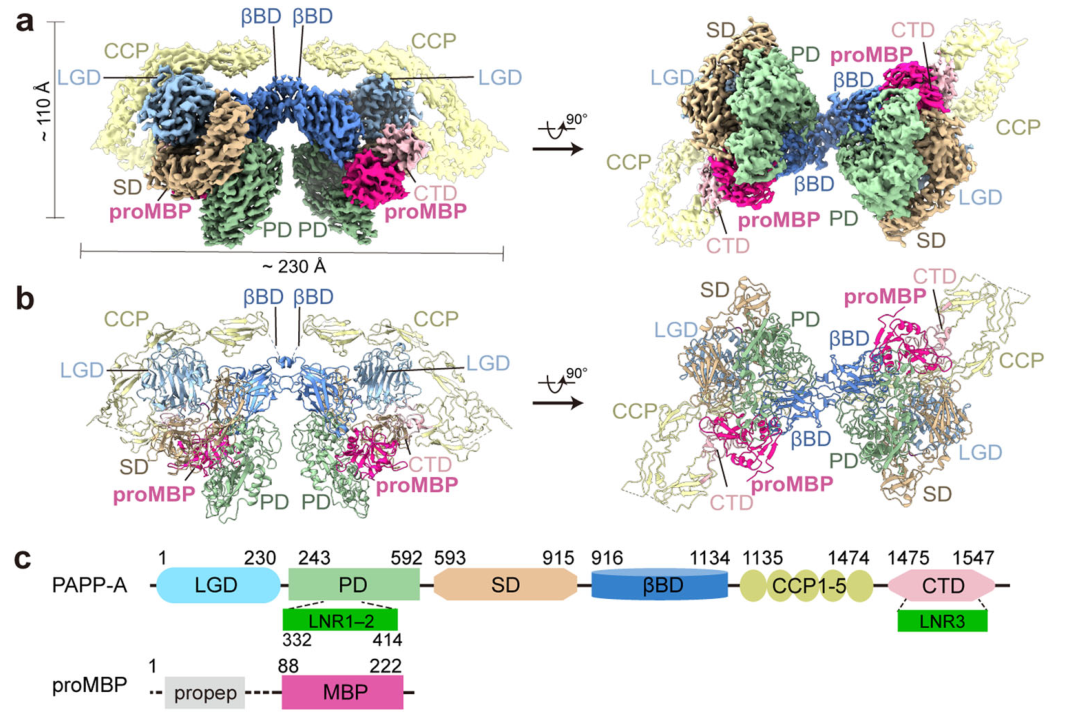
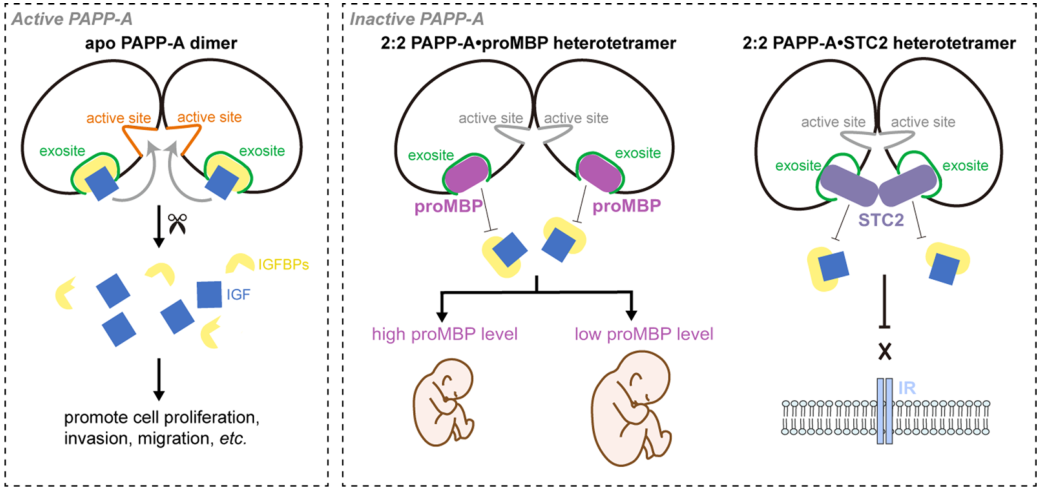
2022年12月22日,北京大学杭婧,乔杰及魏瑗共同通讯在Cell Discovery(IF=38)在线发表题为“Structural insights into the covalent regulation of PAPP-A activity by proMBP and STC2”的研究论文,该研究进行了ProMBP和STC2共价调控PAPP-A活性的结构研究。该研究报道了内源性纯化的PAPP-A与proMBP或STC2复合物的两个冷冻电镜结构。这两种调制剂与PAPP-A形成2:2异四聚体,并与催化裂口远端的PAPP-A的多个结构域建立广泛的相互作用。
这种外位结合特性导致空间位阻,从而阻止IGFBPs的结合和裂解,而含有裂解位点的IGFBP连接子区域衍生肽对调制剂处理不再敏感。对proMBP介导的PAPP-A在选择性宫内生长限制(sIUGR)妊娠中的调节功能研究表明,PAPP-A和proMBP协同调节滋养层外侵和随后的胎儿生长。总之,该研究工作揭示了一种新的共价外位竞争抑制机制及其对胎盘功能的调节作用。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言