北京开展医疗器械注册人试点,京津冀区域企业可被委托生产
2019-02-24 佚名 医谷综合报道
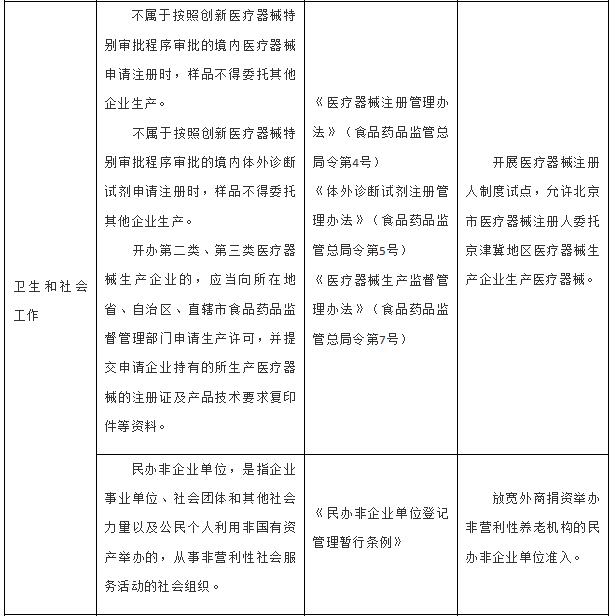
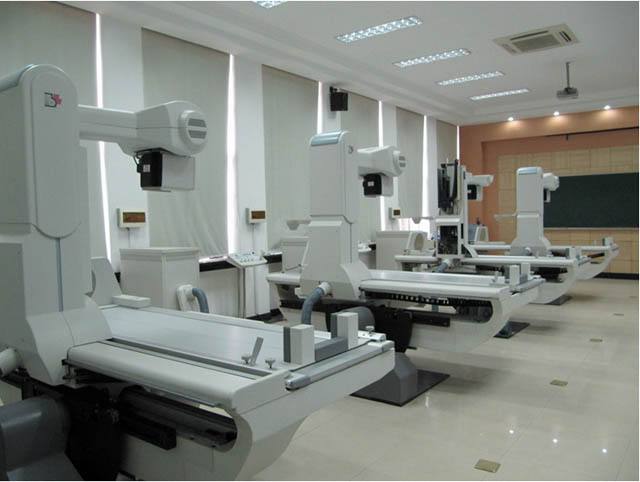
2月22日,中国政府网发布《国务院关于全面推进北京市服务业扩大开放综合试点工作方案的批复》,方案显示:探索京津冀产业链引资合作模式,建立境外投资合作风险预警信息共享机制。开展医疗器械注册人制度试点,允许北京市医疗器械注册人委托京津冀地区医疗器械生产企业生产医疗器械,助推“注册+生产”跨区域产业链发展。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#试点#
0
#京津冀#
35
#注册人#
40
#企业#
0
#生产#
24
#注册#
21