Science封面:太精彩了!来看T细胞与癌细胞的贴身攻防肉搏战!科学家用电镜记录了T细胞抗癌大战最隐秘的细节
2022-04-24 奇点网 奇点网
感谢《科学》,咱们这周又有高清大片儿看了!
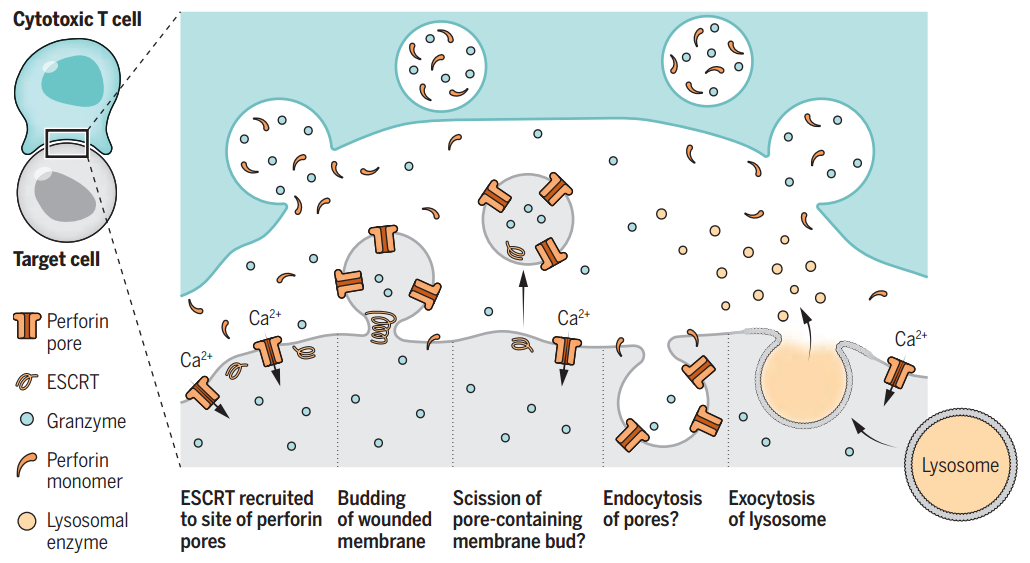
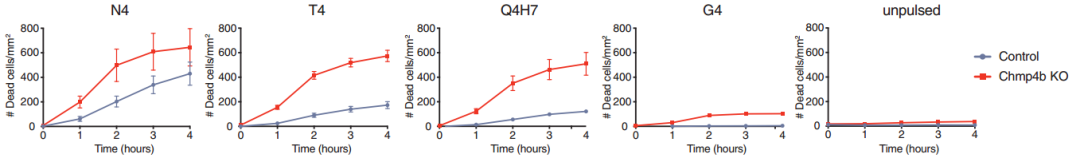
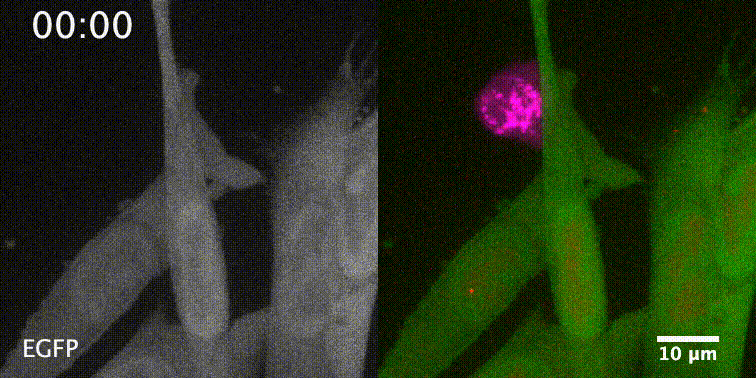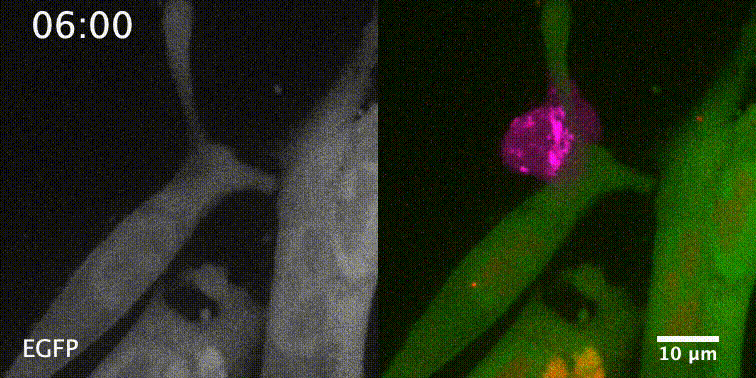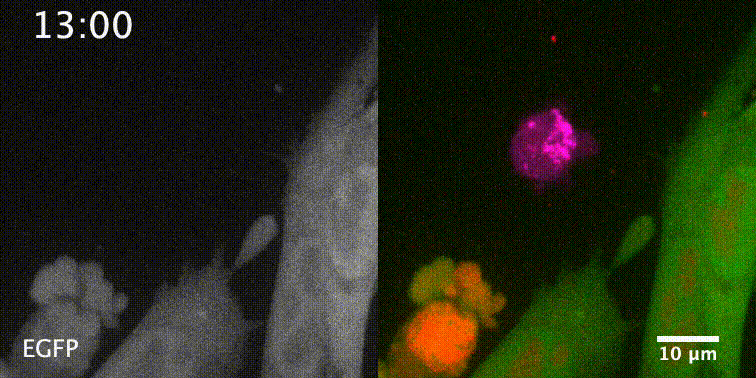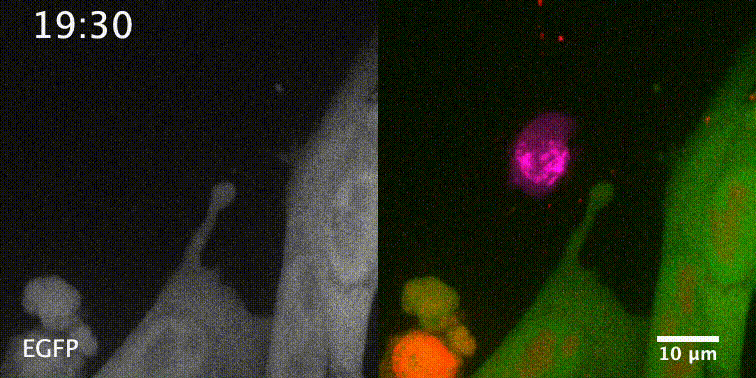
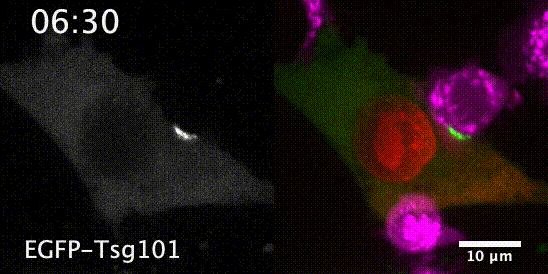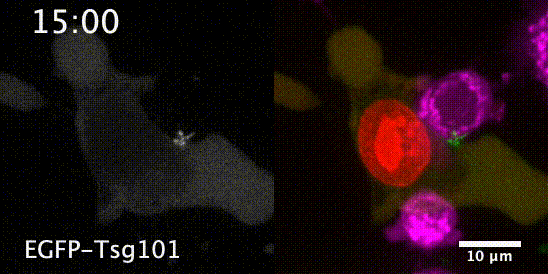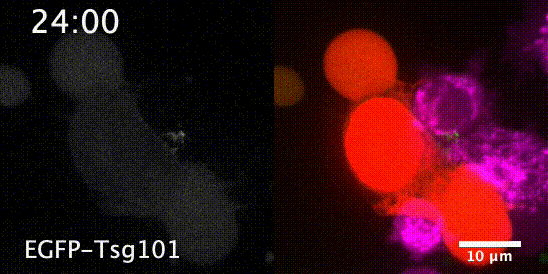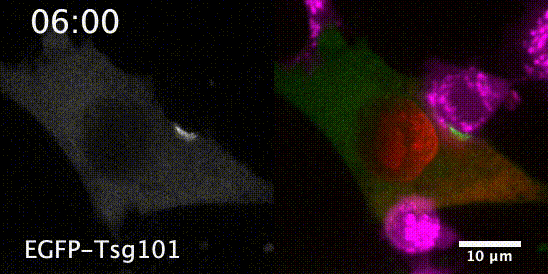
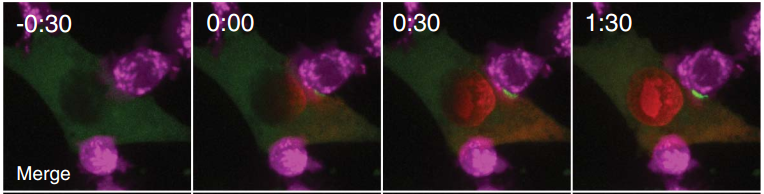
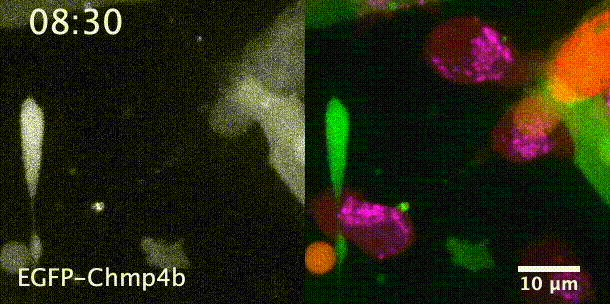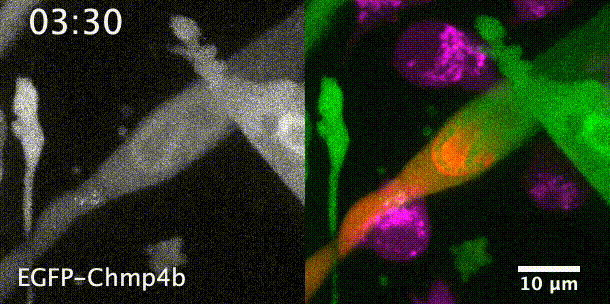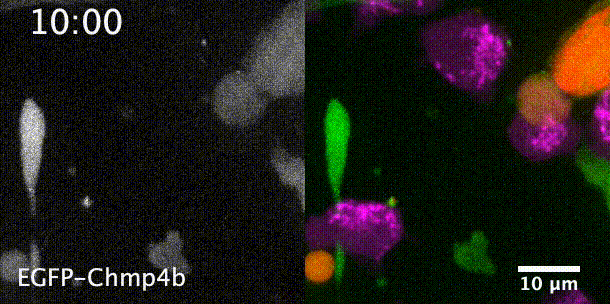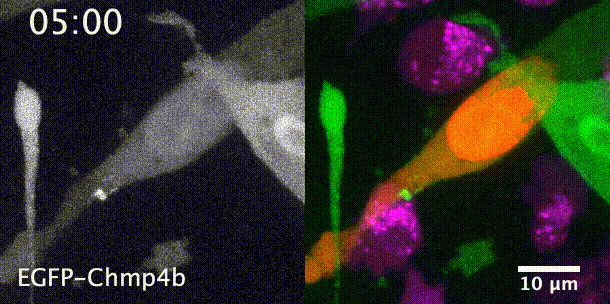
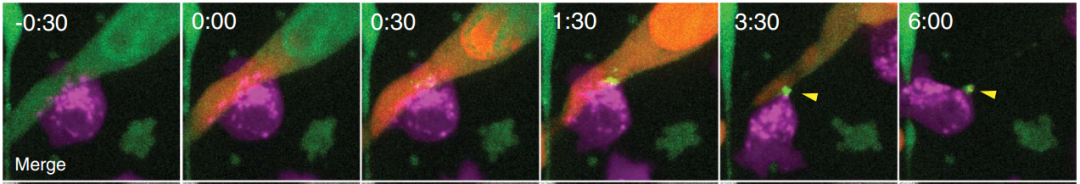
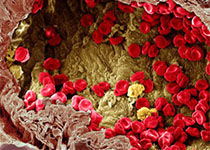
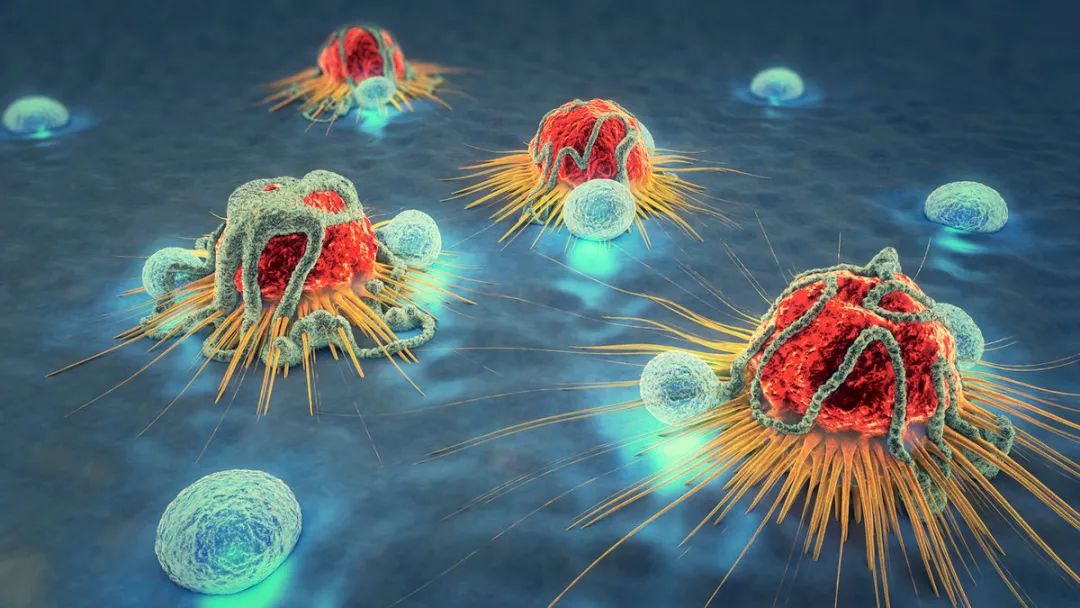
先来一个动图饱饱眼福~ 这是什么啊,这是T细胞抗癌前线发来的第一手现场资料啊~T细胞一个贴身爆破,癌细胞瞬间死翘翘~死亡贴贴属实了。 T细胞杀伤癌细胞,靠的是“近身投毒”。T细胞会紧贴癌细胞,释放穿孔素(perforin),在癌细胞的细胞膜上“开洞”,随后把颗粒酶(granzyme)送进癌细胞体内,实现瞬间爆破。 当然,癌细胞也不是全然被动等死,本周发表在《科学》杂志上的一项新研究,就利用先进的低温成像技术和聚焦离子束扫描电子显微镜(FIB-SEM),在8nm分辨率下重现了这场抗癌大战最细微的战场细节,以及癌细胞的微弱反抗[1]。这篇论文也是本周《科学》的封面研究,通讯作者是来自基因泰克的Ira Mellman和Alex T. Ritter。 癌细胞它咋反抗呢?用一个缺啥补啥的思路,T细胞给细胞膜开洞了,是不是可以趁着还没被颗粒酶弄死之前,先把洞补上再说呢? 别说,这招还真有基础。 有那么一种蛋白,叫做转运所需的内体分选复合体(ESCRT),它就参与细胞膜的重塑和损伤修复,之前有研究发现ESCRT可以修复由细菌致孔毒素、机械损伤和激光导致的质膜上的小孔[2,3]。 嗯,我想此时大家应该意识到这个研究就是为了验证ESCRT也参与癌细胞修复由T细胞穿孔素造成的膜损伤,而且应该是验证成功了…… 所以咱们也不多说废话了,让我来直接给大家说明一下这个好玩的机制。 先来看图。当穿孔素在癌细胞表面造成穿孔(perforin pore),ESCRT就会聚集到穿孔的部位。 在ESCRT的作用下,已经受损穿孔的细胞膜形成出芽,然后“啵儿”的一下掉了(这步存疑)!这样破掉的膜就么得了,咱们又是一个好细胞了。 不过这项研究只是观察到了一些现象,不能说把整个过程都板上钉钉。结合过去的研究结果,基本是这样没跑儿了,研究中也观察到敲除ESCRT后癌细胞对穿孔素和颗粒酶更敏感了。 敲除ESCRT后癌细胞对穿孔素/颗粒酶杀伤更敏感 另外,ESCRT也不会是癌细胞反抗的唯一手段,研究者认为癌细胞也可能会通过内吞掉穿孔部分膜、以及分泌溶酶体的方式来搞修补工程。这些就需要进一步的研究了。 接下来就全是看电影了~ 下面这张图中洋红色的就是T细胞,灰/绿色是癌细胞,明亮的橙红色是一种高浓度染料碘化丙啶(PI),它能透过膜上穿孔迅速扩散,并结合细胞质和细胞核内的核酸。 那么ESCRT在哪呢? 看这里~有没有看到T细胞和癌细胞之间出现了一点明亮的绿色?那就是被荧光蛋白标记的ESCRT了。在碘化丙啶流入后的30秒到60秒内,ESCRT到达了穿孔现场。 这里还有分解图。 研究者们还录到了ESCRT黏在T细胞上的镜头。 研究者猜测,这应该是含有ESCRT的脱落下来的膜碎片,因为里面含有T细胞受体的配体,所以就黏上T细胞了。 最厉害的是,为了搞懂T细胞和癌细胞之间到底发生了什么,研究者们还动用了低温荧光成像,固定住双方交战的瞬间,并用电镜重建3D模型。 来看看这个精美的细节。 连细胞亚结构都能一一还原。 参考资料: [1]https://www.science.org/doi/10.1126/science.abl3855 [2]A. J. Jimenez, P. Maiuri, J. Lafaurie-Janvore, S. Divoux, M. Piel, F. Perez, ESCRT machinery is required for plasma membrane repair. Science343, 1247136 (2014). [3]L. L. Scheffer, S. C. Sreetama, N. Sharma, S. Medikayala, K. J. Brown, A. Defour, J. K. Jaiswal, Mechanism of Ca2+-triggered ESCRT assembly and regulation of cell membrane repair. Nat. Commun.5, 5646 (2014).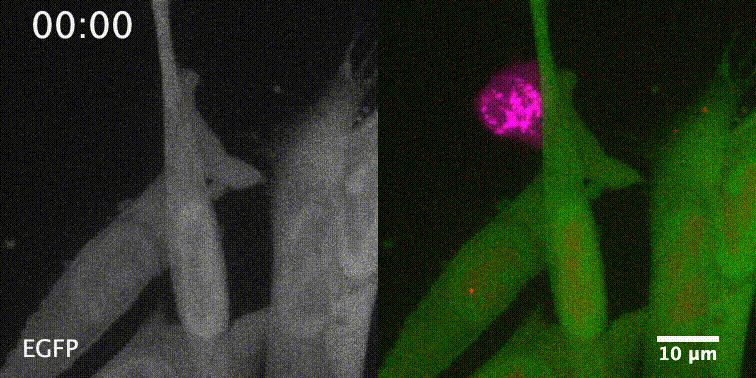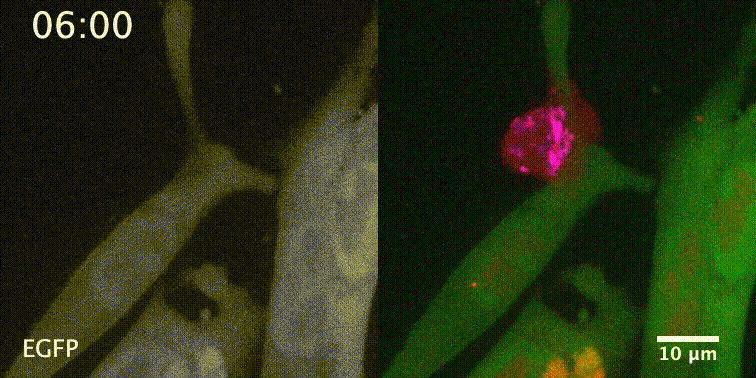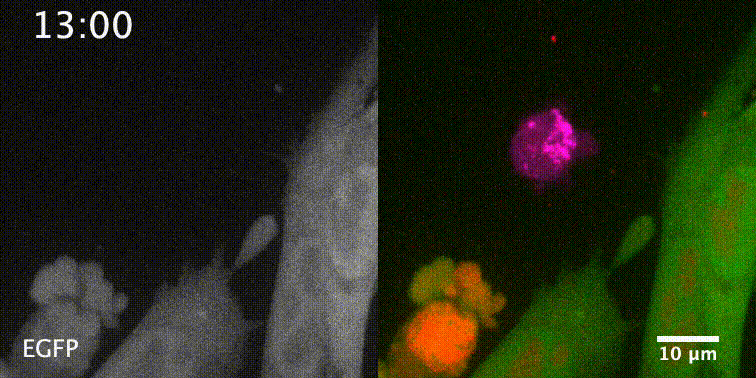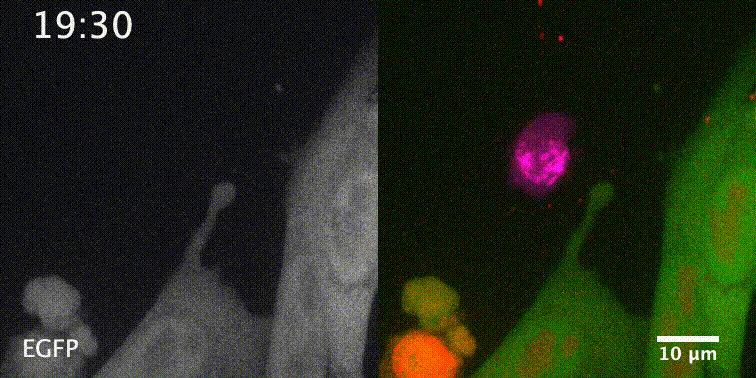




本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#癌细胞#
69
#SCIE#
46