临床研究|不同评分模型对肝硬化患者经颈静脉肝内门体分流术后生存的预测价值
2023-09-07 临床肝胆病杂志 网络 发表于上海
本研究通过分析我国西南地区多家医院近年来接受TIPS治疗的肝硬化患者临床及随访资料,以期为临床提供有益参考。
经颈静脉肝内门体分流术(TIPS)是治疗肝硬化门静脉高压相关并发症的重要手段之一,目前已被多部指南[1-2]推荐用于肝硬化食管胃底静脉破裂急性出血的控制、再出血的预防以及顽固性胸腹水的治疗。相较于外科分流术或断流术,TIPS具有创伤性小、安全性高、适用性广、疗效确切等优点。然而,临床上仍有部分患者术后因肝衰竭、顽固性肝性脑病、再出血等各种原因死亡[3],因此准确的评估预测TIPS术后患者的生存结局对临床患者术前筛选及术后随访管理具有重要意义。
目前临床上已有多种肝脏功能评分模型用于肝硬化患者预后评估,其中包括1973年由Child、Turcotte创建,并被Pugh进一步改良后形成的Child-Pugh评分[4];2001年Malinchoc等[5]提出的终末期肝病(MELD)评分;2006年Biggins等[6]在MELD评分基础上联合血清钠提出了MELD-Na评分;2015年,欧洲肝病学会-慢性肝衰竭联盟(EASL-CLIF)[7]发布了慢性肝衰竭联盟-急性失代偿评分(CLIF-C AD),该评分旨在预测失代偿性肝硬化患者的3个月病死率;2021年Bettinger等[8]基于胆红素、肌酐、年龄及Alb构建新型评分模型(FIPS)预测TIPS患者半年内生存结局。尽管目前对Child-Pugh评分、MELD评分、MELD-Na评分以及CLIF-C AD评分之间预测TIPS患者临床结局价值进行比较的研究已有报道,但由于手术技术的革新及指南意见的更新[9],TIPS治疗适应证相比以往有所拓展,治疗人群基线特征出现了新变化,加上近两年FIPS评分的提出,目前尚无相关研究采用上述几种评分模型对TIPS术后患者生存预测进行比较。此外,既往研究主要评估多种评分模型对术后短期生存的预测价值,而对术后中长期生存预测价值的评估尚未见报道。
为此,本研究通过分析我国西南地区多家医院近年来接受TIPS治疗的肝硬化患者临床及随访资料,比较Child-Pugh评分、MELD评分、MELD-Na评分、CLIF-C AD评分及FIPS评分对TIPS术后患者的中长期生存预测价值,以期为临床提供有益参考。
1资料与方法
1.1 研究对象
回顾性分析2014年1月—2021年2月于陆军军医大学陆军特色医学中心(大坪医院)、重庆医科大学第三附属医院、川北医学院附属南充市中心医院、重庆大学附属涪陵医院、重庆大学附属三峡医院、四川省乐山市人民医院、重庆大学附属黔江医院、重庆市第九人民医院行TIPS治疗的447例患者的病历资料。纳入标准:(1)肝硬化行TIPS治疗患者;(2)年龄18岁~80岁,性别不限;排除标准:(1)合并肝癌及其他恶性肿瘤;(2)非首次TIPS或手术失败;(3)非肝硬化或严重肝衰竭;(4)术后1年内肝移植或失访;(5)合并严重心肺等大器官疾病;(6)精神疾病;(7)研究者认为不适合纳入的其他情况。
1.2 数据收集
收集临床基线资料与随访资料,其中临床基线资料包括患者性别、年龄、BMI、肝硬化病因、肝硬化并发症(腹水、肝性脑病),以及实验室检查,包括血常规(WBC、PLT、Hb),肝肾功能及生化指标(ALT、AST、Alb、TBil、Scr、血Na+)和凝血功能(PT、INR)。随访资料通过电话和门诊进行随访,随访终点是死亡或肝移植,随访截止日期为2022年3月10日。生存时间从TIPS手术之日起计算。
1.3 各评分模型分值计算
Child-Pugh评分[4]由血清TBil、Alb、PT、腹水、肝性脑病分期求和,再进一步分级(A级4~6分,B级7~9分,C级10~15);MELD评分[5]=3.8×ln[TBil (μmol/L)÷17.1] + 11.2 × ln(INR)+9.6×ln[Scr (μmol/L)÷88.4]+6.4,并把任何小于1的实验室检查值均设定为1,以消除负值;MELD-Na评分[6]=MELD+1.59×(137-Na+), 其中血Na+浓度小于125 mmol/L与大于137 mmol/L的血清钠浓度分别设定为125 mmol/L与137 mmol/L。CLIF-C AD评分[7]=10×{[0.03×年龄(岁)]+0.66×ln[Scr(μmol/L)÷88.4]+[1.71×ln(INR)]+[0.88×ln WBC(×109/L)]-[0.05×Na(mmol/L)]+8};FIPS评分[8]=1.43×lg[TBil(μmol/L)]-88.4×1.71÷Scr(μmol/L)+0.02×年龄(岁)-0.02×Alb(g/L);其中CLIF-C AD根据是否大于35,FIPS根据是否大于-0.45,MELD根据是否大于9,MELD-Na根据是否大于15分为高危组与低危组,以进一步评估各模型对不同风险人群预后的区分度。
2结果
2.1 一般资料
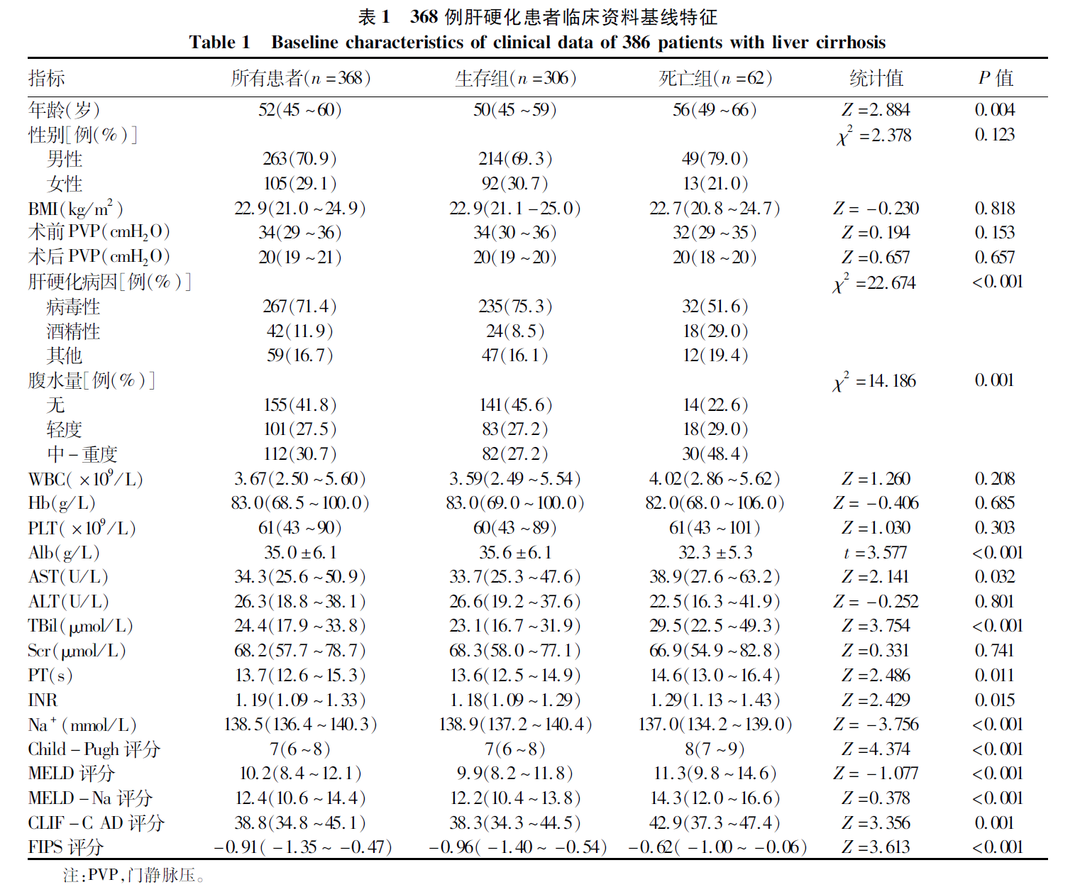
447例肝硬化患者在研究期间接受了TIPS手术治疗,79例被剔除,其中术后1年内失访25例,TIPS支架修复术或手术失败19例,合并肝癌及其他恶性肿瘤14例,其他21例,最终纳入368例患者(图1)。至随访终止,62例患者因肝脏疾病去世,其中上消化道出血20例,肝性脑病14例,原发性肝癌11例,严重感染9例,肝衰竭6例,下消化道大出血2例。生存组与死亡组患者之间年龄、肝硬化病因、腹水严重程度、Alb、AST、PT、INR、TBil、Na+、Child-Pugh评分、MELD评分、MELD-Na评分、CLIF-C AD评分及FIPS评分差异均有统计学意义(P值均<0.05)(表1)。
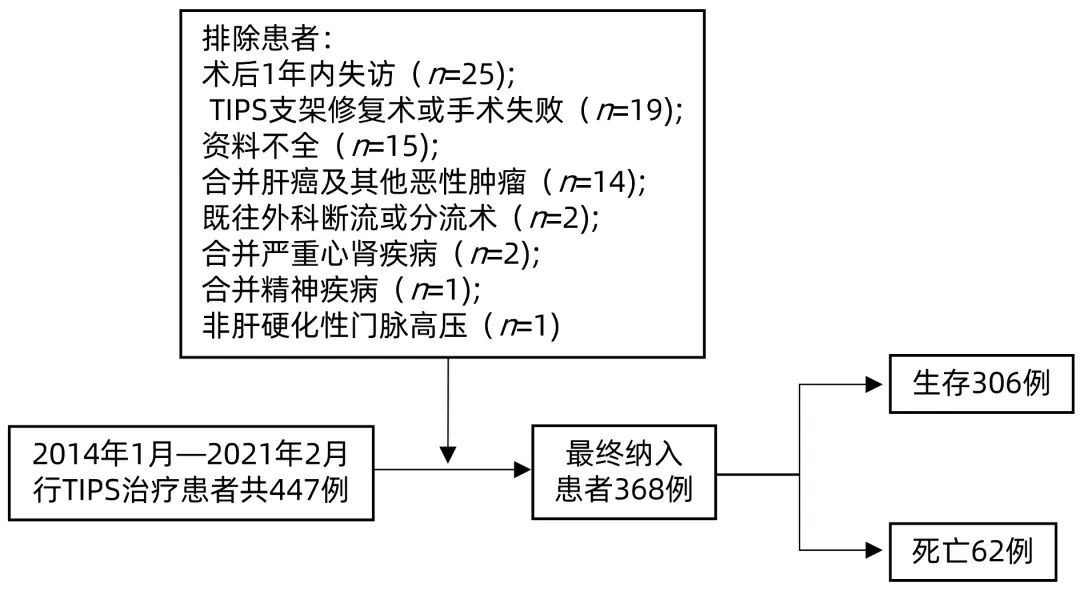
图1 患者筛选流程图
2.2 各评分模型对TIPS患者预后的影响评价
单因素Cox回归分析结果显示,年龄、肝硬化病因、腹水严重程度、Alb、PT、INR、TBil、Na+、Child-Pugh评分、MELD评分、MELD-Na评分、CLIF-C AD评分及FIPS评分差异均有统计学意义(P<0.05)(表2)。鉴于各评分模型所纳入临床指标存在交集,为避免多重共线性,分别将生存组与死亡组间存在统计学差异且未被纳入评分模型的临床指标分别纳入各评分模型行多因素Cox回归分析,进一步验证各评分模型是否为TIPS患者生存的独立危险因素。结果发现,校正年龄、肝硬化病因和Na+后,Child-Pugh评分是TIPS患者预后的独立影响因素(HR=1.51, 95%CI: 1.29~1.77, P<0.05);校正年龄、腹水、Alb和Na+后,MELD评分是TIPS患者预后的独立影响因素(HR=1.14, 95%CI: 1.05~1.24, P<0.05);校正年龄、腹水和Alb后,MELD-Na评分是TIPS患者预后的独立影响因素(HR=1.14, 95%CI: 1.06~1.20, P<0.05);校正肝硬化病因、腹水、Alb和血清TBil后,CLIF-C AD评分是TIPS患者预后的独立影响因素(HR=1.04, 95%CI: 1.01~1.10, P<0.05);校正肝硬化病因、腹水、和Na+后,FIPS评分是TIPS患者预后的独立影响因素(HR=1.79, 95%CI: 1.24~2.56, P<0.05)(图2)。
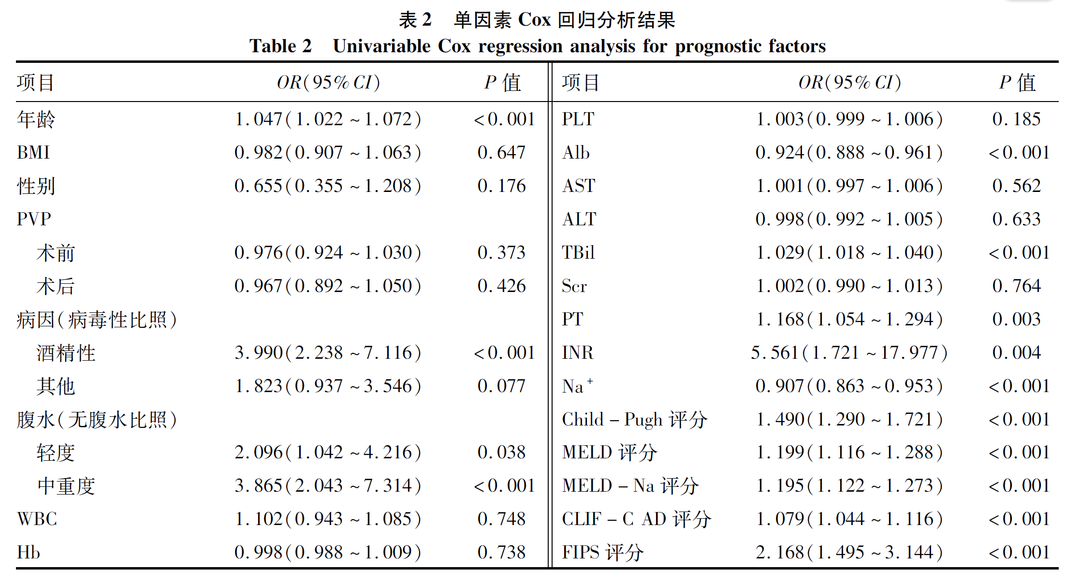
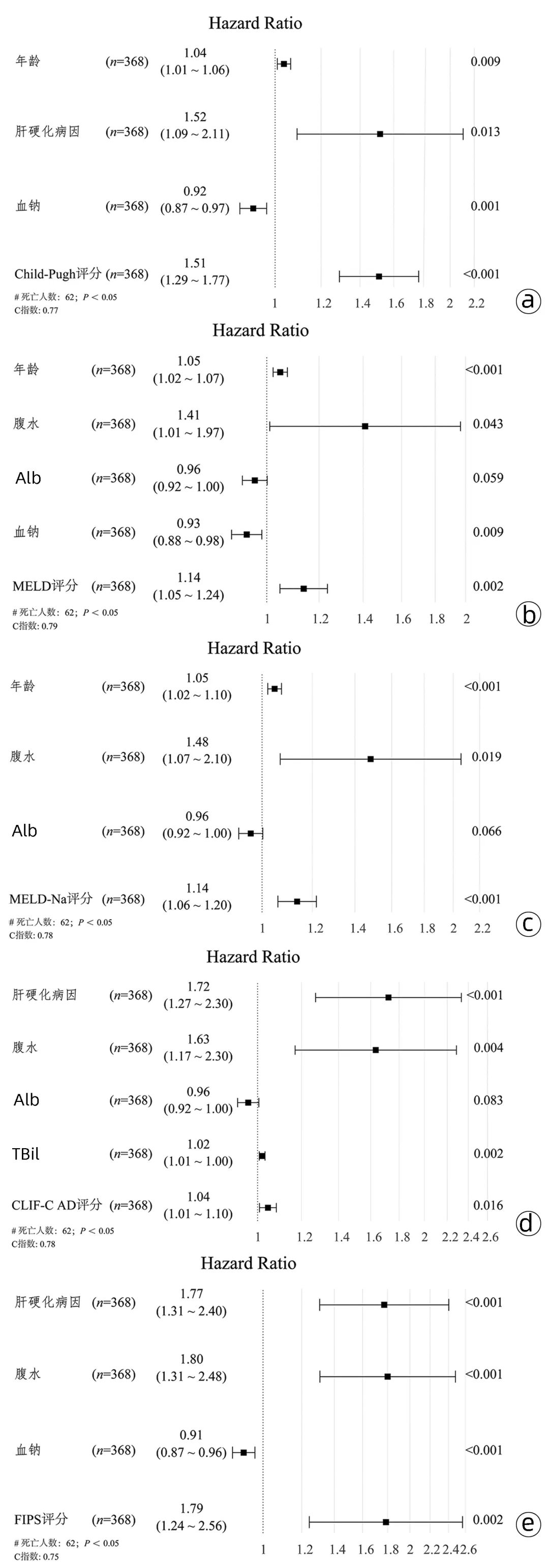
图2 各评分模型多因素Cox回归分析森林图
注:a, 校正年龄、肝硬化病因和Na+后,Child-Pugh评分是TIPS患者预后的独立影响因素;b, 校正年龄、腹水、Alb和Na+后,MELD评分是TIPS患者预后的独立影响因素;c, 校正年龄、腹水和Alb后,MELD-Na评分是TIPS患者预后的独立影响因素;d, 校正肝硬化病因、腹水、Alb和TBil后,CLIF-C AD评分是TIPS患者预后的独立影响因素;e, 校正肝硬化病因、腹水、和Na+后,FIPS评分是TIPS患者预后的独立影响因素。
2.3 各评分模型对TIPS患者死亡风险的区分能力
生存分析显示,Child-PughA与B、C级,MELD低危组(≤9)与高危组(>9),MELD-Na低危组(≤15)与高危组(>15),CLIF-C AD低危组(≤35)与高危组(>35)以及FIPS低危组(≤-0.45)与高危组(>-0.45),各组之间患者生存率存在统计学差异(P值均<0.01),提示五种评分模型均能有效对TIPS患者预后进行风险分层(图3)。
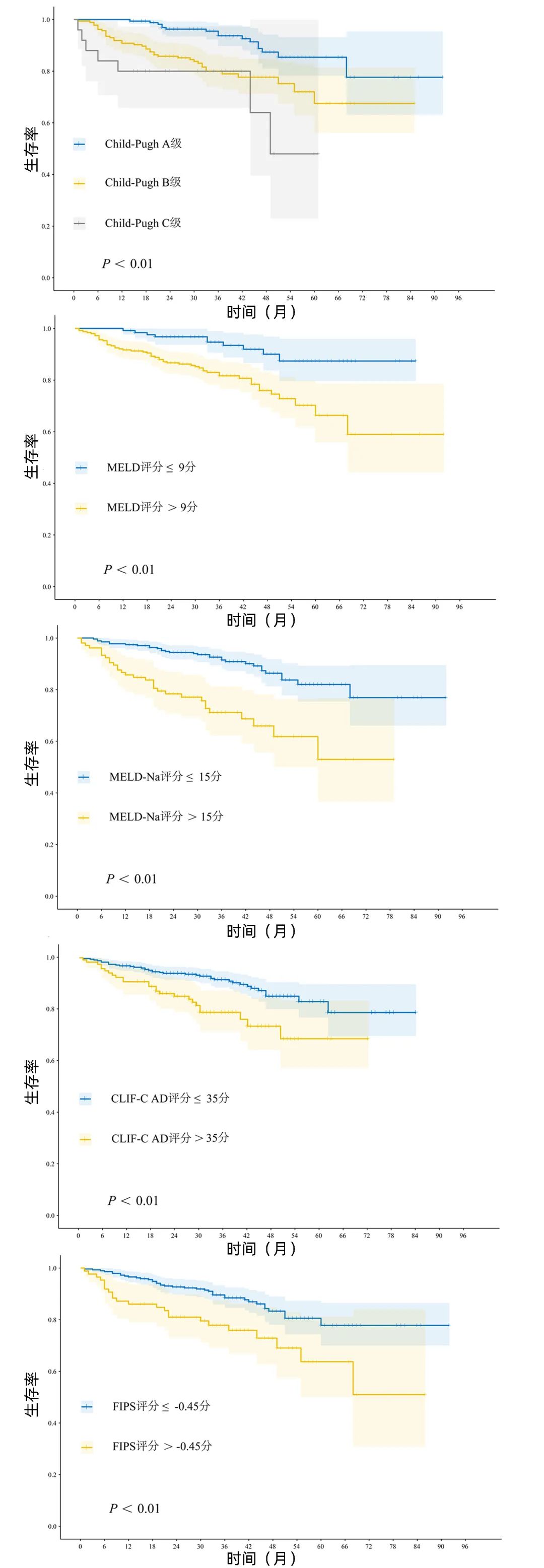
图3 各评分模型内不同风险亚组患者生存曲线
2.4 五种评分模型生存预测能力比较
五种模型均有较好的区分能力,C指数均大于0.6。Child-Pugh评分对术后生存预测能力较高,而FIPS评分预测能力最差,此外,随时间延长,各评分预测能力均减弱(图4a)。决策曲线显示,Child-Pugh评分及MELD-Na评分表现良好(图4b)。为进一步检验各评分模型预测能力,选取术后1年、3年作为观察点,结果显示,Child-Pugh(AUC=0.832)能更好的预测术后1年生存率,然后依次分别为MELD-Na(AUC= 0.807),CLIF-C AD(AUC=0.747),MELD(AUC=0.746)和FIPS(AUC=0.745)。而在预测3年生存率方面,MELD-Na(AUC=0.726)具有更好的预测能力,其次是Child-Pugh(AUC=0.710),MELD(AUC=0.705)和CLIF-C AD(AUC=0.705),然后是FIPS(AUC=0.658)(图4c、d)。
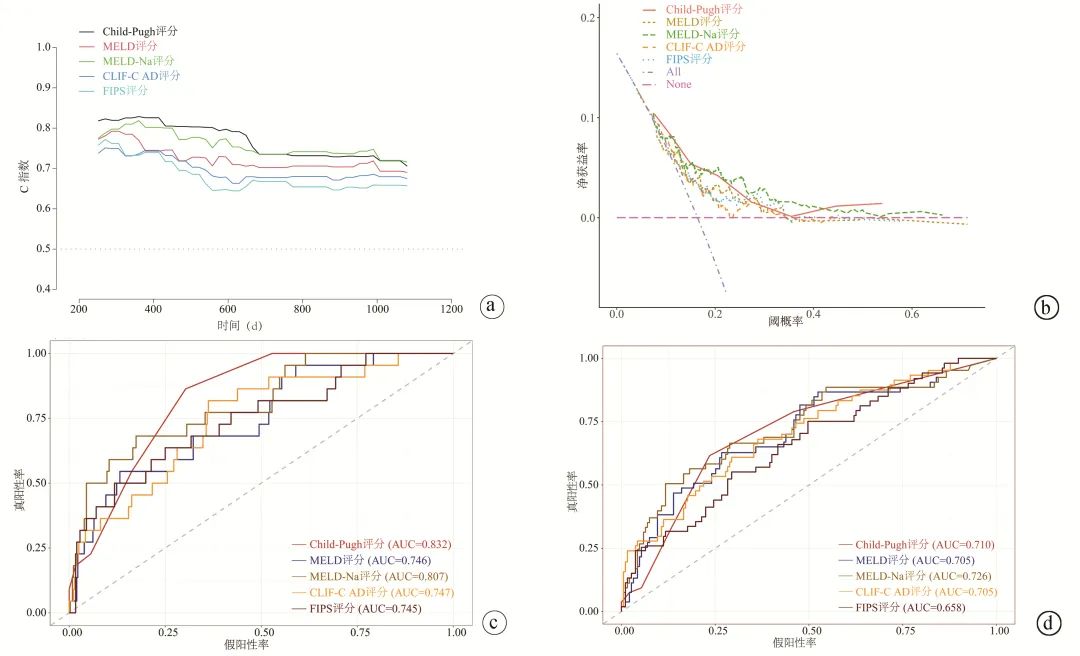
图4 各评分模型预测能力的比较
注:a, C指数;b, 决策曲线;c, 术后1年ROC曲线;d, 术后3年ROC曲线。
3讨论
TIPS自1982年开始应用于临床[10],历经数十年的发展,现已成为治疗肝硬化门静脉高压症的重要手段。患者肝脏功能与TIPS术预后密切相关。为了能够准确预测TIPS术后患者生存结局,目前已应用了一系列肝脏评分模型,如传统的CTP评分及肌酐矫正后CTP(CrCTP-Ⅰ, CrCTP-Ⅱ)、各种改良后MELD评分(MELD-Na、MESO、iMELD等)、APACHEⅡ评分以及近年来新开发的ALBI评分、FIPS评分等[6, 11-13]。既往一些研究已对CTP、MELD、FIPS及APACHEⅡ评分模型的预测能力分别进行对比研究。然而,目前尚未见用传统肝功能Child-Pugh评分、MELD评分、MELD-Na与近年来新开发的CLIF-C AD评分、FIPS评分对TIPS患者生存预测价值相对比的研究。
本研究结果显示,TIPS术后生存组患者年龄低于死亡组,Alb、Na+均高于死亡组,而酒精性肝硬化患者比例、AST、PT、INR、TBil、腹水严重程度及五种模型评分均低于死亡组,差异均有统计学意义(P值均<0.05)。这与之前相关研究[14-18]报道年龄、酒精性肝硬化、肝功能评分是TIPS术后危险因素研究结果一致。分别校正生存组与死亡组患者间存在统计学差异且未被纳入各评分模型的混杂变量后发现,五种评分模型均是TIPS患者预后的独立影响因素。针对人群风险分层,通过Kaplan-Meier方法绘制生存曲线,并采用Log-rank检验进行比较,与既往研究结果相同[19],本研究同样显示,五种评分模型均具有较好的人群风险区分能力。比较每个时间点不同评分模型C指数发现,Child-Pugh评分对术后生存预测能力较高,其次为MELD-Na评分、MELD评分和CLIF-C AD评分,而FIPS评分预测能力相对较差;但随患者生存时间延长,Child-Pugh评分与FIPS评分预测能力均降低,而MELD评分和CLIF-C AD评分预测能力相对稳健。通过决策曲线也发现Child-Pugh评分和MELD-Na评分均表现良好。在1年、3年生存率预测的对比研究发现,Child-Pugh评分预测1年生存率优于另外四种评分;但在3年生存率预测方面,Child-Pugh评分预测能力下降,而MELD评分和CLIF-C AD评分预测能力相对稳健。在两个横断面时间点上,FIPS评分预测能力均不令人满意。
本研究显示,MELD评分在生存组与死亡组之间有统计学差异(P<0.05)。虽然Parvinian等[14]曾报道MELD评分不是TIPS患者预后危险因素,但本研究与既往大多研究[20-21]结果一致。另外,在模型预测能力评估中,本研究发现MELD评分与CLIF-C AD评分预测能力相当,但与Bettinger等[8]研究结果不同,本研究未发现FIPS评分对TIPS术后1年生存率预测能力优于Child-Pugh评分,究其原因可能为:一是纳入人群不同,本研究纳入患者主要是以乙型肝炎肝硬化为主体,而以上五种评分模型主要基于西方酒精性肝硬化人群建立,不同病因的肝硬化患者肝脏损伤特点及发生发展规律不尽一致,这可以导致研究结论不完全相同;二是本研究中患者肾功能基本正常,血肌酐水平在生存组与死亡组中未见明显统计学差异,且基本处于正常参考范围,因此,与Yang等[22]近期发表的回顾性研究结果不同,正常的血肌酐值可能降低了血肌酐作为评分因子(如MELD、FIPS、CLIF-C AD等)的整体预测效能。因此,针对我国肝硬化人群,肌酐是否可作为肝功能评分模型的纳入指标,需要进一步验证。此外,在评价各个评分模型在不同时间点预测肝硬化TIPS术后生存的能力方面,Child-Pugh评分在术后短期的生存率预测效能良好,这与Lv等[23]的研究一致。但本研究发现,Child-Pugh评分的生存预测能力受时间因素影响较大,术后3年生存率的预测能力明显低于其对TIPS术后1年生存率的预测,这可能是由于Child-Pugh评分主要用于预测急性出血情况下门体分流术后的早期存活率,因此,对TIPS术后长期预测价值可能存在局限性。
尽管本研究纳入人群数量相对较多,但仍存在一些局限性。第一,本研究是回顾性的研究,失访患者较多,可能导致统计分析上实际死亡人数降低。第二,由于本研究中患者总死亡人数较少,且部分患者随访时间未满3年,可能导致统计数据产生偏倚。第三,随着TIPS技术的发展及修订后手术适应证的相对宽松,在本研究中未对支架类型、手术适应证等潜在影响因素进行矫正分析,此外,部分患者缺乏术中门静脉压力值,以上均是研究结果出现偏倚的潜在因素。
本研究表明,Child-Pugh、MELD、MELD-Na、CLIF-C AD及FIPS对肝硬化TIPS术后患者生存均有一定的预测价值,且Child-Pugh分级、MELD评分>9、MELD-Na评分>15,CLIF-C AD评分>35及FIPS评分>-0.45均可为TIPS治疗的肝硬化患者提供有效的预后风险分层。在短期预测上Child-Pugh评分生存预测能力更好,长期预测上MELD-Na评分生存预测能力更好。而FIPS评分预测能力均相对较差。
全文下载:
http://www.lcgdbzz.org/cn/article/doi/10.3969/j.issn.1001-5256.2023.03.016.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












经颈静脉肝内门体分流术(TIPS)是治疗肝硬化门静脉高压相关并发症的重要手段之一
30