安进新一代肾脏病药物Parsabiv上市申请遭FDA否决
美国生物技术巨头安进(Amgen)开发的新一代肾脏病药物Parsabiv(etelcalcetide)上市申请近日被美国食品和药物管理局(FDA)否决。Parsabiv是一种拟钙剂,开发用于正接受血液透析治疗的慢性肾脏病(CKD)患者继发性甲状旁腺功能亢进(sHPT,简称继发性甲旁亢)的治疗。安进于2015年8月向FDA提交了Parsabiv的新药申请,原本预期2016年能够拿到上市批文,但FDA
生物谷 - 安进,Parsabiv,etelcalcetide,肾病,透析,继发性甲旁亢 - 2016-08-26
安进骨质疏松症药物ROMO遭FDA拒绝
2016年秋天,安进骨质疏松药物romosozumab未能达到试验的次要关键终点,两个月前该药物再次出现了药物安全问题。对此,7月16日,美国FDA已经拒绝了该药物上市营销请求,但这对于该公司的竞争对手Radius来说是好消息。
新浪医药新闻 - ROMO,骨质疏松症 - 2017-07-17
2017年FDA批准的41个新药
截止目前,CDER已经批准了41个新分子实体,还有2个药物的PDUFA最后期限落在12月,如12月间FDA不加速批准新药,那么2017年获批的新分子实体可能是41-43个。当然本文所涉及的新药,均为 CDER 受理的 NDA 或 BLA,并不包括CBER审评的品种,如 CAR-T 产品。相对去年的20来个,今年算是一个丰收年。已经获批的41个产品中,有31个是全球首次批准,19个产品获得了优先
科睿唯安生命科学与制药 - FDA,新药 - 2017-12-06
2017上半年FDA批准的新药
2017上半年FDA共批准23个新药,包括16个新分子实体和7个新生物制品。这个数字已经超过2016年全年批准的新药数量总和。近20年来批准新药数量最多的年份是2015年的45个,上半年批准了14个新药。如果按此趋势持续下去,2017年批准的新药数量将创下历史新高。
新浪医药 - FDA,新药 - 2017-06-28
2017年FDA批准新药名单,上半年已达21种!
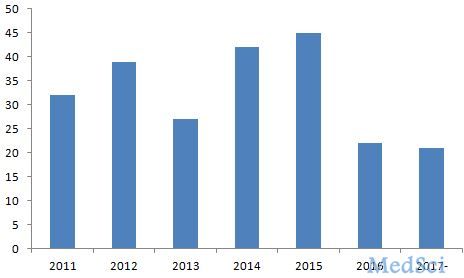
据FDA官网(http://www.fda.org)2017年5月22日提供的最新公布结果,截止2017年5月22日,FDA已经批准了21种新药,约占2016年FDA批准新药数量(22种)的95%,去年创造新药新低,今 年有望获得重大突破,甚至能创造近年来审批新药的新高。2011-2017年5月5日FDA批准新药数量变化见图1所示。 图1 FDA2011-2017年批准新药数量变
诸平 - FDA,新药 - 2017-05-25
安进新一代肾脏病药物Parsabiv获美国FDA批准
2017年02月09日讯 /生物谷BIOON/ --美国生物技术巨头安进(Amgen)开发的新一代肾脏病药物Parsabiv(etelcalcetide)近日在美国监管方面传来喜讯,美国食品和药物管理局(FDA)已批准Parsabiv用于正接受血液透析治疗的慢性肾脏病(CKD)患者继发性甲状旁腺功能亢进(sHPT,简称继发性甲旁亢)的治疗。
生物谷 - 安进,慢性肾脏病,Parsabiv,继发性甲旁亢 - 2017-02-09
为您找到相关结果约6个