Nature综述:靶向癌症干细胞信号通路和免疫微环境研发进展
2019-12-24 曼话 医药魔方Pro
癌症干细胞(CSCs),也被称为肿瘤起始细胞,是恶性肿瘤细胞的一个小亚群,具有增强的自我更新、转移扩散和治疗耐药能力,首次被发现是在急性髓系白血病(AML)中,之后,假定的癌症干细胞也从其它血液恶性肿瘤和多种类型的实体瘤中被分离出来,在肿瘤的发生、复发和转移中起着重要的作用。 目前,癌症干细胞起源于哪种细胞尚不清楚,一种假设是,癌症干细胞起源于分化程度更高的非干细胞,在转化后,主要是上皮-间
癌症干细胞(CSCs),也被称为肿瘤起始细胞,是恶性肿瘤细胞的一个小亚群,具有增强的自我更新、转移扩散和治疗耐药能力,首次被发现是在急性髓系白血病(AML)中,之后,假定的癌症干细胞也从其它血液恶性肿瘤和多种类型的实体瘤中被分离出来,在肿瘤的发生、复发和转移中起着重要的作用。
目前,癌症干细胞起源于哪种细胞尚不清楚,一种假设是,癌症干细胞起源于分化程度更高的非干细胞,在转化后,主要是上皮-间质转化(EMT:指上皮细胞在特定生理或病理情况下向间质细胞表型转变的过程)后获得干细胞样特性;另一种假设是,癌症干细胞起源于非恶性干细胞,致瘤体细胞突变诱导了这些非恶性干细胞转化为癌症干细胞。此外,有研究显示,炎症,尤其是炎性细胞因子(如干扰素、肿瘤坏死因子、IL-6和IL-17)可能在诱导癌症干细胞状态中发挥了作用。
目前,分离和鉴定癌症干细胞依然是一个挑战,因为肿瘤中包含了各种各样的细胞群,而癌症干细胞只占了一小部分(在实体瘤中通常小于1%)。此外,尽管CD133、CD44等细胞表面标志物、上皮细胞粘附分子以及醛脱氢酶酶活性已经在鉴定癌症干细胞中体现出了价值,但区分非癌症干细胞和真正的癌症干细胞依然困难,因为这些标志物并不是癌症干细胞所独有的,且并非所有肿瘤中的癌症干细胞都会表达这些典型的标志物。
在临床相关性方面,研究已证实,癌症干细胞对化疗和放疗具有天然的耐药性。此外,抑制治疗或微环境诱导的分化的癌细胞(即非癌症干细胞)向癌症干细胞的表型转化被认为是根除肿瘤的关键挑战。目前,Notch、WNT、Hedgehog(HH)和Hippo通路是抗癌症干细胞疗法的主要靶点。
知识卡:包括Notch、WNT、Hedgehog (HH)和Hippo在内的发育信号通路在癌症干细胞中通常发生了改变,且这些通路确实具有支持癌症干细胞维持和存活的关键调节功能。理论上来说,使用新型药物靶向具有天然耐药性的癌症干细胞具有降低癌症复发率并提高肿瘤治疗疗效的潜能。基于对癌症干细胞生物学认识的不断加深,多种靶向癌症干细胞的新治疗途径已被开发出来,并进入临床测试,其中,少数已获得监管批准。此外,一些已被批准用于治疗不同癌症的“老药”(如靶向HER2的药物以及CDK4/6抑制剂)也显示可能具有对抗癌症干细胞的活性。

图片来源:Nature Reviews Clinical Oncology
12月2日,来自美国NIH等机构的4位科学家在Nature Reviews Clinical Oncology上发表了题为“Targeting signalling pathways and the immune microenvironment of cancer stem cells — a clinical update”的最新综述,系统汇总了靶向Notch、WNT、Hedgehog和Hippo通路的疗法到目前为止的临床开发进展。同时,文章还讨论了癌症干细胞与免疫系统之间的相互作用,并概述了靶向癌症干细胞的新型免疫疗法。
一、靶向Notch通路
Notch信号通路是一种高度保守的细胞命运决定通路,其功能涉及癌症生物学的许多方面,包括癌症干细胞的表型、血管生成、转移和肿瘤免疫逃避。Notch通路的基因改变(突变)最初见于T细胞急性淋巴细胞白血病(T-ALL),之后,许多类型的癌症中都发现了异常的Notch信号。有趣的是,Notch通路的致病作用似乎取决于肿瘤类型。在T-ALL和大多数实体肿瘤中,Notch信号的异常激活促进了肿瘤发生。然而,在髓系恶性肿瘤中,该通路被发现具有肿瘤抑制作用(在急性髓系白血病中,Notch信号通路通常下调)。
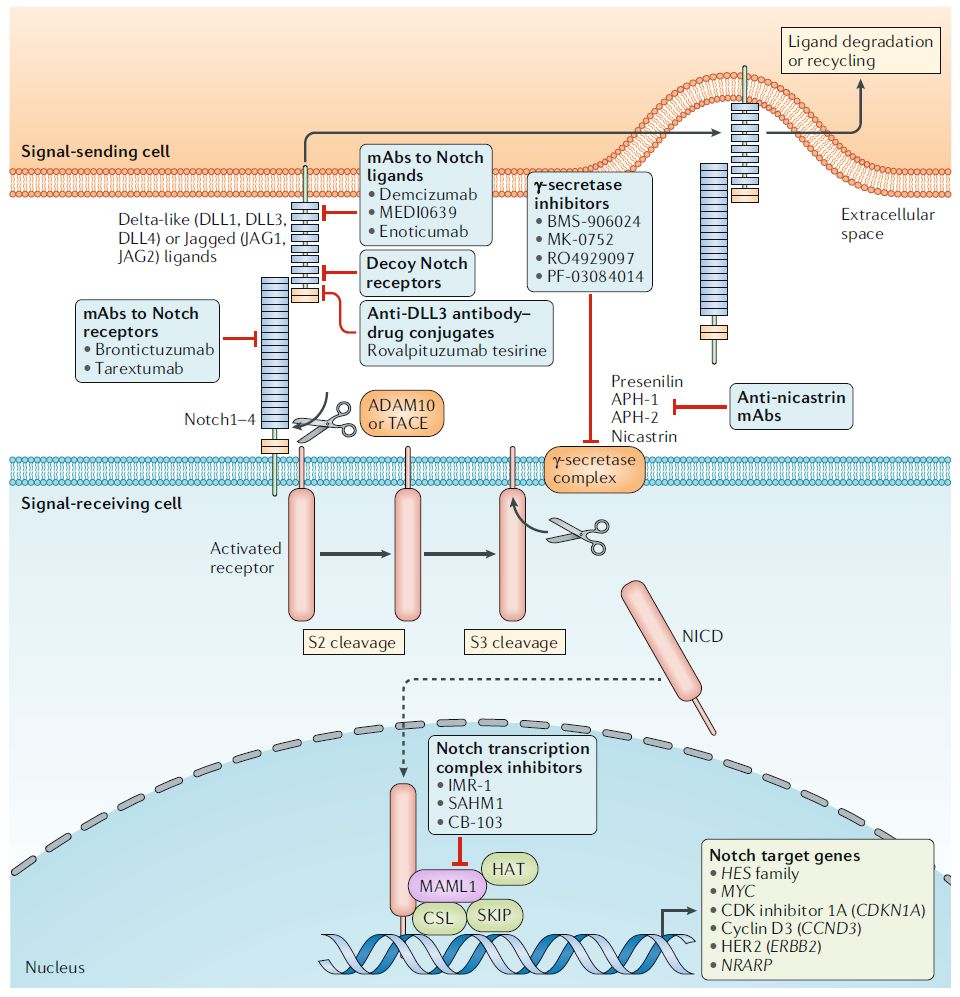 图1 经典Notch信号通路及相关在研抗癌抑制剂(图片来源:Nature Reviews Clinical Oncology)
图1 经典Notch信号通路及相关在研抗癌抑制剂(图片来源:Nature Reviews Clinical Oncology)药物研发
由于Notch信号通路的这种复杂性,想要成功开发一款靶向该通路的疗法必须对其在特定癌症中的机制有确切的理解。目前,科学家们已经开发出了多种具有不同靶点和作用机制的Notch通路抑制剂,且各种药物正处于不同的临床开发阶段(表1)。γ分泌酶抑制剂(γ-secretase inhibitors, GSIs,如MRK-003、PF-03084014、BMS-906024)是规模最大的一类药物,在临床前模型中显示了较强的抗肿瘤活性。PF-03084014、BMS-906024、MK-0752等γ分泌酶抑制剂的临床调查也取得了良好的结果。
利用单克隆抗体靶向Notch配体是抑制异常Notch信号的另一种策略,如DLL抗体Demcizumab。此外,也有团队开发靶向Notch受体的抗体,如抗Notch1的单抗Brontictuzumab、同时靶向Notch2和Notch3的全人源IgG2抗体Tarextumab。
表1靶向Notch信号通路的在研药物的临床试验结果
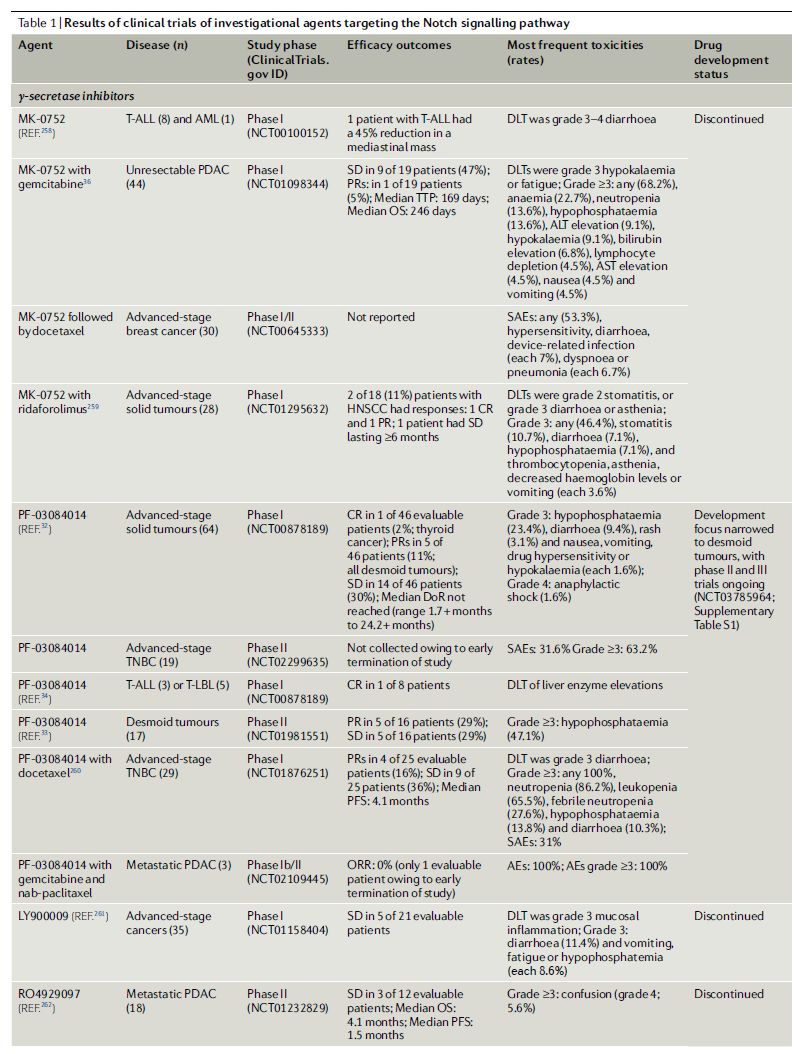

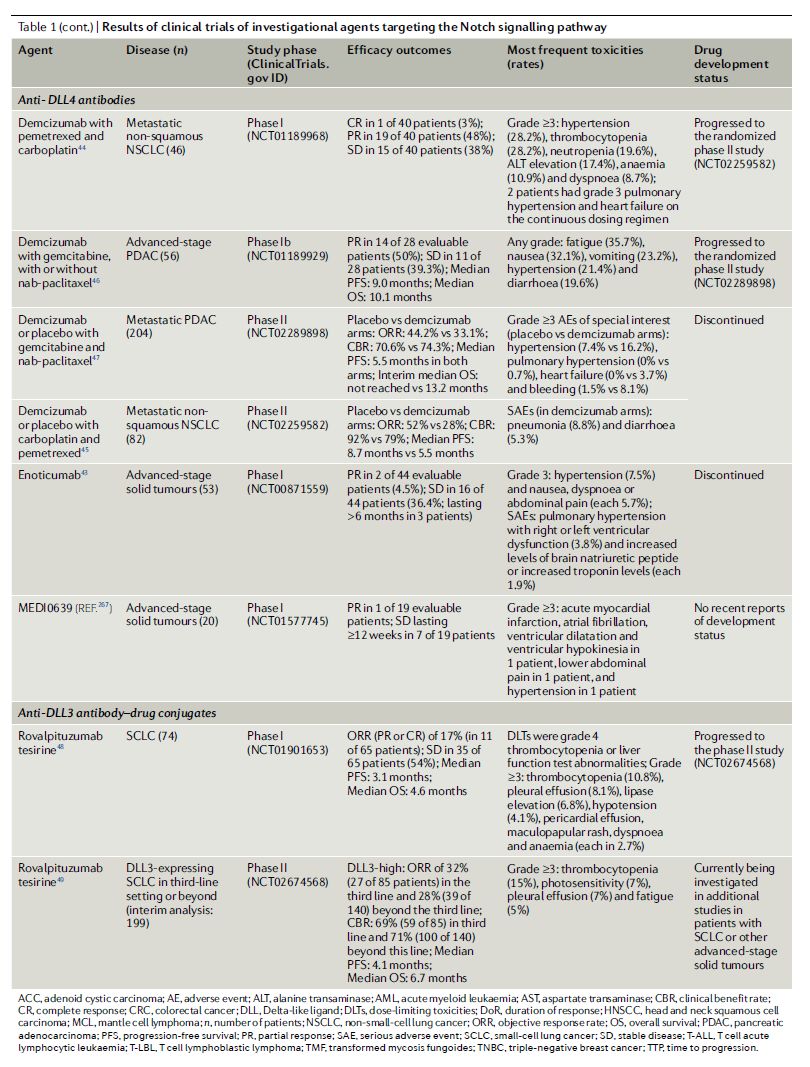 数据来源:Nature Reviews Clinical Oncology
数据来源:Nature Reviews Clinical Oncology
二、靶向WNT通路
WNT信号级联由三个主要的通路组成:1)经典(β-catenin依赖性)WNT通路,该通路与一种转录反式激活复合物的激活有关,该复合物包括β-catenin、T细胞特异性转录因子(TCF)以及淋巴增强结合因子(lymphoid enhancer-binding factor,LEF);2)非经典(β-catenin非依赖性)平面细胞极性通路(planar-cell polarity pathway),该通路参与了细胞骨架的调控;3)非经典WNT-钙离子通路,该通路参与调节细胞内钙水平。
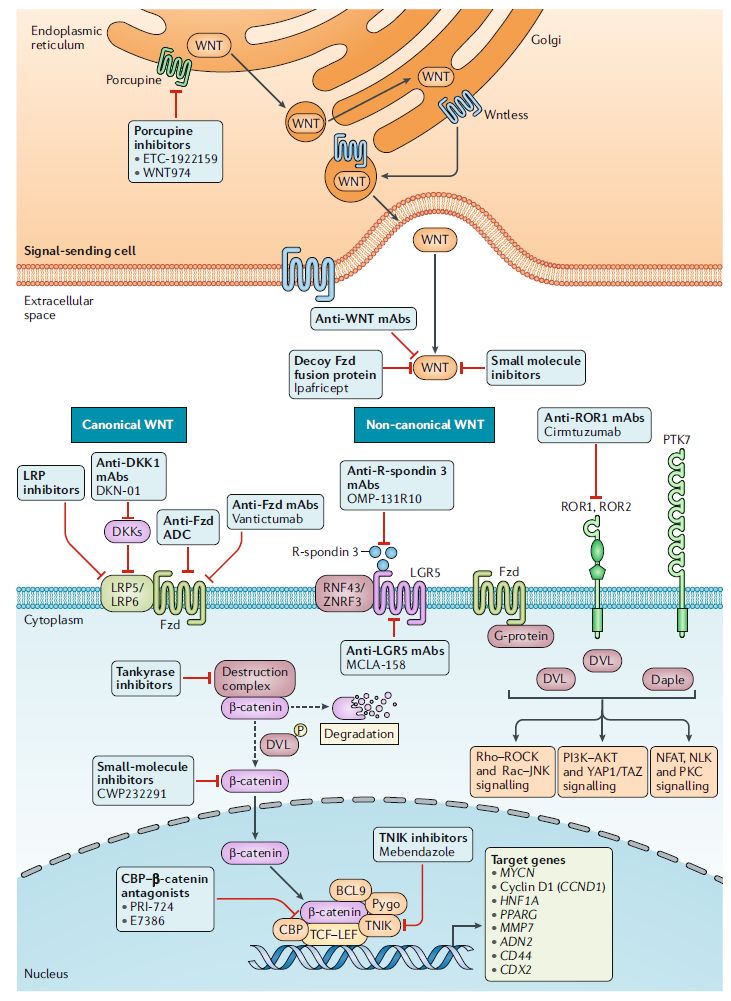 图2 经典和非经典(canonical and non-canonical)WNT信号通路以及相关在研抗癌抑制剂(图片来源:Nature Reviews Clinical Oncology)
图2 经典和非经典(canonical and non-canonical)WNT信号通路以及相关在研抗癌抑制剂(图片来源:Nature Reviews Clinical Oncology)
WNT通路的功能与癌症有明显的相关性,WNT信号失调在多种癌症的肿瘤发生中起重要作用。举例来说,在大多数结直肠癌(CRCs)中,WNT信号通路会上调,这种上调最常归因于APC(adenomatous polyposis coli protein)功能的丧失(约50%的结直肠癌会发生APC突变)。此外,异常的WNT通路激活(归因于经典WNT受体和配体的过表达)也存在于约一半的基底样乳腺癌中,且与不良的治疗结果有关。WNT信号失调在急性髓系白血病(AML)、多发性骨髓瘤(MM)、慢性粒细胞白血病(CML)、T-ALL、慢性淋巴细胞白血病(CLL)等癌症中也有重要作用。因此,抑制该通路的药物具有诱人的抗癌潜能。
药物研发
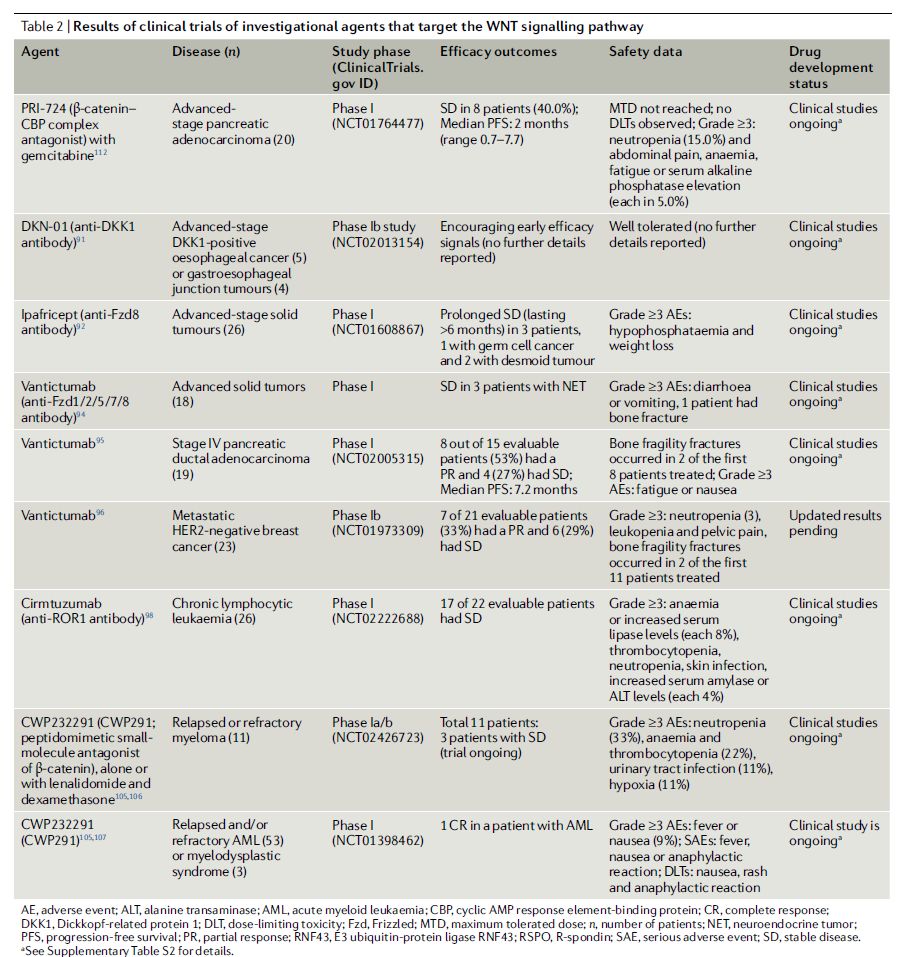
WNT通路的药理学拮抗剂可分为四大类:1)靶向WNT信号通路中跨膜蛋白或配体的药物,这类药物包括单抗(如DKN-01、Vantictumab、Cirmtuzumab)、ADC、小分子等多种类型;2)干扰WNT配体加工和分泌的Porcupine抑制剂,如WNT974、ETC-1922159;3)激活caspases酶或抑制tankyrase酶的药物,这类药物可促进β-catenin降解,如CWP232291;4)下游β-catenin-TCF-LEF依赖性转录抑制剂(inhibitors of downstream β-catenin–TCF–LEF-dependent transcription)。目前,这几类药物均有候选产品进入临床测试(表2)。
表2 靶向WNT信号通路的在研药物的临床试验结果
 数据来源:Nature Reviews Clinical Oncology
数据来源:Nature Reviews Clinical Oncology
三、靶向Hedgehog(HH)通路
HH信号通路在胚胎发育过程中起着重要作用,该通路在成人组织中活性异常已被证实与多种实体肿瘤有关,如皮肤基底细胞癌、髓母细胞瘤SHH亚型等。HH配体分泌细胞可加工和释放多种HH亚型,包括Sonic hedgehog (SHH)、Indian hedgehog和Desert hedgehog,这些HH亚型主要以旁分泌的方式与跨膜受体Patched 1 (PTCH1)和PTCH2结合,从而抑制其对另一种跨膜蛋白Smoothened (SMO)的抑制活性(图3)。随后,这种信号级联导致GLI转录因子的激活和核定位,而GLI转录因子会驱动HH靶基因的表达。其中,大部分靶基因与细胞增殖、生存和血管生成有关。
 图3 经典Hedgehog信号通路以及作为抗癌疗法的相关在研抑制剂(图片来源:Nature Reviews Clinical Oncology)
图3 经典Hedgehog信号通路以及作为抗癌疗法的相关在研抑制剂(图片来源:Nature Reviews Clinical Oncology)
异常的HH信号也与多种血液恶性肿瘤中白血病干细胞(leukaemic stem cell,LSCs)的维持和扩增相关。举例来说,有研究在髓系LSCs中鉴定出了异常的HH信号,且HH通路组成表达的增加与急性髓系白血病(AML)细胞系对化疗耐药有关。HH信号在慢性粒细胞白血病(CML)中也被激活,促进了BCR–ABL1-阳性LSCs的扩增,因此与CML的进展有关。其它与HH信号相关的血液恶性肿瘤包括多发性骨髓瘤(MM)、慢性淋巴细胞白血病(CLL)、弥漫性大B细胞淋巴瘤等。
药物研发
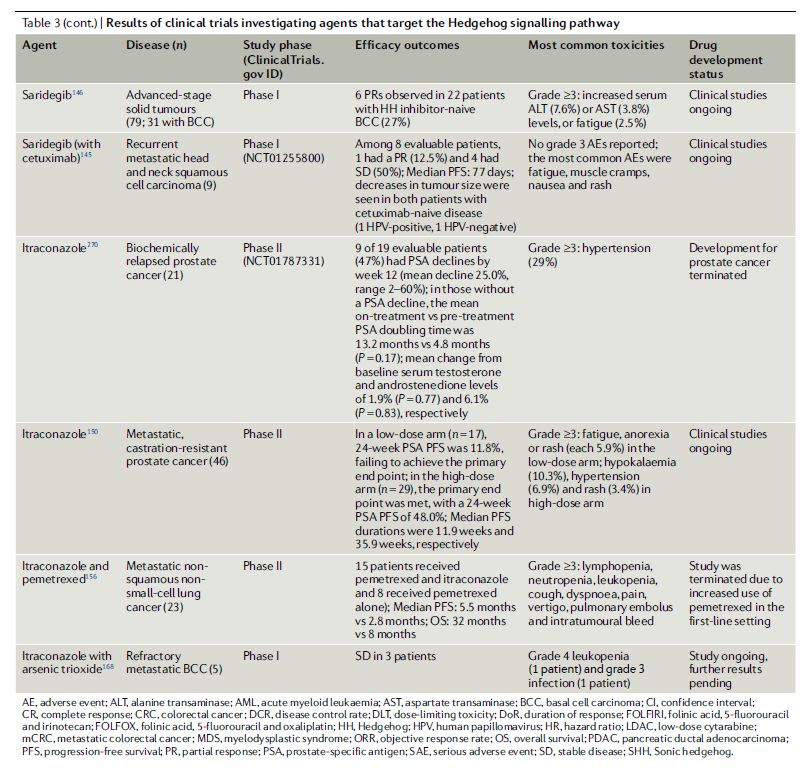
目前,已有靶向HH通路的药物被批准上市,但调查这类药物治疗血液肿瘤和实体瘤的潜力依然是热门研究领域。HH通路拮抗剂的三个主要靶点是HH配体、SMO和GLI转录因子(图3),后两类药物已在临床试验中得到验证(表3)。
美国FDA分别于2012、2015以及2018年批准了3款SMO抑制剂上市,Vismodegib和Sonidegib用于治疗基底细胞癌,glasdegib用于治疗急性髓系白血病(AML)。
靶向GLI转录因子也是一种有吸引力的治疗选择,因为这些HH通路的下游效应因子能够诱导参与细胞增殖和生存的基因的上调,但不依赖于经典HH通路。靶向GLI转录活性的药物(如GANT58、GANT61、pirfenidone)旨在克服肿瘤对SMO抑制剂的耐药性。临床前研究已经为这些药物的抗肿瘤活性提供了证据,特别是GANT61在肝细胞癌(HCC)、非小细胞肺癌(NSCLC)、横纹肌肉瘤和胰腺癌、卵巢癌和乳腺癌模型中的作用。GANT61和GANT58也被证明可在HH通路激活的胰腺癌小鼠异种移植中降低GLI1介导的转录,抑制细胞增殖。还有研究显示,GANT58可通过降低GLI1和PTCH1的表达来降低T-ALL细胞的生存能力。不过,目前,没有关于这些药物的活跃肿瘤临床试验正在进行中。
值得一提的是,被FDA批准用于治疗急性早幼粒细胞白血病的三氧化二砷(ATO)也是GLI1和GLI2的有效抑制剂。在临床前研究中,ATO可与GLI1结合,抑制其转录活性,从而降低GLI1靶基因的表达。目前,许多试验正在血液或实体恶性肿瘤患者中调查ATO单药治疗或联合标准治疗的潜力。
表3 调查靶向Hedgehog信号通路的药物的临床试验结果


 数据来源:Nature Reviews Clinical Oncology
数据来源:Nature Reviews Clinical Oncology
四、靶向Hippo通路
进化上保守的Hippo信号通路发挥着平衡细胞增殖和凋亡能力的功能。经典Hippo通路的核心由两种激酶复合物组成,第一种激酶复合物由MST1和MST2 (MST1/2)组成,第二种激酶复合物由LATS1和LATS2 (LATS1/2)组成,两者分别与接头蛋白SAV1和MOB1结合。这些激酶调节磷酸化事件,导致下游转录共激活因子YAP1和TAZ的细胞质保留和降解,从而抑制与细胞生长、存活、迁移、自我更新和上皮间质转化(EMT)相关的靶基因的转录(图4)。
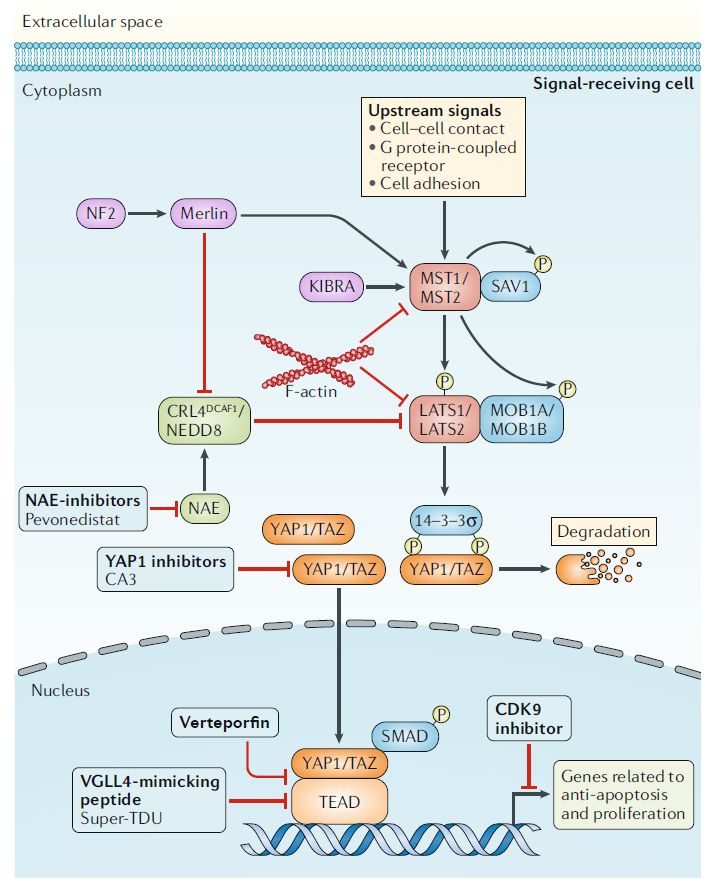 图4 Hippo信号通路和相关治疗靶点(图片来源:Nature Reviews Clinical Oncology)
图4 Hippo信号通路和相关治疗靶点(图片来源:Nature Reviews Clinical Oncology)
研究证实,Hippo通路异常会导致YAP1和/或TAZ活性增加,进而导致癌症干细胞群扩增,而这种扩增又会促进实体瘤的发展。大量证据表明,YAP1和TAZ在实体肿瘤中是强有力的致癌基因,其中,YAP1在实体肿瘤中的过表达与癌症进展以及耐药性发展有关。不过,这两种蛋白在血液恶性肿瘤中的作用尚不明确。
值得一提的是,Hippo通路基因和其它肿瘤相关信号通路之间的串扰已被证明导致了恶性肿瘤的发展。例如,来自癌症基因组图谱的组学数据显示,HH与Hippo通路活性呈正相关。科学家们认为,考虑到Hippo是连接多种通路(包括Notch、WNT和HH)的枢纽,其作为治疗靶点的潜力值得进一步被研究。
药物研发
Hippo通路中重要的药物靶点包括肿瘤抑制激酶LATS1/2和MST1/2。与驱动肿瘤发生的典型激酶(如AKT、SRC、ABL1和RAF)不同(这些激酶的促癌作用通常源于其功能激活突变),Hippo通路的激酶发生了功能缺失突变。这表明,为了抗癌,科学家们必须想办法增强Hippo通路核心激酶的活性,这是一项比抑制激活激酶更具挑战性的任务。
目前,很少有特异性靶向Hippo通路的药物在临床试验中进行测试,但一些实验方法显示出了希望(图4),如YAP1抑制剂Verteporfin和CA3、内源性YAP1拮抗剂VGLL4等。
此外,first-in-class NEDD8激活酶抑制剂pevonedistat已被证实可阻止CRL4DCAF1介导的LATS1/2降解,从而减弱YAP1活性(图4)。在一项涉及急性髓系白血病(AML)和骨髓增生异常综合征(MDS)患者的I期试验中,pevonedistat联合azacitidine导致了50%的ORR,患者接受6个周期以上治疗后,ORR上升到了83%。在涉及髓系恶性肿瘤或晚期实体瘤患者的其它早期试验中,Pevonedistat作为单药以及联合其它药物也显示出了活性(表4)。
表4 靶向Hippo信号通路的在研药物的临床试验结果
 数据来源:Nature Reviews Clinical Oncology
数据来源:Nature Reviews Clinical Oncology
五、癌症干细胞(CSCs)的免疫学
在过去几十年里,大量文献广泛描述了癌细胞与免疫系统的相互作用,然而,癌症干细胞与肿瘤微环境(TME)中免疫细胞之间的关系在最近才开始被研究。
CSCs与免疫系统相互作用
肿瘤相关巨噬细胞(TAMs)是TME中被研究的比较透彻的细胞群,根据TAMs与其它免疫细胞的相互作用及其细胞因子表达情况,可分为抑癌M1型和促癌M2型。经证实,TAMs可通过IL-6诱导的STAT3激活增加肝细胞癌来源的癌症干细胞的增殖,STAT3还会进一步刺激细胞因子的产生,形成一个促进癌症干细胞自我更新的正反馈环路。TAMs也被证明可通过与EPHA4(ephrinwith ephrin type A receptor 4)直接相互作用帮助乳腺癌症干细胞群的维持(图5)。
 图5 新型基于免疫的靶向癌症干细胞的途径(图片来源:Nature Reviews Clinical Oncology)
图5 新型基于免疫的靶向癌症干细胞的途径(图片来源:Nature Reviews Clinical Oncology)
骨髓来源的抑制性细胞(MDSCs)是另一种支持癌症干细胞的免疫细胞。来自卵巢癌细胞的证明表明,可抑制TME中其它免疫细胞的MDSCs能够通过诱导microRNA-101表达促进癌症干细胞表型。此外,树突状细胞(DCs)也被证明可促进滤泡性淋巴瘤癌症干细胞的化疗耐药性和致瘤性,而表达IL-17的调节性T细胞(Treg细胞)也被发现可在体外促进癌症干细胞的发展。
在TME中的免疫细胞支持癌症干细胞的同时,癌症干细胞也在通过调节免疫细胞的活性来驱动肿瘤发生和疾病进展。举例来说,胶质母细胞瘤癌症干细胞被证明可通过表达各种细胞因子(包括集落刺激因子、TGF-β和巨噬细胞抑制性细胞因子)来促进巨噬细胞向M2型极化。癌症干细胞还可削弱巨噬细胞和树突状细胞(DCs)的活性。黑色素瘤和胶质母细胞瘤癌症干细胞也被发现可在体外抑制T细胞反应。而来自头颈部鳞状细胞癌和黑色素瘤患者的癌症干细胞也被证实能够招募具有免疫抑制和促瘤作用的调节性T细胞(Treg细胞),并促进其体外增殖。此外,癌症干细胞还可通过分泌多种细胞因子(如TGF-β、IL-10、IL-4 和IL-13)到肿瘤微环境中对多种免疫细胞产生抑制作用。
CSCs的免疫逃逸
肿瘤细胞逃避免疫系统检测的一个主要机制与最小化抗原性有关,而最小化抗原性是通过下调细胞抗原处理和递呈机制的关键组成来实现的。研究证实,抗原处理和递呈机制组成的下调为癌症干细胞提供了逃避T细胞介导的免疫反应的方式。此外,癌症干细胞还被发现通过表达高水平的PD-L1来抑制T细胞的功能。还有研究证实,双功能配体CD80的表达也通过介导抗肿瘤T细胞的功能抑制调节了不同肿瘤类型癌症干细胞的免疫逃逸。
癌症干细胞也能有效躲避先天免疫系统的攻击。研究证实,急性髓系白血病(AML)、乳腺癌和胶质母细胞瘤的癌症干细胞能够降低NK细胞激活配体(如NKG2D)的表达,并表现出对NK细胞介导的细胞毒性的抵抗。
癌症干细胞自身的致癌信号通路也可能有助于免疫逃逸。比如,有研究证实,WNT–β‐catenin信号与免疫排斥具有相关性。肝细胞癌和黑色素瘤肿瘤样本的基因表达分析显示,β‐catenin信号与肿瘤微环境中T细胞浸润缺乏有关。一些其它证据也表明,肿瘤内癌症干细胞通路的异常与特定的免疫特征有关,如在胰腺癌中,NOTCH2扩增与细胞毒性T细胞活性较低有关;在乳腺癌中,Notch通路激活与肿瘤相关巨噬细胞(TAMs) 激活和招募有关;在卵巢癌中,YAP1表达增加与细胞毒性T细胞浸润受损有关;在前列腺癌中,YAP1活性增加与骨髓来源的抑制性细胞(MDSCs)招募增加有关。
免疫疗法
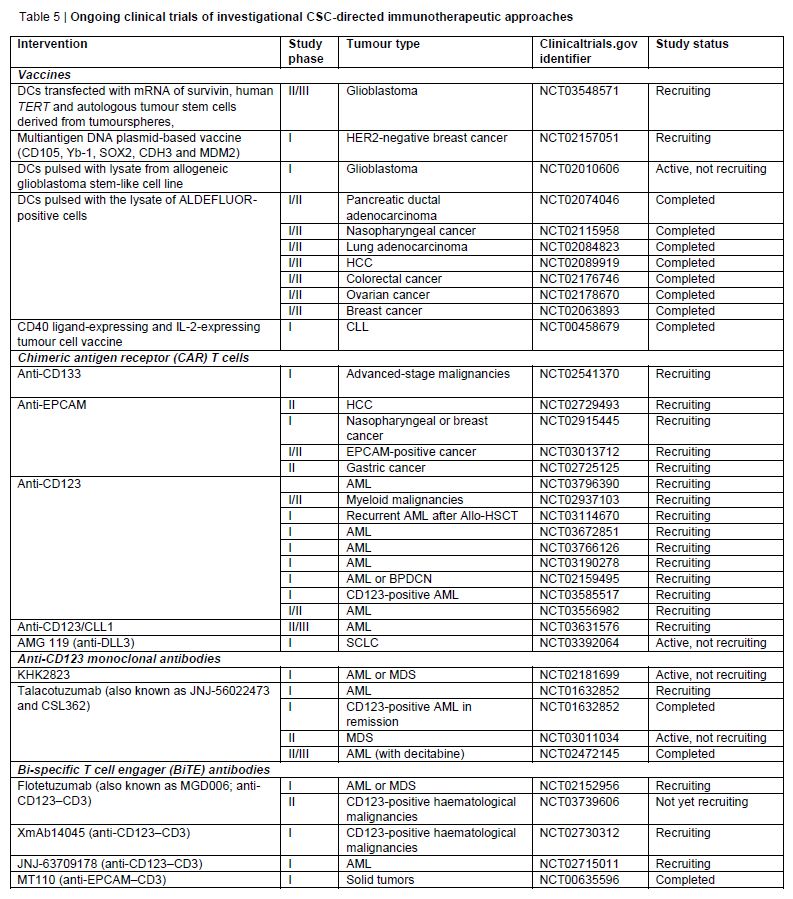
靶向癌症干细胞与免疫系统相互作用的多种方法正在被积极研究中,一些靶向癌症干细胞的免疫疗法正处于临床开发阶段(表5)。这些实验性治疗策略包括利用基于抗体的疗法刺激肿瘤特异性T细胞、改变免疫抑制肿瘤微环境以及靶向癌症干细胞表面标志物。
迄今为止,被研究最多的是用于促进肿瘤细胞识别和清除的DC疫苗。来源于癌症干细胞的材料被用作抗原资源,以产生DC介导的肿瘤特异性免疫反应。
此外,通过在体外利用CSC peptide-pulsed autologous DCs刺激供者CD8+ T细胞产生的CSC启动T细胞在临床前模型中显示了显著的抗肿瘤作用。特异性靶向CSC标志物的CAR-T细胞也正在临床研究中被测试(表5)。
靶向CSC表面标志物的基于抗体的治疗途径包括单抗(如CD123单抗Talacotuzumab、KHK2832)、ADC(如IMGN632、Tucotuzumab、Tagraxofusp、rovalpituzumab tesirine)以及BiTE抗体(如Flotetuzumab、XmAb14045、JNJ-63709178、MT110、AMG757)。
由于大量证据表明,激活STAT3可直接调节某些类型癌症干细胞中PD-L1的表达,且可通过其它机制促进免疫抑制肿瘤微环境,因此,STAT3抑制剂被认为是一种有潜力的治疗策略。
临床前数据支持的其它有吸引力的癌症干细胞免疫治疗靶点包括趋化因子IL-8及其受体CXCR1、细胞因子IL-6、以及癌症干细胞表达的蛋白CD47。
表5 靶向癌症干细胞的在研免疫疗法正在进行的临床试验
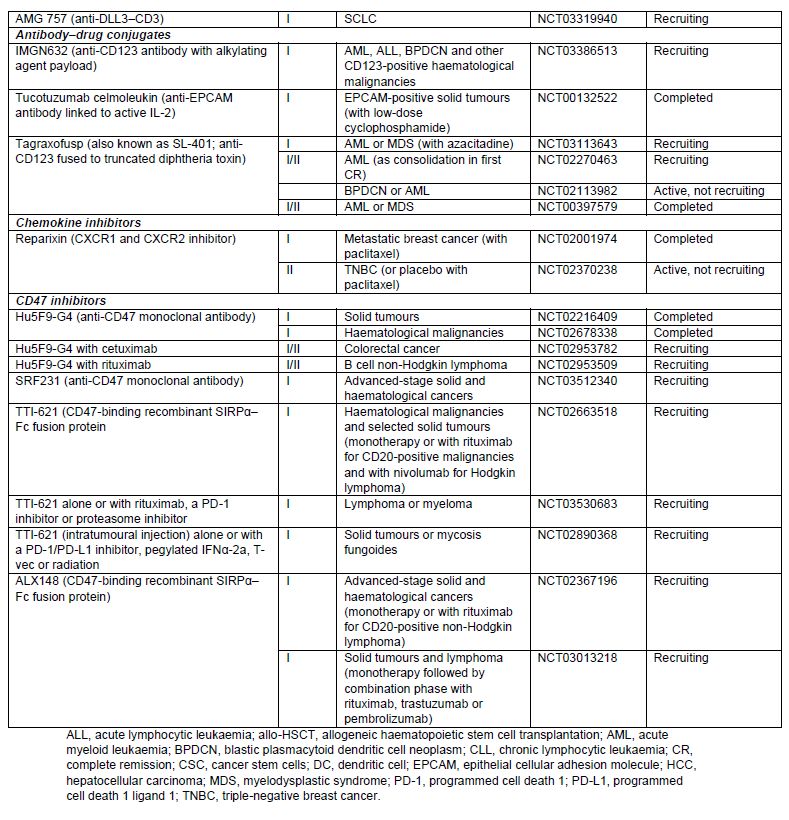 数据来源:Nature Reviews Clinical Oncology
数据来源:Nature Reviews Clinical Oncology
六、小结
在过去一些年里,业界做了很多努力来开发靶向癌症干细胞信号通路的新药。值得注意的进步是,FDA批准了治疗AML患者的SMO抑制剂glasdegib。一些其它药物虽然暂未获批但也取得了积极进展。随着科学家们对癌症干细胞与免疫系统独特关系的进一步了解,未来,靶向癌症干细胞的免疫疗法更加令人期待。
相关论文:
Joseph A. Clara et al. Targeting signalling pathways and the immune microenvironment of cancer stem cells — a clinical update. Nature Reviews Clinical Oncology (2019).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#靶向癌症干细胞#
32
#Nat#
34
干细胞是热点,但是进入临床仍然需要时间和临床疗效验证哦
48
#研发#
33
#癌症干细胞#
30
#信号通路#
21