JACC Basic Transl Sci:TGF-β 诱导蛋白的内皮过度表达会损害静脉血栓溶解:在 CTEPH 中的可能作用
2024-05-12 刘少飞 MedSci原创 发表于上海
本研究发现,内皮细胞中TGFBI的过表达与慢性血栓栓塞性肺动脉高压(CTEPH)患者中血栓未溶解和纤维化相关,揭示了其在CTEPH发病机制中的重要作用。
内皮细胞在血栓栓塞的血管内壁上扮演着重要角色,它们不仅仅是血管的构成要素,还参与了血管功能的调节和修复。在静脉血栓重塑的过程中,内皮细胞通过释放多种生物活性物质,如细胞因子和生长因子,参与了血栓的形成、溶解和重塑过程。然而,在慢性血栓栓塞性肺动脉高压(CTEPH)患者中,血栓的重塑过程常常出现问题,导致形成未解决的、纤维化的血栓,这些血栓不规则地阻塞了肺动脉,严重影响了患者的生命质量和预后。

为了探究内皮细胞在静脉血栓溶解障碍中的调控机制,本研究旨在识别受损的内皮介质,并确定其在CTEPH患者血管阻塞病理过程中的作用。通过从肺动脉内膜切除标本(PEA)中培养出的内皮细胞,研究人员进行了mRNA分析,发现了与CTEPH相关的内皮细胞特异性基因表达谱。通过nCounter基因表达分析和PEA组织微阵列的免疫组化分析,以及血浆免疫测定,验证了这些基因在CTEPH中的表达。同时,利用人类肺动脉内皮细胞(HPAECs)进行慢病毒过表达,以及在小鼠模型中进行外源性重组蛋白的给予,进一步评估了这些内皮介质对静脉血栓溶解的影响。
研究结果显示,与转化生长因子β(TGFβ)信号通路相关的因子,如TGFβ诱导蛋白(TGFBI或BIGH3)和转胶蛋白(TAGLN),在CTEPH患者中显著过表达。这些因子的过表达可能与血栓形成和重塑过程中TGFβ信号通路的异常活化有关。同时,免疫组织化学分析将潜在的疾病候选基因定位到了血管富集的区域,进一步证明了它们在CTEPH病理生理过程中的重要性。
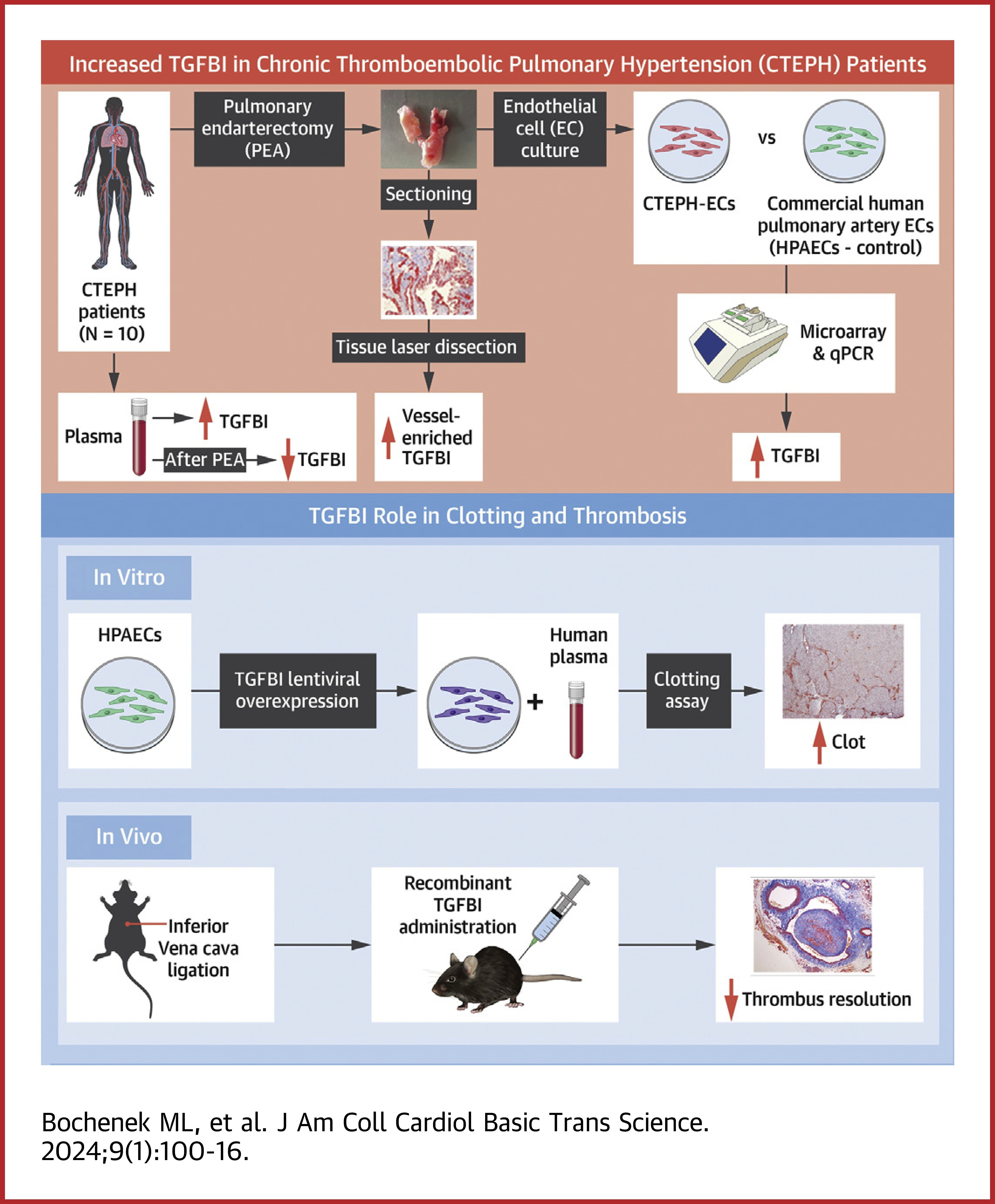
此外,实验结果还显示,在HPAECs中过表达TGFBI会增加人类血栓的纤维化重塑,在小鼠模型中外源性给予重组TGFBI会延迟静脉血栓的溶解。此外,研究还观察到CTEPH患者血浆中TGFBI水平显著升高,并在PEA手术后出现下降,进一步验证了TGFBI在CTEPH发病机制中的重要作用。
综上所述,本研究发现内皮中TGFBI的过表达会促进静脉血栓的非溶解和纤维化,这对CTEPH的发病机制具有重要的影响。这一发现为CTEPH的治疗提供了新的靶点,未来有望通过干预TGFBI信号通路来改善患者的血栓栓塞病情。
参考文献:
Bochenek ML, Saar K, Nazari-Jahantigh M, Gogiraju R, Wiedenroth CB, Münzel T, Mayer E, Fink L, Schober A, Hübner N, Guth S, Konstantinides S, Schäfer K. Endothelial Overexpression of TGF-β-Induced Protein Impairs Venous Thrombus Resolution: Possible Role in CTEPH. JACC Basic Transl Sci. 2023 Oct 25;9(1):100-116. doi: 10.1016/j.jacbts.2023.08.005. PMID: 38362348; PMCID: PMC10864968.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#TGF-β# #CTEPH#
0