PNAS:U2AF的不同构象在mRNA前体剪接中起着关键性作用
2016-11-07 佚名 生物谷
在基因的RNA转录本能够表达蛋白之前,它们的非编码区被一种称作剪接体的复合体移除。在一项新的研究中,德国科学家们报道这种分子复合体的一种成员的不同构象在这种移除过程中发挥着至关重要的作用。 RNA充当着将储存在DNA中的遗传信息有序地转化为合成特异性蛋白的蓝本的中间产物。在细胞核中,DNA的特定片段首先转录为mRNA前体(pre-mRNA)。在很多情形下,这些主要的RNA转录本含有打断实际的蛋白
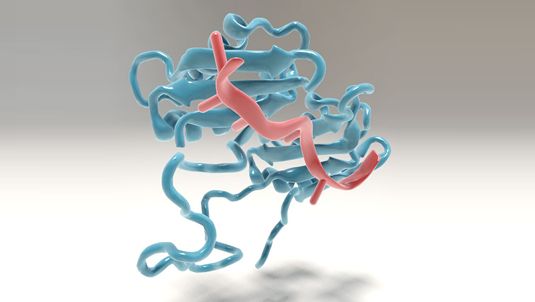
RNA充当着将储存在DNA中的遗传信息有序地转化为合成特异性蛋白的蓝本的中间产物。在细胞核中,DNA的特定片段首先转录为mRNA前体(pre-mRNA)。在很多情形下,这些主要的RNA转录本含有打断实际的蛋白编码序列的散在序列(即内含子)。在这种信息能够被用来合成蛋白之前,这些内含子必须被移除,这样编码序列就被拼接在一起。确实,一种给定的基因可能通过一种被称作选择性剪接的过程编码一种蛋白的几种不同形式---不同剪接的mRNA链编码不同的蛋白形式,其中选择性剪接在转录后基因调节发挥着重要作用。所有的剪接都是被细胞核中的一种复杂的分子复合体(被称作剪接体)执行的。
在这项项新的研究中,在德国慕尼黑大学化学系Don Lamb教授和德国慕尼黑理工大学Michael Sattler教授的领导下,研究人员证实在剪接体在mRNA前体上的组装中起着至关重要作用的一种蛋白所采用的不同结构构象对剪接效率产生关键性影响。相关研究结果于2016年10月26日在线发表在PNAS期刊上,论文标题为“Recognition of the 3′ splice site RNA by the U2AF heterodimer involves a dynamic population shift”。
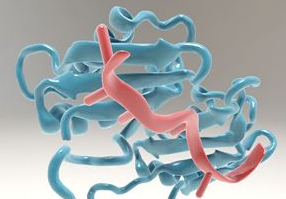
在人细胞中发现的剪接体是由很多不同的亚基组成的,这些亚基必须以一系列精心设计的步骤在mRNA前体上组装在一起。单个亚基的结合特异性在剪接体组装和功能中起着至关重要的作用。论文第一作者Lena Voithenberg说,“我们研究的被称作U2辅助因子(简写为U2AF)的组装因子在正确识别这些内含子的一端上的剪接位点中发挥关键性作用。” U2AF本身是由两种不同的亚基组成的。Voithenberg和她的同事们利用单分子荧光显微技术证实在U2AF的游离形式时,它的大亚基是一种高度动态的蛋白。利用核磁共振开展的实验进一步提供与U2AF的结构和构象动态变化相关联的信息。
Voithenberg解释道,“我们发现U2AF的大亚基在微妙到毫秒的时间范围内快速地切换它的构象:从一种开放结构切换到一种封闭结构。”仅有开放结构的这种大亚基能够结合到mRNA前体上。再者,具有这种构象的这种大亚基的比例依赖于可获得的mRNA前体序列的相对结合亲和度:相比于具有较低亲和度的那些序列,对这种结合亚基(即U2AF的大亚基)具有较高亲和度的序列具有更高的被识别和切割的概率。这些结果提示着U2AF的大亚基采取的不同结构构象起着调节不同剪接位点上的剪接效率的作用。这接着对mRNA前体如何被切割和剪接产生显著的影响,而这不仅会影响最终蛋白的结构,而且也影响它的合成速率。
Lena Voith von Voithenberg, Carolina Sánchez-Ricoe,f,g, Hyun-Seo Kange,f,g, Tobias Madle,f,g,h, Katia Zanieri, Anders Bartha,b,c,d, Lisa R. Warnere,f,g, Michael Sattlere,f,g,1, and Don C. Lamb.Recognition of the 3′ splice site RNA by the U2AF heterodimer involves a dynamic population shift.PNAS.2016
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#PNAS#
33