JAMA ONCOLOGY:实体瘤相关骨转移治疗新选择:MW032与Denosumab(地诺单抗)效用和安全性的对照分析
2024-02-14 生物探索 生物探索 发表于陕西省
研究人员旨在评估MW032与denosumab在治疗实体瘤相关骨转移方面的效果是否等同。
转移性骨疾病(metastatic bone disease, MBD)是癌症的一种常见并发症,全球超过150万患者受到影响,尤其是乳腺癌(breast cancer)和前列腺癌(prostate cancer)患者。在这些患者中,骨转移导致的骨破坏(bone destruction)会引起一系列临床上重要的并发症,如骨折(fracture)、需要进行骨放射治疗(bone radiation)或手术、脊髓压迫(spinal cord compression)、高钙血症(hypercalcemia)或骨痛(bone pain)。这些并发症统称为骨相关事件(skeletal-related events, SREs),与患者的生存率和生活质量密切相关。
Denosumab(地诺单抗)是一种针对人类RANKL的高亲和力和特异性的人源化单克隆抗体(human monoclonal antibody),通过抑制成骨细胞(osteoclasts)的成熟、分化和功能,减少骨吸收和破坏,增加骨矿物质密度(bone mineral density)。然而,denosumab的价格和可获得性限制了其在发展中国家和经济困难地区的应用。因此,开发denosumab的生物仿制药可能会扩大药物的可及性,减轻患者的经济负担。
2月8日发表于JAMA ONCOLOGY 的研究“Efficacy, Safety, and Population Pharmacokinetics of MW032 Compared With Denosumab for Solid Tumor-Related Bone Metastases: A Randomized, Double-Blind, Phase 3 Equivalence Trial”,报道了一种名为MW032的药物,一种denosumab生物仿制药(biosimilar),用于治疗与实体瘤(solid tumor)相关的骨转移(bone metastases)。在这项随机、双盲、III期(phase 3)等效试验(equivalence trial)中,研究人员旨在评估MW032与denosumab在治疗实体瘤相关骨转移方面的效果是否等同。研究包括了701名患者,这些患者来自中国46个临床中心(clinical sites)。
研究结果表明,MW032与denosumab在疗效(efficacy)、人群药代动力学(population pharmacokinetics)和安全性(safety profile)方面具有生物相似性(biosimilarity),这表明MW032可能成为治疗实体瘤相关骨转移患者的一个新的治疗选择。

Highlights
生物相似性证明:研究成功证明了MW032与denosumab在治疗实体瘤(solid tumor)相关骨转移(bone metastases)方面具有等效的疗效(efficacy)。这一发现基于骨转换标志物(bone turnover markers)的评估和骨相关事件(skeletal-related events, SREs)的发生率,两组之间的差异在预先定义的等效边界(equivalence margins)内。
大规模、多中心的随机对照试验:这项研究为期53周,是在中国46个临床中心进行的大规模、多中心、随机、双盲的III期(phase 3)等效试验。研究共纳入了701名患者,这为MW032的疗效和安全性提供了强有力的证据。
安全性和人群药代动力学(population pharmacokinetics)评估:MW032不仅在疗效上与denosumab相似,而且在安全性和人群药代动力学方面也显示出相似性。这意味着MW032的安全性与denosumab相似,且MW032在不同患者群体中的药物动态行为与denosumab一致。
提高药物可及性:作为denosumab的生物仿制药(biosimilar),MW032的开发有潜力降低治疗成本,从而扩大患者对于这种有效治疗骨转移的药物的可及性和可负担性。
全面的疗效和安全性数据:研究提供了包括基线到第13周的尿液N-端肽/肌酐比率(urinary N-telopeptide/creatinine ratio, uNTx/uCr)的百分比变化等综合疗效指标,以及通过尿液和血液生物标志物的长期跟踪,对MW032与denosumab在治疗骨转移中的效果进行了全面评价。
为未来研究铺平道路:通过证明MW032的疗效和安全性,这项研究为进一步探索MW032在其他癌症类型和疾病状态中的应用提供了基础,有可能进一步扩大其治疗领域。
Strategies
研究设计(Study Design)
随机、双盲、III期(phase 3)等效试验:该研究为期53周,采用随机、双盲的设计,确保了研究的客观性和结果的可靠性。
多中心研究(Multicenter Study):在中国46个临床中心进行,增加了研究结果的普遍适用性。
参与者(Participants)
纳入标准(Inclusion Criteria):年龄≥18岁,有组织学证实的恶性肿瘤,放射学证据显示至少有一个骨转移,预期寿命超过6个月,东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)表现状态(performance status)≤2。
排除标准(Exclusion Criteria):明确的血液肿瘤病史或其他不适合本研究的医疗条件。
干预措施(Interventions)
治疗分配(Treatment Allocation):参与者1:1随机分配接受MW032或参考药物denosumab,通过皮下注射(subcutaneously)给药,每4周一次,直到第49周。
主要和次要终点(Main and Secondary Endpoints)
主要终点(Primary Endpoint):基线到第13周尿液N-端肽/肌酐比率(urinary N-telopeptide/creatinine ratio, uNTx/uCr)的自然对数转换后的百分比变化。
次要终点(Secondary Endpoints):包括uNTx/uCr和骨特异性碱性磷酸酶(bone-specific alkaline phosphatase, s-BALP)从基线到第5、25、37和53周的百分比变化,以及SREs的发生率。
安全性和药代动力学评估(Safety and Pharmacokinetics Assessments)
安全性监测(Safety Monitoring):根据国家癌症研究所(NCI)的普通术语标准(Common Terminology Criteria for Adverse Events, CTCAE)版本5.0评估不良事件的发生率和严重性。
药代动力学(Population Pharmacokinetics):通过分析血药浓度和其他药动学参数来评估MW032与denosumab的相似性。
Advancements
疗效(Efficacy)结果
主要终点(Main Endpoint):MW032组和denosumab组在基线到第13周的尿液N-端肽/肌酐比率(urinary N-telopeptide/creatinine ratio, uNTx/uCr)的百分比变化上显示出相似的结果。两个治疗组的平均变化率分别为-72.0%和-72.7%,这表明两种药物在抑制骨转换(bone turnover)方面具有相似的效力。
次要终点(Secondary Endpoints):uNTx/uCr和骨特异性碱性磷酸酶(bone-specific alkaline phosphatase, s-BALP)的变化也显示出两种治疗之间没有显著差异,进一步证明了MW032与denosumab在治疗期间具有类似的作用机制和效果。
安全性(Safety)结果
不良事件(Adverse Events, AEs):MW032和denosumab的安全性概况相似,两组中报告的治疗相关不良事件的类型和频率没有显著差异。最常见的不良事件包括低钙血症(hypocalcemia)、低磷血症(hypophosphatemia)和高尿酸血症(hyperuricemia)。
严重不良事件(Serious Adverse Events, SAEs):两种治疗组中严重不良事件的发生率也相似,没有发现新的安全性问题或不良反应模式。
人群药代动力学(Population Pharmacokinetics)结果
药代动力学参数(Pharmacokinetic Parameters):MW032与denosumab在主要药代动力学参数,如最大血药浓度(Cmax)、药物暴露度(area under the curve, AUC)等方面表现出相似性。这些结果支持了MW032在体内的行为与denosumab相似,说明其可能具有相似的作用机制和效果。
骨相关事件(Skeletal-Related Events, SREs)结果
SREs发生率:在研究期间,MW032组和denosumab组的骨相关事件发生率相似,进一步证实了MW032在预防骨相关并发症方面与denosumab具有相似的效力。
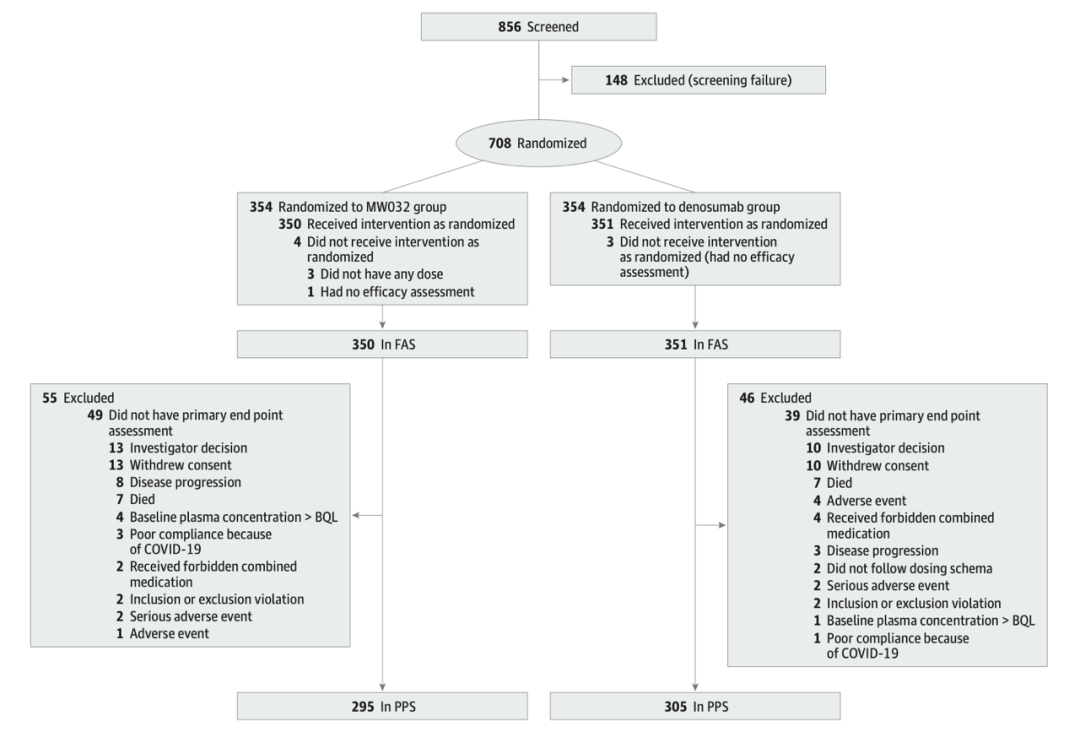
试验流程图(Credit: JAMA ONCOLOGY)
Prospects
长期疗效和安全性:研究期限为53周,对于评估长期疗效和安全性而言可能仍不充分。长期跟踪研究能够提供更多关于持续使用MW032后可能出现的不良反应或疗效持续性的信息。
特定人群的效果:研究中虽然包含了不同类型实体瘤的患者,但对于某些特定人群,如不同肿瘤亚型、不同遗传背景或具有特定并发症的患者,MW032的效果可能需要进一步评估。
与其他治疗方法的比较:除了与denosumab的直接比较外,未来研究中MW032与其他骨转移治疗方案,如双磷酸盐(bisphosphonates)等的比较,将有助于更全面地评估其在综合治疗策略中的地位。
经济性评估:虽然生物仿制药的开发旨在降低治疗成本,但关于MW032在实际医疗环境中的经济性评估,包括成本效益分析(cost-effectiveness analysis)和预算影响分析(budget impact analysis),仍需进一步研究。
生物标志物的应用:研究中使用了尿液N-端肽/肌酐比率(uNTx/uCr)作为主要疗效评估指标,未来研究可以探讨更多潜在的生物标志物,以便更精确地监测治疗效果和早期预测疗效。
不同治疗间隔和剂量的效果:研究中采用了每4周一次的给药方案,未来研究可以探索不同的治疗间隔和剂量对疗效和安全性的影响,以寻找最优化的治疗方案。
原文链接
https://jamanetwork.com/journals/jamaoncology/fullarticle/2814859
Zhang S, Yin Y, Xiong H, Wang J, Liu H, Lu J, Zhang Q, Zhang L, Zhong J, Nie J, Lei K, Wang H, Yang S, Yao H, Wu H, Yu D, Ji X, Zhang H, Wu F, Xie W, Li W, Yao W, Zhong D, Sun H, Sun T, Guo Z, Wang R, Guo Y, Yu Z, Li D, Jin H, Song H, Chen X, Ma W, Hu Z, Liu D, Guo Y, Tang J, Jiang Z. Efficacy, Safety, and Population Pharmacokinetics of MW032 Compared With Denosumab for Solid Tumor-Related Bone Metastases: A Randomized, Double-Blind, Phase 3 Equivalence Trial. JAMA Oncol. 2024 Feb 8:e236520. doi: 10.1001/jamaoncol.2023.6520. Epub ahead of print. PMID: 38329745; PMCID: PMC10853867.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















学到了
18
#实体瘤# #骨转移# #Denosumab# #MW032#
22