“绘”解读真报告丨胃肠间质瘤患者检出NTRK3融合,实体瘤1299基因助力临床诊疗
2024-01-22 苏州绘真医学 苏州绘真医学 发表于陕西省
近期,我司实体瘤1299基因为一位病理诊断为胃间质瘤的患者检出ETV6-NTRK3融合变异,参考指南和临床研究,为患者的诊治提供了诸多信息。
胃肠间质瘤(GIST)按分子病理亚型分为KIT/PDGFRA突变型和野生型,野生型GIST是指病理诊断符合GIST,但不携带KIT/PDGFRA基因突变。据统计,约85%儿童GIST和10%-15%成人GIST为野生型GIST。
2023 CSCO指南中对于经典型/继发耐药型GIST患者,II级推荐NGS检测;对于野生型GIST患者,NGS则由原先II级推荐前移至I级推荐,同时明确,NGS检测基因突变包括KIT、PDGFRA、SDH(A/B/C/D)、BRAF、NF1、KRAS和PIK3CA,检测基因重排包括FGFR1、NTRK3和BRAF基因(图1)。因此,基因检测作为指南推荐的策略,能够为GIST患者提供更多的分型判读和治疗指导。
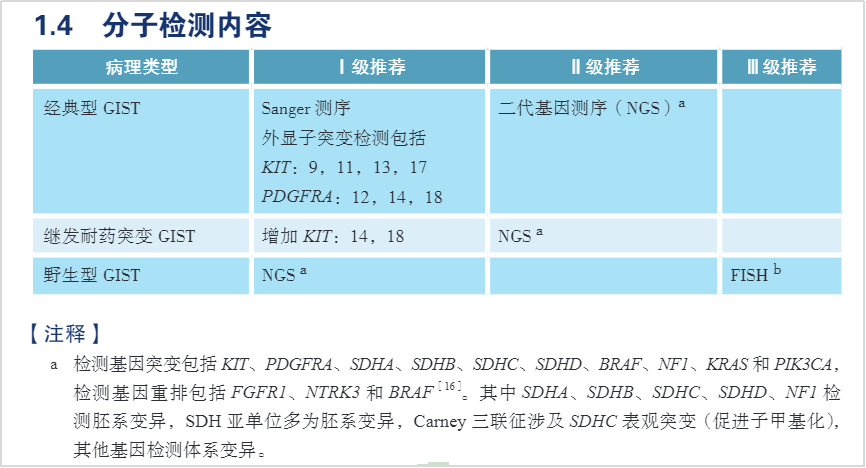
图1 摘自2023版CSCO胃肠间质瘤诊疗指南
近期,我司实体瘤1299基因为一位病理诊断为胃间质瘤的患者检出ETV6-NTRK3融合变异,参考指南和临床研究,为患者的诊治提供了诸多信息。
案 例
患者信息:男、66岁
临床诊断:胃体大弯侧间质瘤(图2)
送检样本:石蜡切片+血液
检测项目:实体瘤1299基因检测
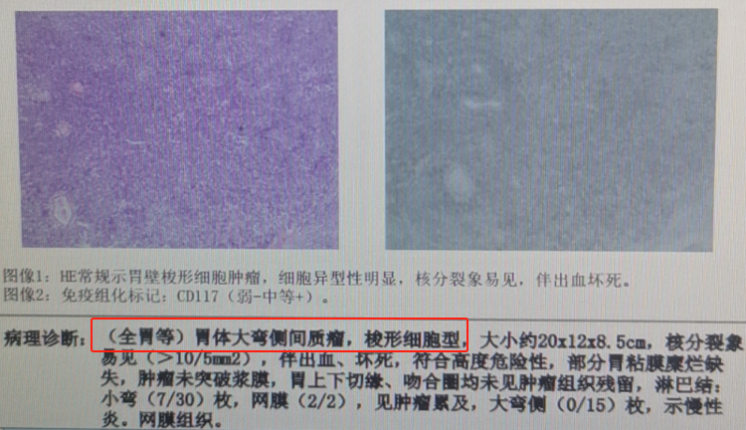
图2 患者病理报告

图3 患者报告检出ETV6-NTRK3融合
本次,GIST患者样本中检出ETV6(exon5)和NTRK3(exon14)基因发生融合(图3),形成ETV6-NTRK3融合形式,突变丰度为35.11%。该融合会导致配体非依赖的二聚化,保留了ETV6的PNT结构域和NTRK3激酶结构域,形成融合蛋白(图4),结构性激活细胞转化表达、促进肿瘤发生和发展。
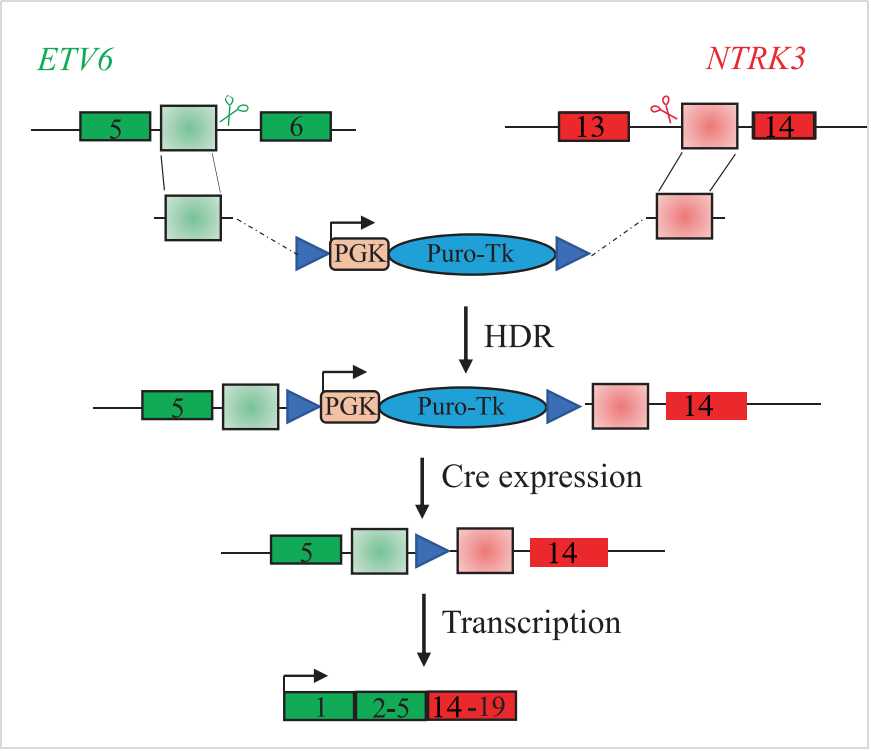
图4 本案例患者检出的ETV6-NTRK3融合图示
NTRK融合高发的癌种和人群有哪些?
据统计,目前已经在肿瘤中鉴定出超过80种NTRK(含NTRK1/2/3)融合的伴侣基因,主要包括ETV6、TPM3、TPR、STRN、LMNA、SQSTM1等(图5)。本案例患者检出的ETV6-NTRK3融合是NTRK3融合最常见的亚型,并且遍布于各个实体肿瘤,理应成为基因检测的重点关注。
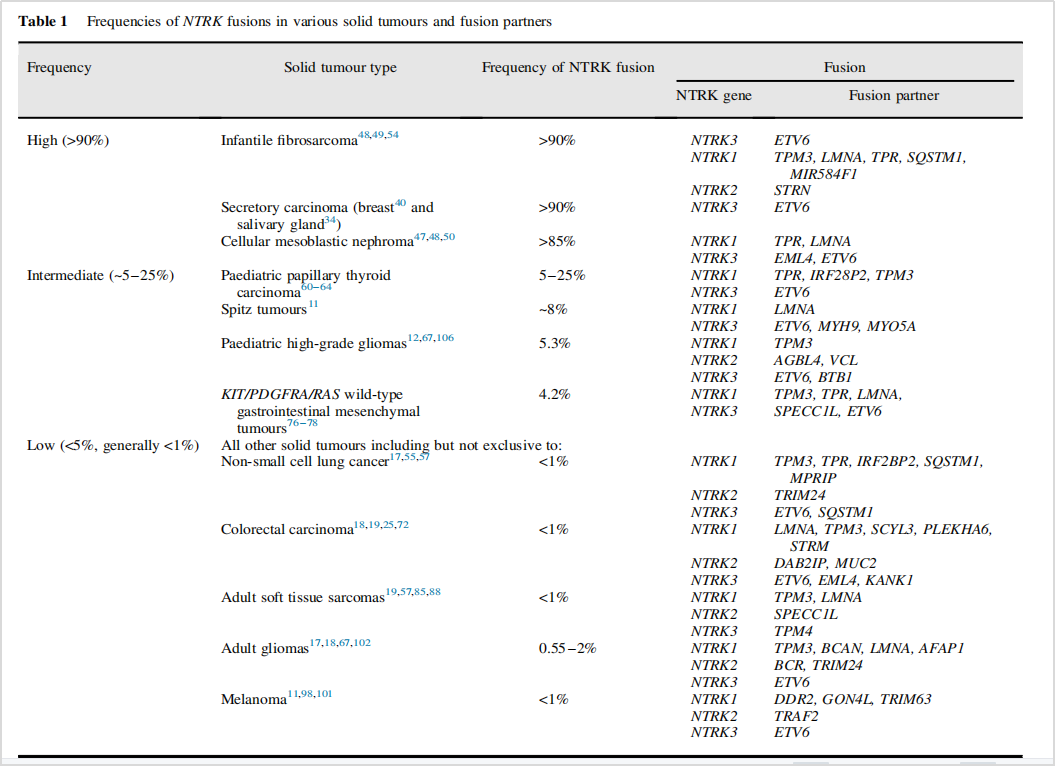
图5 NTRK与不同伴侣融合的发生情况
关于NTRK融合高发癌种,关注国内,2023年北京大学肿瘤医院发表在International Journal of Cancer上的临床研究,涵盖15种实体瘤67883例中国患者的数据[1]。总结NTRK1/2/3融合的整体发生率为0.18%,癌肿发生比例上,依次是黑色素瘤(1.64%)、肉瘤(0.82%)、神经内分泌肿瘤(0.72%)、甲状腺癌(0.69%)、结直肠癌(0.33%)等(图6)。在纳入的414例GIST患者中,NTRK融合检出率为0.24%,均为NTRK1融合。在突变谱上,NTRK融合阳性患者与驱动基因变异共发生的概率显著更低(46% vs 60%),但阳性患者伴随MSI-H比例显著更高(19.4% vs 2.4%),提示免疫治疗可能是NTRK融合患者后续关注的治疗方案。
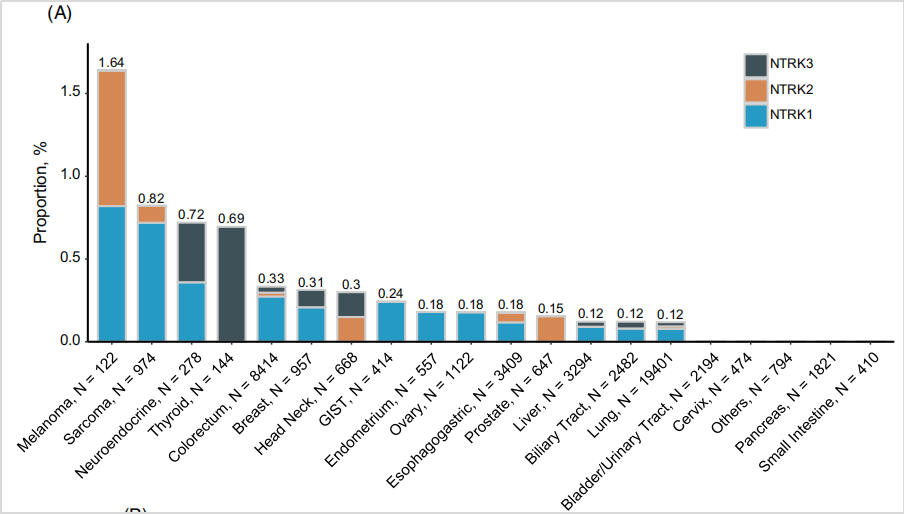
图6 不同实体瘤检出NTRK融合阳性率
放眼国外,2021年发表在npj Precision Oncology上的大样本(>29.5万例,FoundationCORE database)数据显示(图7)[2],NTRK融合阳性肿瘤在45种实体瘤中发生率为0.30%。在不同年龄段患者人群中,NTRK融合发生率存在较大差异,在年龄≥18岁和年龄<18岁人群中发生率分别为0.28%和1.34%,尤其在年龄<5岁患儿中的发生率最高(2.28%)。所以,儿童肿瘤患者中的整体发生率显著高于成人患者,且好发于年龄越小的人群。另外,在NTRK融合的癌种中,以唾液腺肿瘤,甲状腺癌,软组织肉瘤以及GIST为高发癌种,GIST患者NTRK融合的发生率为0.55%,而在所有NTRK融合的患者中,GIST患者比例占1%,这也是由于GIST发病罕见导致。由此可见,NTRK融合在实体肿瘤中的发生率,国内外的数据出现了大同小异的区别!
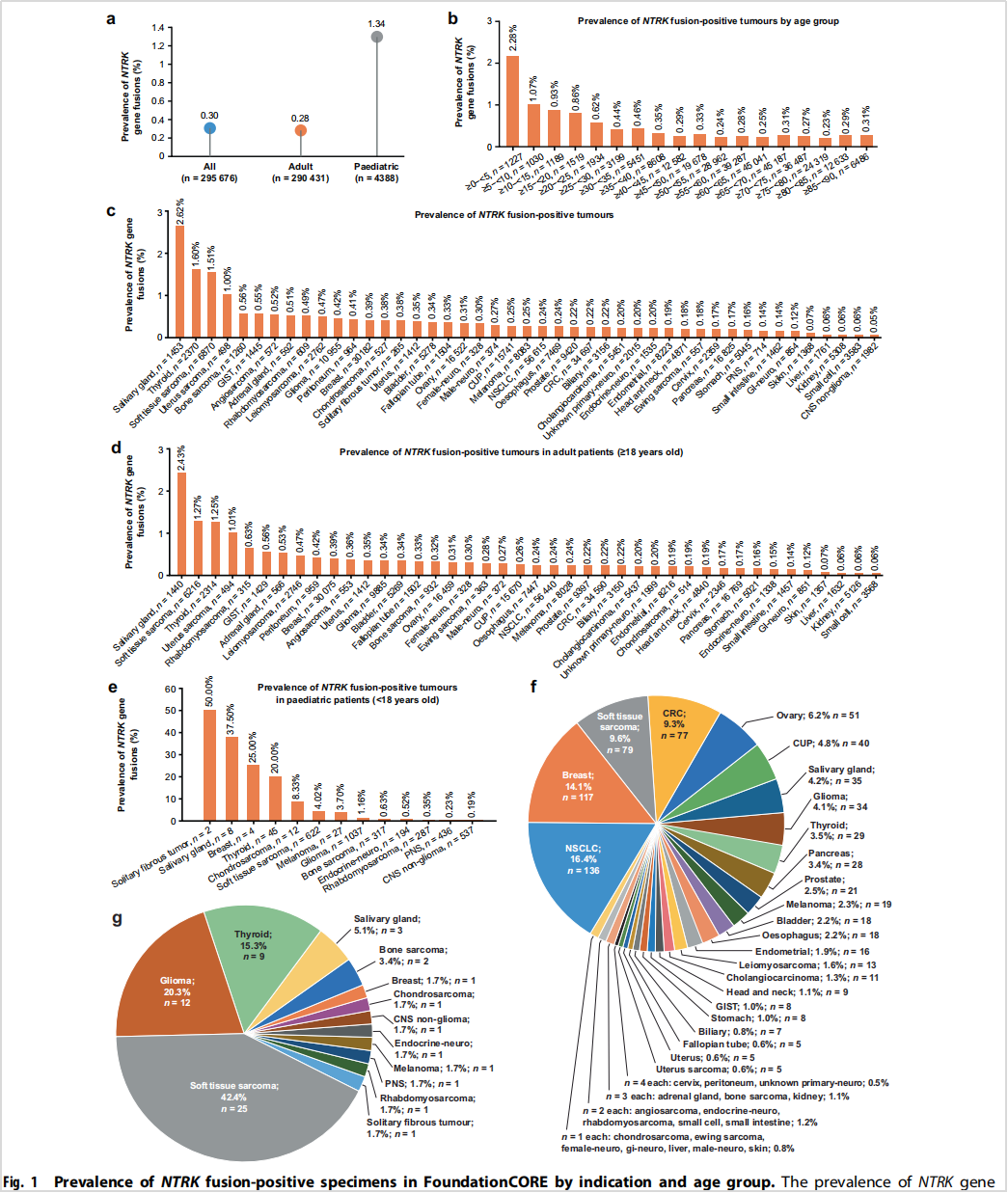
图7 NTRK融合阳性患者数据分析
(a)整体、成人和儿童患者的发生率;(b)按年龄分组的NTRK融合阳性率;(c)所有患者阳性率;(d)成年患者阳性率;(e)儿童患者阳性率;(f)NTRK融合阳性成人患者癌症类型分析;(g)NTRK融合阳性儿童患者癌症类型分析
NTRK3融合的GIST患者有什么病理特征?
本次GIST患者检出ETV6-NTRK3融合变异,我们聚焦于NTRK融合GIST患者的病理探究,为患者提供更多的肿瘤信息参考。2022年,天津市肿瘤医院在cancers上公布研究结果[3],研究通过使用IHC初筛、NGS检测和FISH验证在46例野生型GIST样本中筛选出2例ETV6-NTRK3融合GIST,另结合文献报道的其他10个案例,总结了NTRK融合GIST的临床病理学特征(图8):NTRK融合型GIST常见于肠道(75%),包括直肠、十二指肠、空肠、结肠、小肠和肠系膜,其次是胃(16.7%),携带NTRK3融合比NTRK1融合在GIST中更多见。在这些患者的组织学上,上皮样细胞型最常见(60%),其次是梭形细胞型(20%)和混合型(20%),并且往往肿瘤体积较大。此外,在风险可评的9例患者中,大多数(8/9,88.9%)具有NTRK 重排的GIST具有较高的复发和转移风险,只有1例患者评估为低风险 。这也从肿瘤的病理的角度提示本案例患者应注意后续肿瘤的高度侵袭性,在做好治疗的同时,务必密切关注肿瘤进展和转移的风险,做更合理的临床管理!
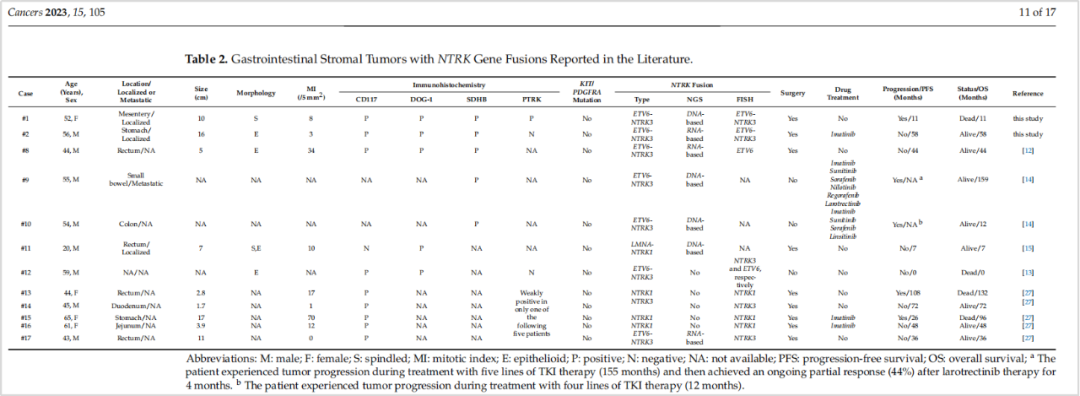
图8 文献中报道的NTRK基因融合的GIST
NTRK3融合患者如何考虑后续靶向治疗方案?
现阶段,得益于伊马替尼、阿伐替尼等靶向药物的研发,KIT和PDGFRA突变型GIST患者能够获益于靶向治疗,药物可及性高。而在突变型GIST之外,深受指南推荐的BRAF、NTRK、NF1等多个基因也为野生型GIST提供了获批的靶向治疗,尤其是该患者检出的NTRK3融合变异。
在新版GIST CSCO指南中明确,早在新辅助治疗开始前,就建议病理活检明确诊断,推荐行基因检测,评估患者可能获益的治疗方案(图9)。对于NTRK融合患者,拉罗替尼可以考虑作为新辅助治疗或者转移性GIST患者一线治疗的方案(III级),一项拉罗替尼治疗NTRK融合实体瘤研究中,入组的NTRK融合胃肠间质瘤患者全部显示显著的肿瘤退缩[4]。NEJM(The New England Journal of Medicine)期刊发表的临床研究纳入了55例NTRK融合实体瘤患者[5],经拉罗替尼治疗,总缓解率高达75%,其中22%的患者完全缓解!其中,2例携带ETV6-NTRK3的GIST患者获得缓解。
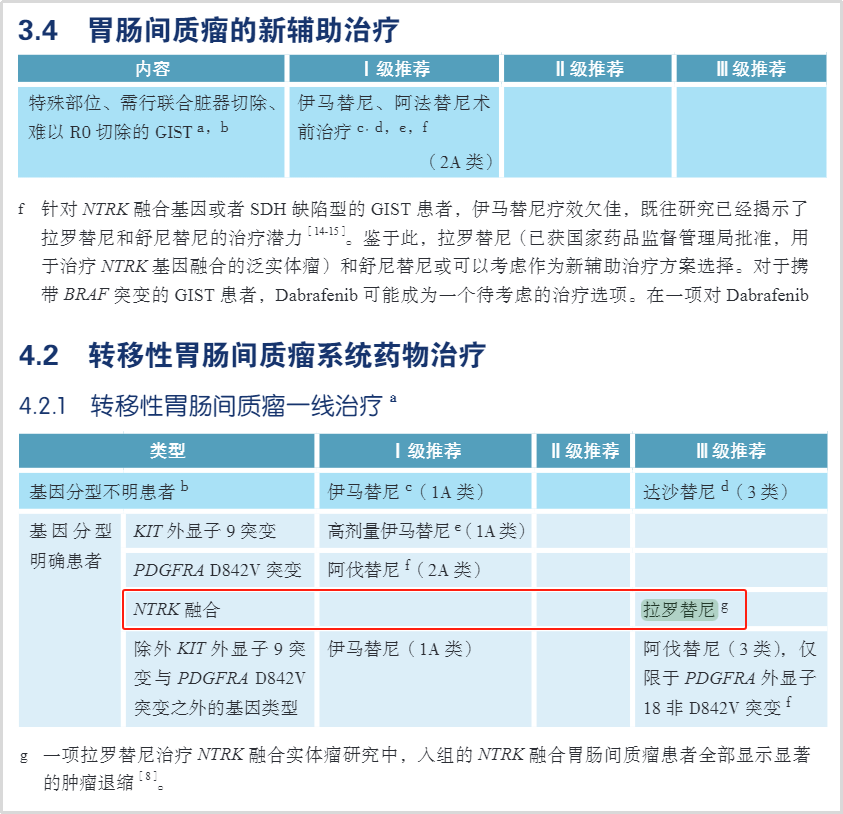
图9 GIST CSCO指南对于新辅助治疗和一线治疗的推荐
同样,在最新版的NCCN指南中关于拉罗替尼的适应症推荐与CSCO指南一致。除此之外,参考临床研究数据[6],在19名不同实体瘤类型的患者中,恩曲替尼的总体反应率(ORR)为57.4%,其中7% 的患者肿瘤全部消失,达到完全缓解(CR),还有45%的患者获得了超过一年的持久反应。针对NTRK融合的GIST患者(图10),NCCN指南在拉罗替尼之余,又增加了恩曲替尼的推荐。同时,指南还推荐BRAF V600E(达拉非尼+曲美替尼)、SDH缺陷(舒尼替尼、瑞戈非尼、培唑帕尼等)等基因检测匹配药物指导,并提倡NGS多基因方法学检测。

图10 NCCN指南关于GIST的检测和推荐
值得强调的是,伴随着2023年国家医保报销目录的公布,在NTRK融合的实体瘤中,新增了恩曲替尼的报销适应症:用于12岁及以上,携带NTRK融合,患有局部晚期、转移性疾病或手术切除可能导致严重并发症的患者,或无满意替代治疗或既往治疗失败的患者。
总结来说,该患者通过本次全面的NGS基因检测检出ETV6-NTRK3融合,不但明确了指南推荐且获批于监管机构的靶向药物,而且提供了获益于国家医保政策的可能,为患者带来了诸多希望!
共识如何推荐NTRK基因融合检测?
近年来,随着NTRK融合靶向药物拉罗替尼,恩曲替尼的上市,涌现出多篇NTRK融合检测的指南和共识,强调了NTRK融合在实体瘤中的检测价值和方法学应用。
在《拉罗替尼治疗TRK融合儿童肿瘤中国专家共识》中提到[7],可选择用于NTRK基因融合检测的方法有免疫组织化学(IHC)、荧光原位杂交(FISH)、逆转录聚合酶链反应(RT-PCR)和二代测序(NGS)。共识总结了不同方法学的特点(图10),简要总结:FISH检测技术已十分成熟,但需要组织或细胞学标本,且只能检测一种融合类型。RT-PCR也只适用于检测已知的融合,对样本质量要求较高。IHC检测成本低,但经证实准确性的抗体依赖性强,特异性不佳,可作为初筛手段。而NGS检测具有较高的灵敏性和特异性,可同时分析NTRK融合和位点变异等多种已知或未知变异,适用于组织和血液,尤其是RNA和DNA层面的双组学检测更为全面,但RNA-NGS对样本质量要求高。
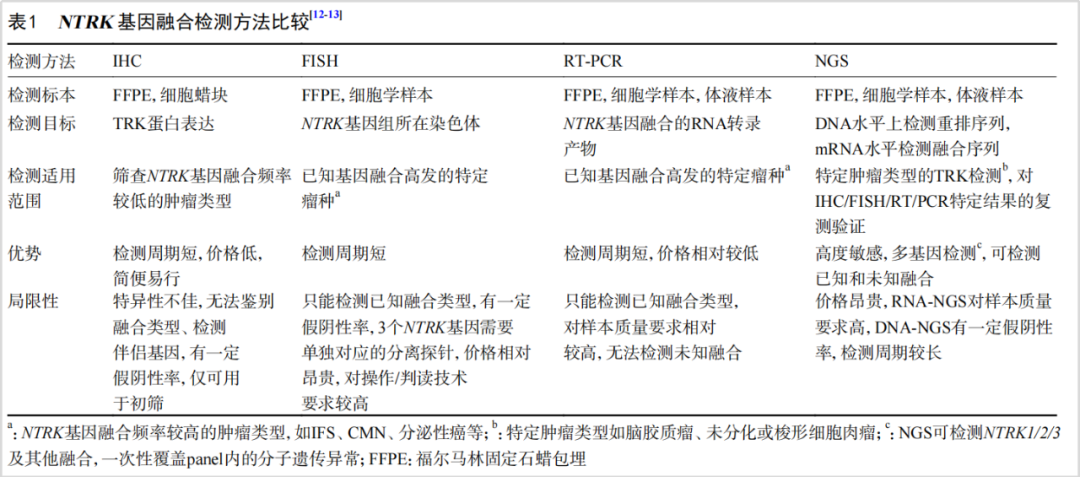
图11 摘自《拉罗替尼治疗TRK融合儿童肿瘤中国专家共识》
另外,由中国科学院基础医学与肿瘤研究所领衔38家医院颁布的《中国实体瘤NTRK融合基因临床诊疗专家共识》中给予了NTRK融合检测较为全面的建议(图12)[8]:

图12 摘自《中国实体瘤NTRK融合基因临床诊疗专家共识》部分
何时检测?在共识中强烈推荐所有晚期成人实体瘤和儿童实体瘤患者进行NTRK融合基因检测,NTRK基因融合发生率高的局部晚期肿瘤患者应提早在新辅助治疗前进行检测,并且根据不同癌种的特性采取不同的检测策略。
如何检测?强烈建议使用覆盖NTRK基因内含子区域的NGS DNA panel或者全外显子组检测作为NTRK融合检测的首要手段。NGS RNA panel比 DNA NGS panel具有更高的灵敏性,尤其在IHC呈阳性DNA NGS panel检测阴性的情况下,建议RNA NGS panel或者转录组作为NTRK融合检测的补充手段。在条件允许的情况下,推荐同时提取FFPE切片的DNA和RNA,以实现DNA和RNA同步测序。
本次为患者检测的实体瘤1299基因就覆盖了NTRK1/2/3 CDS编码区和部分融合断点的内含子序列,正是共识中首推的NTRK检测手段。共识还提到,NTRK基因FISH检测可以作为NTRK融合基因发生率高的肿瘤的确诊手段,其他类型实体瘤则不建议。基于免疫组化平台的pan-TRK检测可以作为NTRK融合基因发生率较低、NTRK基因不表达且常规条件下不推荐NGS DNA panel方法的癌种初筛方法,也可以作为NGS检测手段的复核手段。
结合共识,我司基于NGS方法学,提供多种覆盖NTRK融合检测的实体肿瘤项目,不仅检测NTRK不同变异,还满足多基因检测的需求。另外,还有来自FISH平台的单项NTRK1/2/3基因融合断裂检测,以及IHC平台的pan-TRK蛋白表达检测,方便临床依需选择,旨在为患者提供全方位的检测服务(图13)。
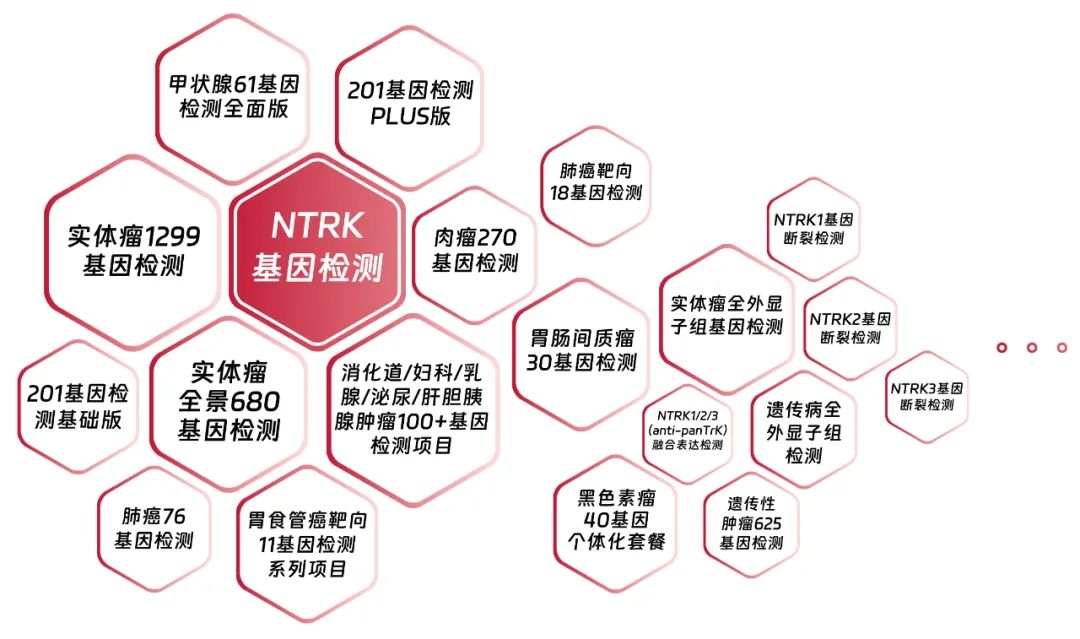
图13 绘真医学NTRK基因检测相关产品线
参考文献:
[1]Qi C, Zhou T, Bai Y, et al. China special issue on gastrointestinal tumor-NTRK fusion in a large real-world population and clinical utility of circulating tumor DNA genotyping to guide TRK inhibitor treatment [published online ahead of print, 2023 Mar 22]. Int J Cancer. 2023;10.1002/ijc.34522. doi:10.1002/ijc.34522
[2]Westphalen CB, Krebs MG, Le Tourneau C, Sokol ES, Maund SL, Wilson TR, Jin DX, Newberg JY, Fabrizio D, Veronese L, Thomas M, de Braud F. Genomic context of NTRK1/2/3 fusion-positive tumours from a large real-world population. NPJ Precis Oncol. 2021 Jul 20;5(1):69. doi: 10.1038/s41698-021-00206-y. Erratum in: NPJ Precis Oncol. 2021 Sep 17;5(1):86. PMID: 34285332; PMCID: PMC8292342.
[3]Cao Z, Li J, Sun L, Xu Z, Ke Y, Shao B, Guo Y, Sun Y. GISTs with NTRK Gene Fusions: A Clinicopathological, Immunophenotypic, and Molecular Study. Cancers (Basel). 2022 Dec 23;15(1):105. doi: 10.3390/cancers15010105. PMID: 36612101; PMCID: PMC9817796.
[4]LAETSCH TW, DUBOIS SG, MASCARENHAS L, et al. Larotrectinib for paediatric solid tumours harbouring NTRK gene fusions: Phase 1 results from a multicentre, open-label, phase 1/2 study. Lancet Oncol, 2018, 19 (5): 705-714.
[5]Drilon A, Laetsch TW, Kummar S, DuBois SG, Lassen UN, Demetri GD, Nathenson M, Doebele RC, Farago AF, Pappo AS, Turpin B, Dowlati A, Brose MS, Mascarenhas L, Federman N, Berlin J, El-Deiry WS, Baik C, Deeken J, Boni V, Nagasubramanian R, Taylor M, Rudzinski ER, Meric-Bernstam F, Sohal DPS, Ma PC, Raez LE, Hechtman JF, Benayed R, Ladanyi M, Tuch BB, Ebata K, Cruickshank S, Ku NC, Cox MC, Hawkins DS, Hong DS, Hyman DM. Efficacy of Larotrectinib in TRK Fusion-Positive Cancers in Adults and Children. N Engl J Med. 2018 Feb 22;378(8):731-739. doi: 10.1056/NEJMoa1714448. PMID: 29466156; PMCID: PMC5857389.
[6]Doebele RC, Drilon A, Paz-Ares L, Siena S, Shaw AT, Farago AF, Blakely CM, Seto T, Cho BC, Tosi D, Besse B, Chawla SP, Bazhenova L, Krauss JC, Chae YK, Barve M, Garrido-Laguna I, Liu SV, Conkling P, John T, Fakih M, Sigal D, Loong HH, Buchschacher GL Jr, Garrido P, Nieva J, Steuer C, Overbeck TR, Bowles DW, Fox E, Riehl T, Chow-Maneval E, Simmons B, Cui N, Johnson A, Eng S, Wilson TR, Demetri GD; trial investigators. Entrectinib in patients with advanced or metastatic NTRK fusion-positive solid tumours: integrated analysis of three phase 1-2 trials. Lancet Oncol. 2020 Feb;21(2):271-282. doi: 10.1016/S1470-2045(19)30691-6. Epub 2019 Dec 11. Erratum in: Lancet Oncol. 2020 Feb;21(2):e70. Erratum in: Lancet Oncol. 2020 Jul;21(7):e341. Erratum in: Lancet Oncol. 2020 Aug;21(8):e372. Erratum in: Lancet Oncol. 2021 Oct;22(10):e428. PMID: 31838007; PMCID: PMC7461630.
[7]中国抗癌协会小儿肿瘤专业委员会, 中国研究型医院学会儿童肿瘤专业委员会. 拉罗替尼治疗TRK融合儿童肿瘤中国专家共识[J]. 中国肿瘤临床, 2023, 50(17): 865-872. doi: 10.12354/j.issn.1000-8179.2023.20230698
[8]Xu C, Si L, Wang W, Li Z, Song Z, Wang Q, Liu A, Yu J, Fang W, Zhong W, Wang Z, Zhang Y, Liu J, Zhang S, Cai X, Liu A, Li W, Zhan P, Liu H, Lv T, Miao L, Min L, Chen Y, Yuan J, Wang F, Jiang Z, Lin G, Pu X, Lin R, Liu W, Rao C, Lv D, Yu Z, Lei L, Li X, Tang C, Zhou C, Zhang J, Xue J, Guo H, Chu Q, Meng R, Wu J, Zhang R, Hu X, Zhou J, Zhu Z, Li Y, Qiu H, Xia F, Lu Y, Chen X, Ge R, Dai E, Han Y, Pan W, Luo J, Jia H, Dong X, Pang F, Wang K, Wang L, Zhu Y, Xie Y, Lin X, Cai J, Wei J, Lan F, Feng H, Wang L, Du Y, Yao W, Shi X, Niu X, Yuan D, Yao Y, Huang J, Zhang Y, Sun P, Wang H, Ye M, Wang D, Wang Z, Wan B, Lv D, Wei Q, Kang J, Zhang J, Zhang C, Yu G, Ou J, Shi L, Li Z, Liu Z, Liu J, Yang N, Wu L, Wang H, Jin G, Yang L, Wang G, Fang M, Fang Y, Li Y, Wang X, Zhang Y, Ma S, Wang B, Zhang X, Song Y, Lu Y. Expert consensus on the diagnosis and treatment of NTRK gene fusion solid tumors in China. Thorac Cancer. 2022 Nov;13(21):3084-3097. doi: 10.1111/1759-7714.14644. Epub 2022 Sep 20. PMID: 36127731; PMCID: PMC9626341.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#实体瘤# #胃肠间质瘤# #NTRK3#
24