【JCO】Pirtobrutinib用于既往共价BTK抑制剂治疗的MCL的1-2期研究结果
2023-11-12 聊聊血液 聊聊血液 发表于上海
I/II 期 BRUIN 研究纳入复发难治B细胞肿瘤患者(包括既往过cBTKi 治疗的患者)纳入给予Pirtobrutinib单药治疗。
Pirtobrutinib治疗MCL
2023年10月16日,中国国家药监局药品审评中心官网公示,礼来公司Pirtobrutinib片的上市申请拟纳入优先审评,用于既往接受过BTK抑制剂治疗的复发或难治性套细胞淋巴瘤成人患者。
共价BTK抑制剂 (cBTKi) 改变了多种 B 细胞恶性肿瘤的治疗现状,包括复发性/难治性 (R/R)MCL,但其疗效受限于耐药性或不耐受。cBTKi 治疗后的R/R MCL患者历来结局极差,中位总生存期 (OS)不足10个月。CD19 CAR-T 细胞疗法扩大了 R/R MCL 的治疗选择,但使用受限,并非所有患者均合格,并且具有重度毒性。对于 cBTKi 治疗后的 MCL 患者,使用另一个cBTKi的疗效也不佳,因此对于有效、广泛可用和耐受良好的治疗仍存在显著未满足的医疗需求。
Pirtobrutinib 是一种高选择性、非共价(可逆)BTKi,可抑制野生型和 C481 突变型BTK,具有相同的低 nM 效力,并且具有良好的口服药理学,能够在每日一次给药间隔内持续抑制BTK,无论 BTK 转换的内在速率如何。
I/II 期 BRUIN 研究纳入复发难治B细胞肿瘤患者(包括既往过cBTKi 治疗的患者)纳入给予Pirtobrutinib单药治疗,《Journal of Clinical Oncology》近期报告了既往cBTKi 治疗的 MCL 患者的主要疗效和安全性分析结果。

研究结果
1-2期 BRUIN研究纳入复发性或难治性 B 细胞肿瘤患者接受Pirtobrutinib单药治疗,包括套细胞淋巴瘤、慢性淋巴细胞白血病/小淋巴细胞淋巴瘤、华氏巨球蛋白血症和边缘区淋巴瘤等,既往接受过cBTKi治疗的患者可入组。患者在1期部分或2期部分接受Pirtobrutinib单药治疗。在1期部分,患者接受Pirtobrutinib治疗的剂量范围为25-300 mg,每日一次,28天为一个周期。在 II 期部分,患者接受推荐剂量 200mg 每日一次
基线患者和疾病特征
共有164例 MCL 患者入组并接受Pirtobrutinib治疗,包括90例 cBTKi 既往治疗患者(主要疗效队列)和14例cBTKi-未暴露(naive)患者;未纳入疗效分析的另外60例 MCL 患者,要么没有无法进入主要疗效队列,要么随访不充分。主要疗效队列 (n=90) 中47%(n=42) 的患者使用 PET-CT 扫描进行缓解评估,其余患者仅通过 CT 扫描进行评估。在主要疗效队列的患者中,中位年龄为70岁,中位既往治疗线数为3,根据简化 MCL 国际预后指数评分,大多数患者 (77.8%,n=70)为中危或高危疾病(表1)。其他既往治疗包括抗 CD20 抗体 (95.6%,n=86)、化疗 (87.8%,n=79)、免疫调节剂(21.1%,n=19)、干细胞移植(21.1%,n=19;包括自体 [18.9%] 或异基因 [4.4%])、BCL-2抑制剂 (15.6%,n=14)、CAR-T细胞治疗 (4.4%,n=4) 和PI3K抑制剂 (3.3%,n=3)。大多数患者既往停用cBTKi的患者是因疾病进展 (82.2%,n=74),其次为毒性/不耐受 (17.8%,n=16)。6例患者 (6.7%) 既往仅接受过1线 BTKi 治疗,66例患者 (73.3%) 既往接受过1线 cBTKi 但也接受过其他类型既往治疗,18例患者 (20%) 既往接受过1线以上 cBTKi 治疗。
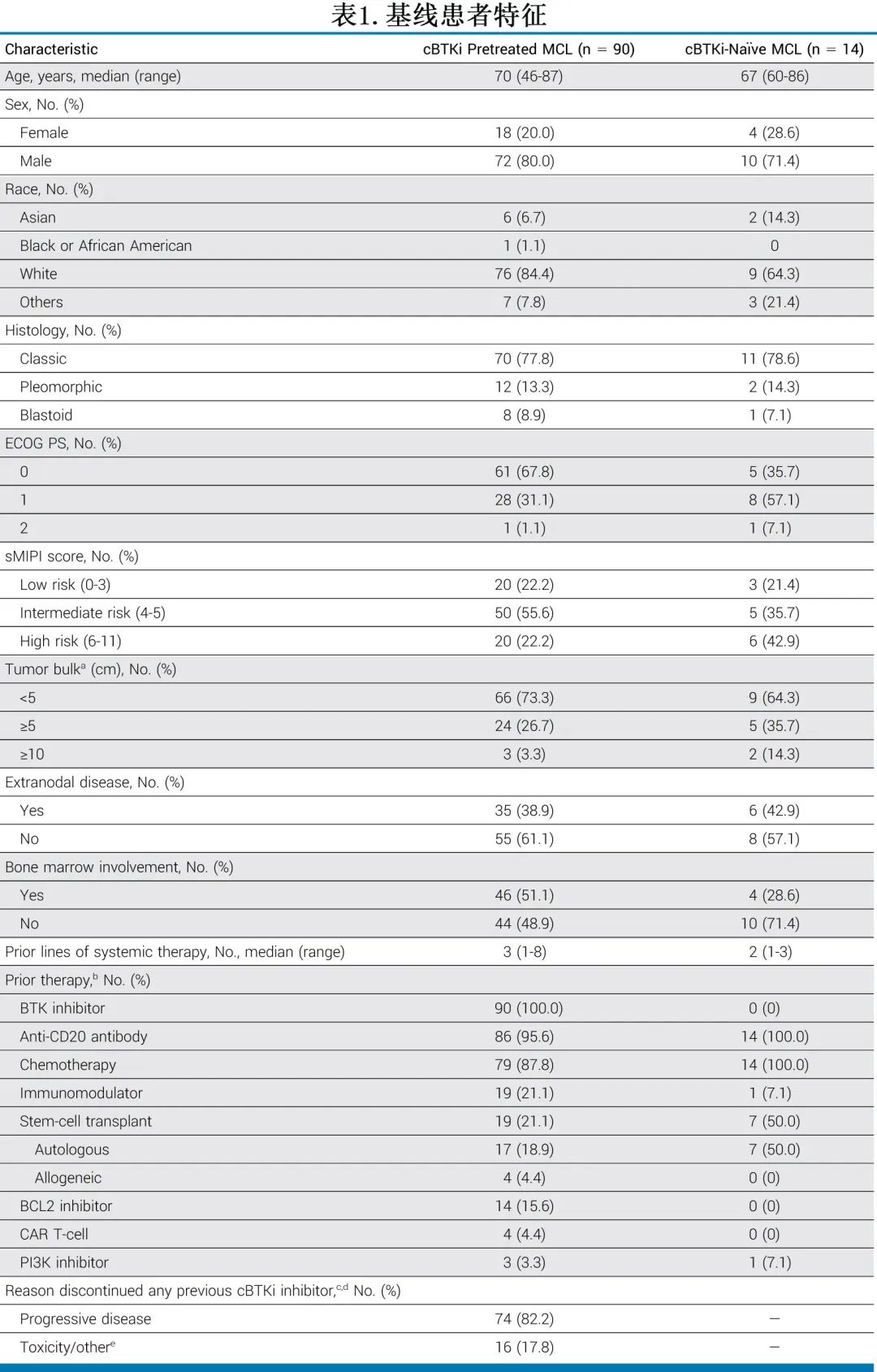
大多数患者 (n=79,87.8%) 以推荐的 II 期剂量 200 mg 每日一次接受至少一次Pirtobrutinib给药,77例 (85.6%) 患者以 200mg 每日一次作为起始剂量。治疗的中位时间为5.2个月,72例 (80.0%) 患者停止治疗,其中49例 (54.4%) 由于疾病进展,11例 (12.2%) 由于治疗中出现的不良事件(TEAE),其中3例 (3.3%) 被认为是治疗相关不良事件(体重减轻、胆囊炎和中性粒细胞计数降低),3例 (3.3%) 由于开始替代治疗,2例 (2.2%) 因为撤回知情同意,5例 (5.6%) 因为死亡,2例 (2.2%) 因为其他原因。14例cBTKi-未暴露 MCL 患者的基线特征见表1。
疗效
在主要疗效队列 (n=90) 中,独立审查委员会(IRC)确定的 ORR 为57.8%,包括20.0%(n=18) 完全缓解和37.8%(n=34) 部分缓解(表2;图1)。中位缓解时间为1.8个月。在母细胞样组织学 (n=8) 和多形性组织学 (n=12) 患者中,ORR分别为75.0%和50.0%。既往接受过 CAR-T 细胞治疗的4例患者中有2例获得缓解,既往接受过干细胞移植的19例患者的 ORR 为57.9%。ORR 在其他预先指定的亚组中基本一致,无论人口统计学、既往治疗线数或既往治疗。在既往接受过伊布替尼、阿可替尼或泽布替尼治疗的患者中,Pirtobrutinib的 ORR 相似。
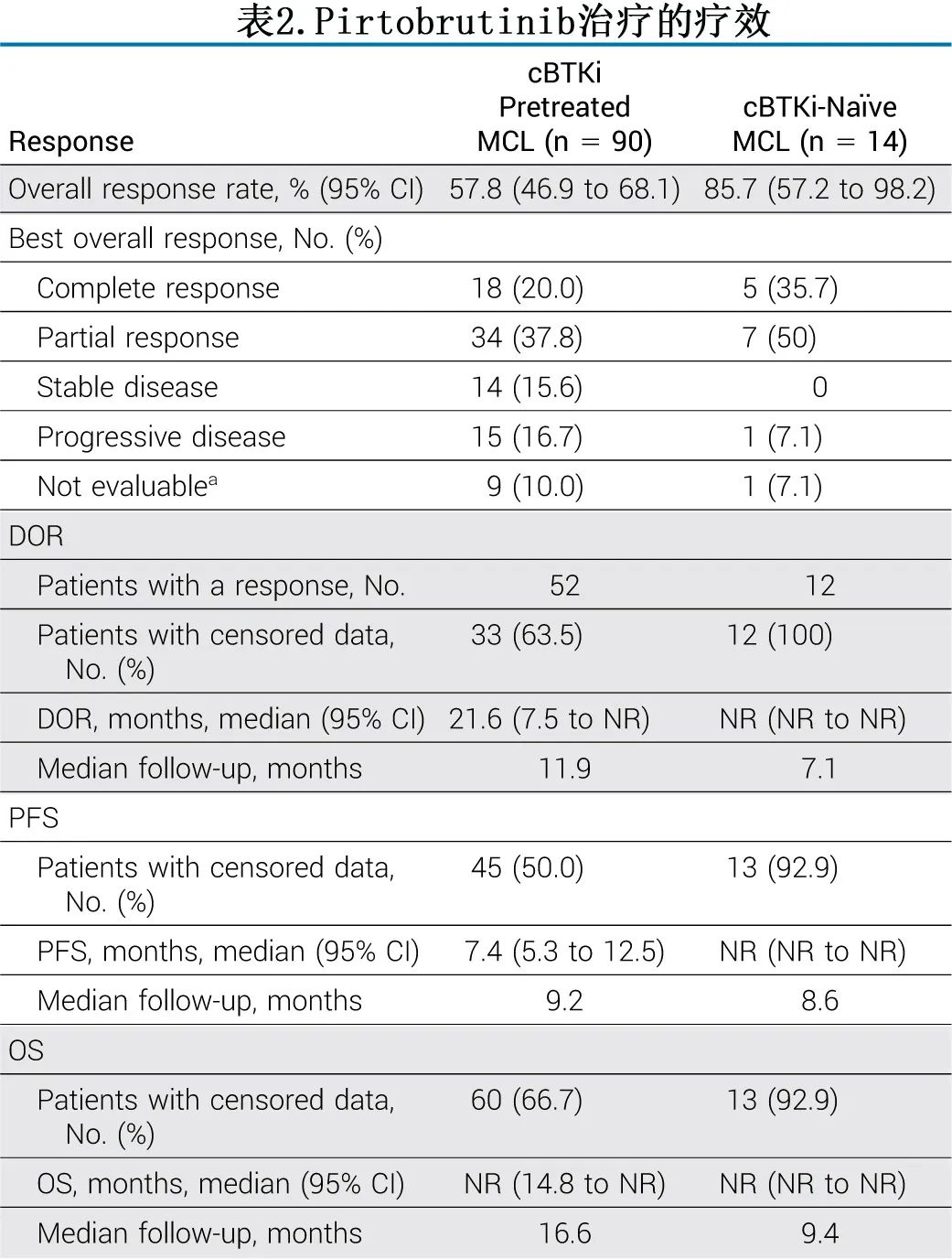
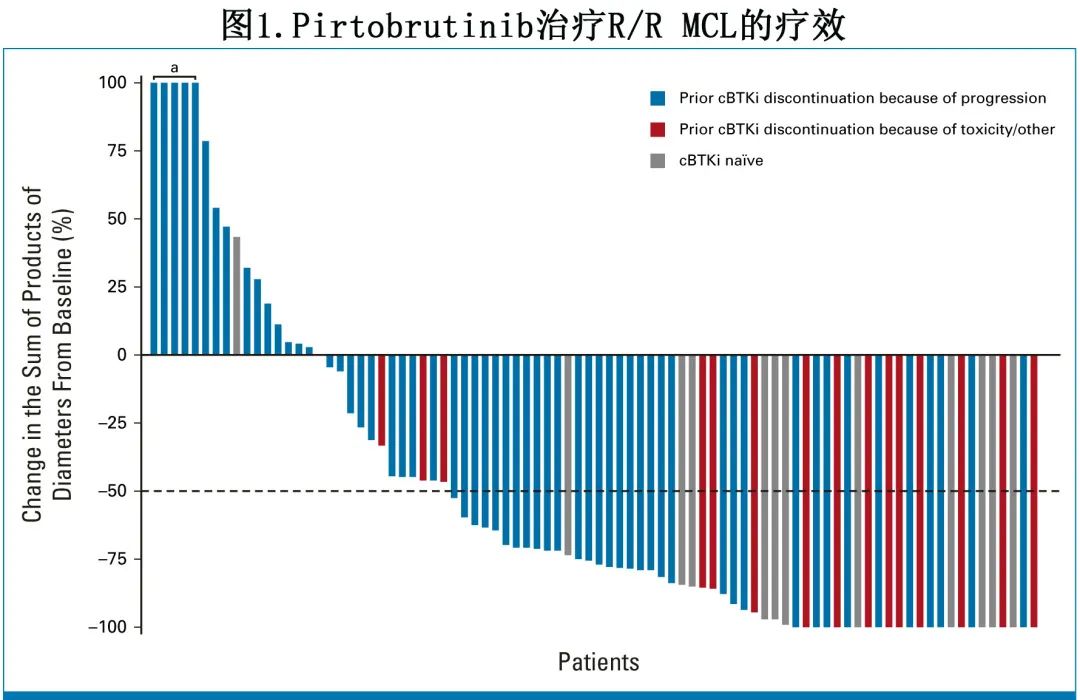
中位缓解随访12个月,52例缓解者中 IRC 评估的中位 DOR 为21.6个月(图2A;表2),6、12和18个月的估计 DOR 率分别为73.6%、57.1%和52.4%。在缓解患者中,35%的缓解在数据截止时仍在持续,最长持续缓解时间为26.2个月。BTKi 作为末线治疗线的患者 (n=55) 的中位 DOR 为14.8个月,ORR为52.7%。IRC 评估的中位 PFS 为7.4个月(图2B;表2)。中位 OS 为未达到(图2C;表2),12个月和18个月的估计 OS 率分别为67.6%和59.3%。Pirtobrutinib治疗后,17例 (18.9%) 患者接受后续 CAR-T 细胞治疗。
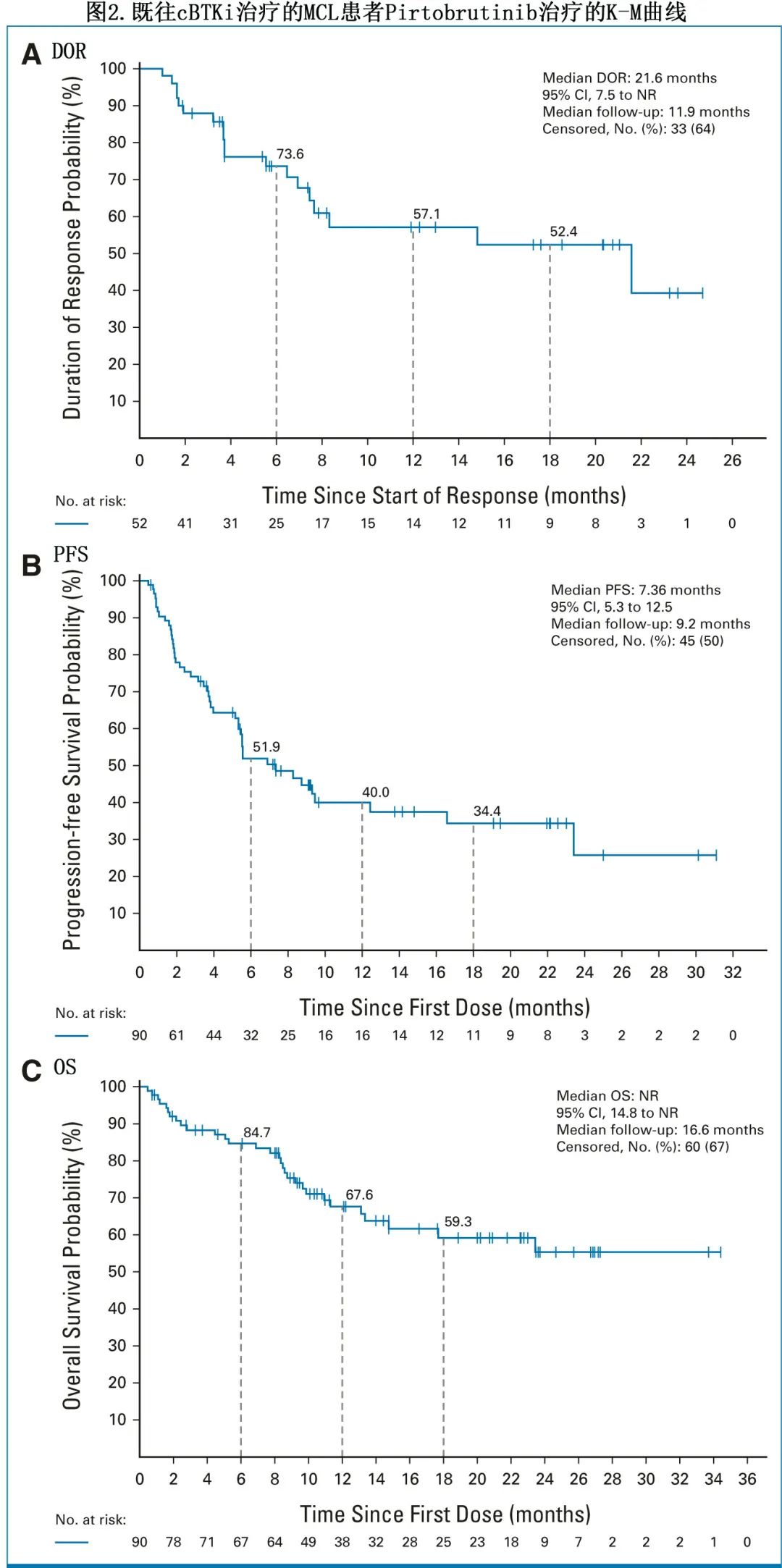
根据IRC,14例cBTKi-未暴露患者的 ORR 为85.7%,其中完全缓解率为35.7%(5/14),部分缓解率为50.0%(7/14)(表2;图1)。中位随访7.1个月,中位 DOR 为NR(表2)。6个月的估计 DOR 率为100%。未达到中位 PFS 和OS(表2),6个月时PFS和 OS 率均为92.3%。
因疾病进展而中止既往 cBTKi 治疗的患者 (n=74) 的 ORR 为50%(n=37),中位 DOR 为14.8个月,中位 PFS 为5.5个月,中位 OS 为23.4个月。因毒性中止既往 BTKi 治疗的患者 (n=12) 的 ORR 为92%(n=11),中位DOR、中位 PFS 和中位OS均无法评估,12个月率分别为78.8%、82.5%和91.7%。
安全性
截至数据截止日期,在接受Pirtobrutinib治疗的164例 MCL 患者中,92.1%的患者接受了至少一剂Pirtobrutinib,推荐的 II 期剂量为200mg每日一次。中位治疗时间为4.5个月。最常见的 TEAE 和特别关注的 AE 见表3。不考虑因果关系,最常见的 TEAE 为疲乏 (29.9%,n=49)、腹泻 (21.3%,n=35) 和呼吸困难 (16.5%,n=27)。最常见的≥3级 TEAE 为感染 (17.1%,n=28)。
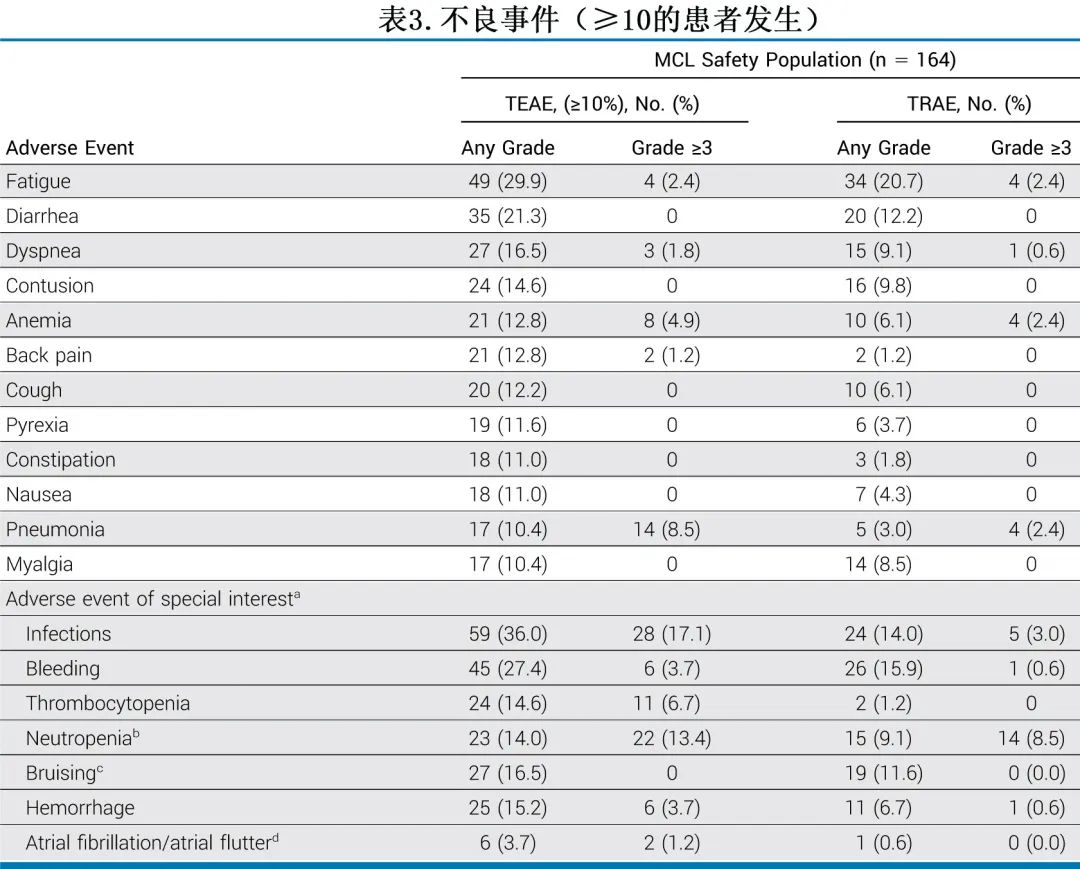
≥3级Pirtobrutinib相关 AE 不常见,其中中性粒细胞减少 (8.5%,n=14) 最常见;未观察到≥3级高血压TEAE。房颤/房扑不常见,见于6例 (3.7%) 患者,其中3例有房颤病史,但17例 (10.4%) 入组患者有房颤/房扑病史;仅2例房颤/房扑事件为≥3级,均未导致停用Pirtobrutinib。≥3级出血 TEAE 的发生率较低 (3.7%,n=6),无≥3级瘀伤事件(表3)。28例 (17.1%) 患者发生≥3级感染TEAE;最常见的任何等级感染为感染性肺炎 (10.4%,n = 17) 和 COVID-19 相关感染性肺炎 (3%,n=5);有8例 (4.9%) 患者记录了任何级别的 COVID-19 疾病。分别有42例 (25.6%) 和8例 (4.9%) 患者因AE导致给药中断和剂量降低。15例 (9.1%) 患者因 TEAE 永久停药,最常见的是肺炎 (n=2,1.2%),而其他事件均未导致1例以上停药。5例 (3.0%) 患者因药物相关不良事件永久停药。发生11起5级TEAE,研究者认为均与药物不相关(表3),但无法完全排除疗效。所有 MCL 患者 (n=164) 的安全性特征与总体人群一致,包括所有接受Pirtobrutinib治疗 B 细胞恶性肿瘤的患者 (n=725).
总结
I/II 期 BRUIN 研究纳入90例既往接受过cBTKi治疗的R/R MCL患者,患者的中位年龄为70岁,中位既往治疗线数为3,82.2%的患者由于疾病进展而停用既往cBTKi,77.8%的患者具有中危或高危简化 MCL 国际预后指数评分。ORR 为57.8%,包括20.0%的完全缓解 (n=18)。中位随访12个月,中位 DOR 为21.6个月,6个月和12个月估计 DOR 率分别为73.6%和57.1%。在 MCL 安全性队列 (n=164) 中,最常见的治疗中出现的不良事件 (TEAE) 为疲乏 (29.9%)、腹泻 (21.3%) 和呼吸困难 (16.5%)。≥3级出血 (3.7%) 和房颤/房扑 (1.2%)TEAE较少见。仅3%的患者因治疗相关不良事件而停用Pirtobrutinib。
Pirtobrutinib 是一种首创的新型非共价(可逆性)BTKi,也是首个在多线治疗(包括cBTKi 治疗)的 R/R MCL 患者中证实持久疗效的BTKi。Pirtobrutinib耐受性良好,因毒性导致的治疗中止率较低。多项临床试验正在评估Pirtobrutinib治疗 B 细胞恶性肿瘤,包括一项在经治但BTKi未暴露的MCL患者中比较Pirtobrutinib与研究者选择的 cBTKi 的随机化、全球、III期研究(NCT04662255)。
参考文献
Wang M,et al. Pirtobrutinib in Covalent Bruton Tyrosine Kinase Inhibitor Pretreated Mantle-Cell Lymphoma.J Clin Oncol . 2023 Aug 20;41(24):3988-3997. doi: 10.1200/JCO.23.00562.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言