读书报告 | 肿瘤肝转移的机制
2023-10-26 iCombo iCombo 发表于上海
肿瘤细胞和大量非癌细胞构成一个复杂生态系统嵌入改变的细胞外基质中,相互作用共同决定了肿瘤的发生发展及对其治疗的敏感性。
导读
肿瘤的发生是一个多步骤的过程,遗传学改变是肿瘤发展的基础,而肿瘤微环境是肿瘤细胞生长、扩散的重要影响因素。肿瘤细胞和大量非癌细胞构成一个复杂生态系统嵌入改变的细胞外基质中,相互作用共同决定了肿瘤的发生发展及对其治疗的敏感性。肿瘤细胞的内在特征是肿瘤塑造其微环境的关键决定因素。在综述“The evolving tumor microenvironment: From cancer initiation to metastatic outgrowth”一文中,作者详细复习了肿瘤肝转移的机制。
肝脏血管广泛分布,具有肝门静脉和肝动脉的双重血供,是恶性肿瘤最常见的转移脏器之一。肝脏炎症或纤维化诱导的特异性细胞外基质支持肝转移瘤微环境。组织驻留肝细胞、肝星状细胞、肿瘤相关巨噬细胞通过多种机制诱导利于肿瘤生长及存活的微环境,介导治疗耐药。肝转移的存在还会影响患者的全身免疫状态,导致免疫治疗耐药。针对肝脏的放疗联合免疫治疗可以恢复免疫细胞的功能,改善肝转移患者预后(Cancer Cell.2023 Mar 13;41(3):374-403. doi: 10.1016/ j.ccell. 2023.02.016)。
肿瘤发展过程中TME演变

肿瘤发生:组织内稳态被破坏
肿瘤进展:侵袭迁移,炎症催化
肿瘤转移:
转移前生态位形成
CTC在循环中生存
器官嗜性和外渗
肿瘤在转移部位休眠和生长
不同肿瘤类别、肿瘤内在特征、分期、病人状态相关的肿瘤微环境组成和功能状态可能存在巨大差异,肿瘤细胞的内在特征,包括遗传改变、表观遗传改变、代谢重编程和信号释放,是肿瘤塑造其微环境的关键决定因素。
转移前生态位关键特征:血管通透性增加、ECM 重塑、成纤维细胞和上皮细胞等常驻细胞改变、骨髓来源免疫细胞的调动和免疫抑制
肝转移瘤微环境
肝窦内皮细胞
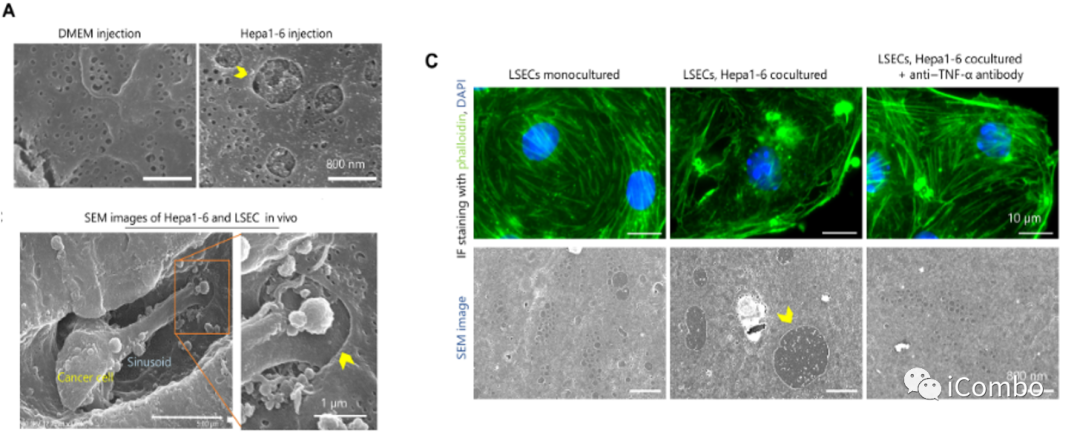
肝脏血管广泛分布,肝门静脉和肝动脉的双重血液供应。
癌细胞通过促炎性旁分泌机制形成肝窦内皮细胞间隙(LSEC iGap),促进CTC外渗。
肝毒素损伤和纤维化可导致LSECs iGap的形成。
器官特异性细胞外基质(ECM)支持转移瘤微环境
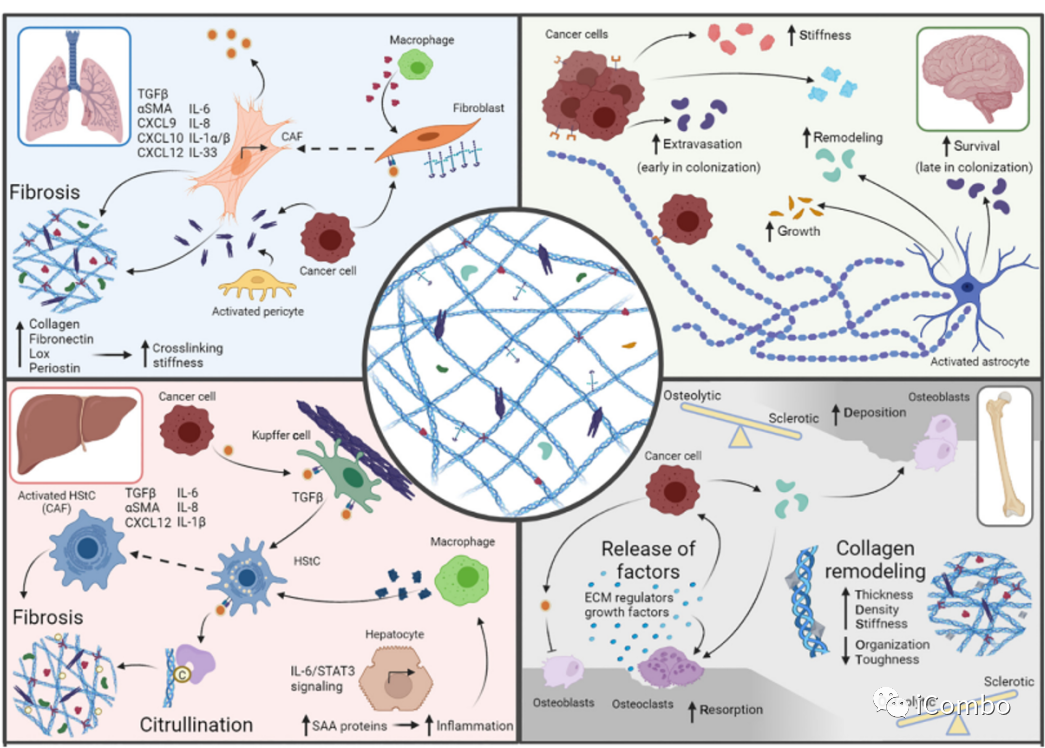
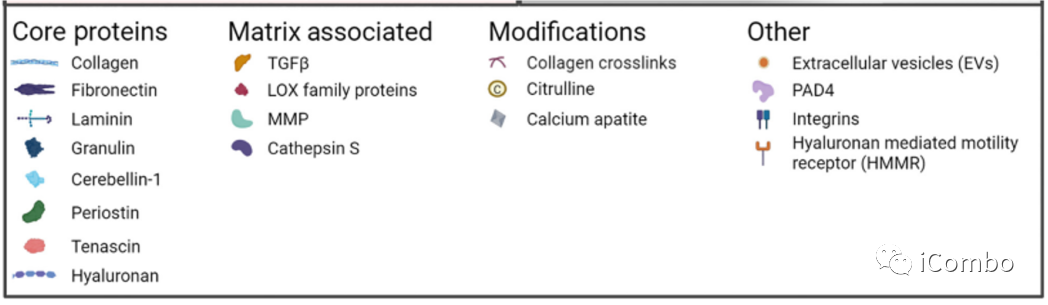
Immune cells play a significant role in profibrotic changes in the liver metastatic niches.(巨噬细胞,以及固有的成纤维细胞)
组织驻留肝细胞
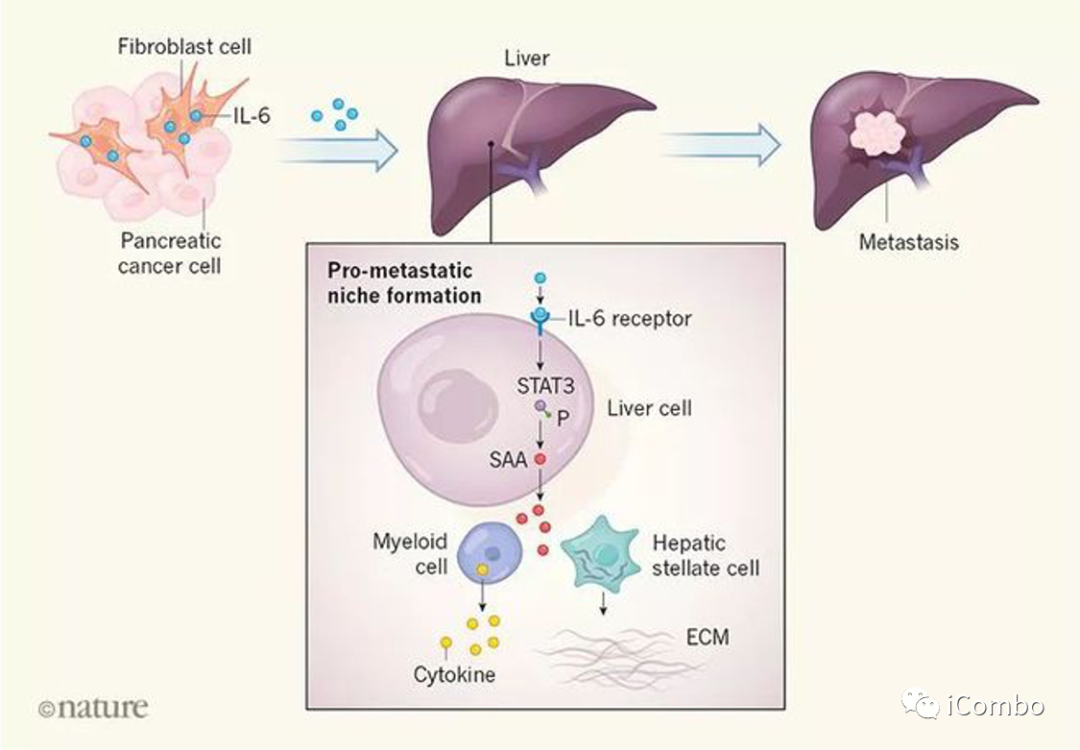
Hepatocytes direct the formation of a pro-metastatic niche in the liver
肝细胞通过IL-6-STAT3信号激活,血清淀粉样蛋白A(SAA)的产生,导致纤维化和免疫微环境的改变。
肝星状细胞(HSC)
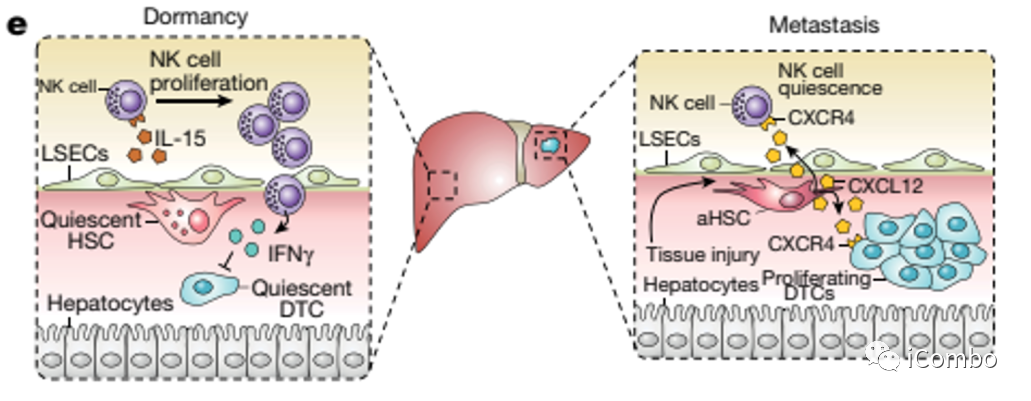
NK细胞和激活的肝星状细胞之间的相互作用是调节肿瘤细胞休眠与否的关键开关。
在肿瘤细胞休眠的微环境中,NK细胞通过干扰素-γ信号维持肿瘤细胞的休眠;
而激活的肝星状细胞能够分泌趋化因子CXCL12使NK细胞失能,促进休眠的肿瘤细胞苏醒。
肝转移瘤巨噬细胞介导T细胞凋亡
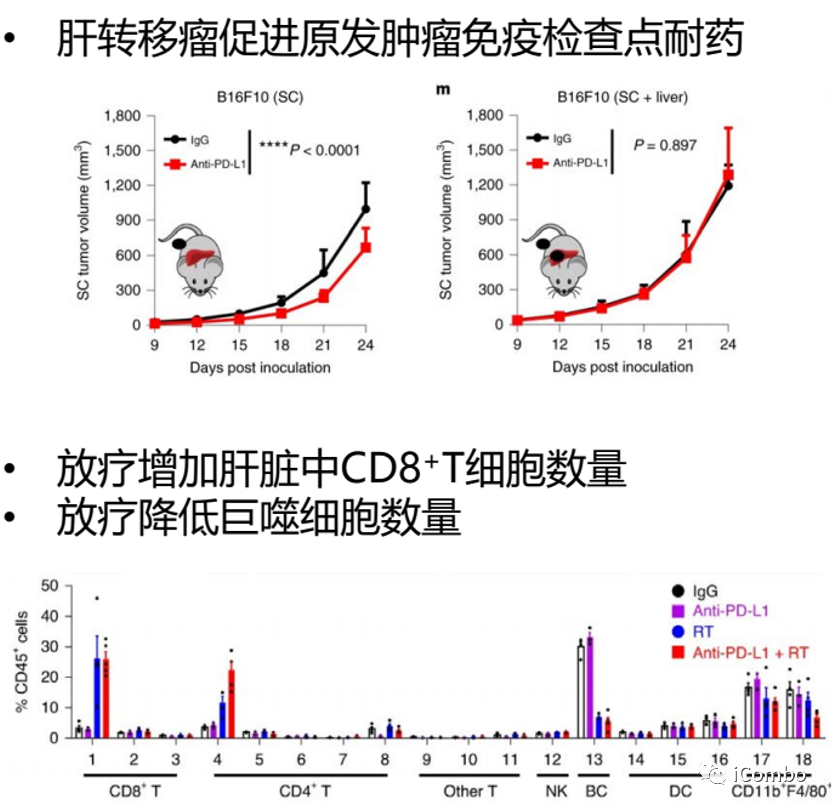
炎症巨噬细胞数量显著上升

肝转移对全身肿瘤免疫循环的影响

肝转移瘤利用宿主外周免疫耐受机制,通过CD8+ T细胞缺失引起获得性免疫治疗耐药。
肝脏放射疗法结合免疫治疗可以恢复免疫细胞的功能,改善癌症转移患者的预后。
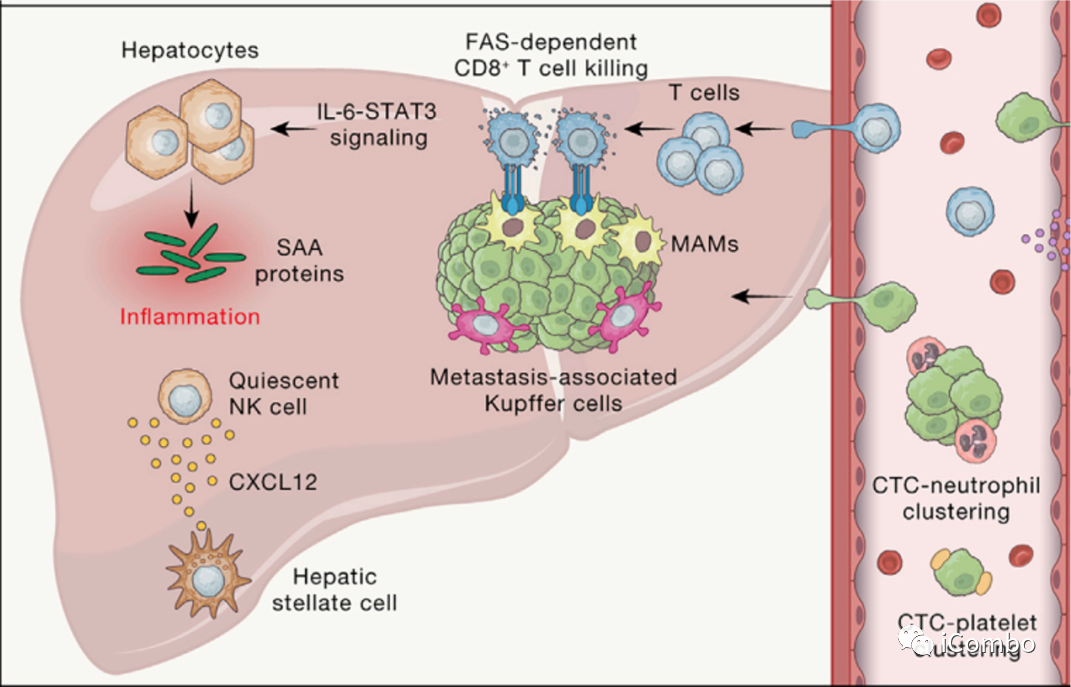
肝转移瘤微环境与转移肿瘤细胞命运
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








