读书报告 | 立体定向放射治疗加或不加免疫治疗对早期或孤立性肺实质复发淋巴结阴性的非小细胞肺癌的一项开放标签、随机、2期试验
2023-11-01 iCombo iCombo 发表于上海
本研究是一个开放标签,随机II临床试验,在MD安德森综合网络内的美国德克萨斯州的三家不同医院进行。
导读
肺癌是我国发病率和死亡率最高的恶性肿瘤,每年新发肺癌病例近80万例,因肺癌死亡高达60余万例,其中约80%为非小细胞肺癌(NSCLC)。对于可手术的早期NSCLC,标准治疗模式为根治性手术,而SABR对于IA期(<3cm)患者已经可实现与可手术相似的总生存率,且毒性显著降低;对于不可手术或拒绝手术的患者,SABR为标准治疗模式,2年局部控制率为80%-97%。尽管SABR后照射野的可以得到满意的局部控制率,但仍有较高的照射野外的复发率(5年11-13%)或远处转移率(5年11-20%),同时联合化疗并未显著改善患者的RFS和OS。
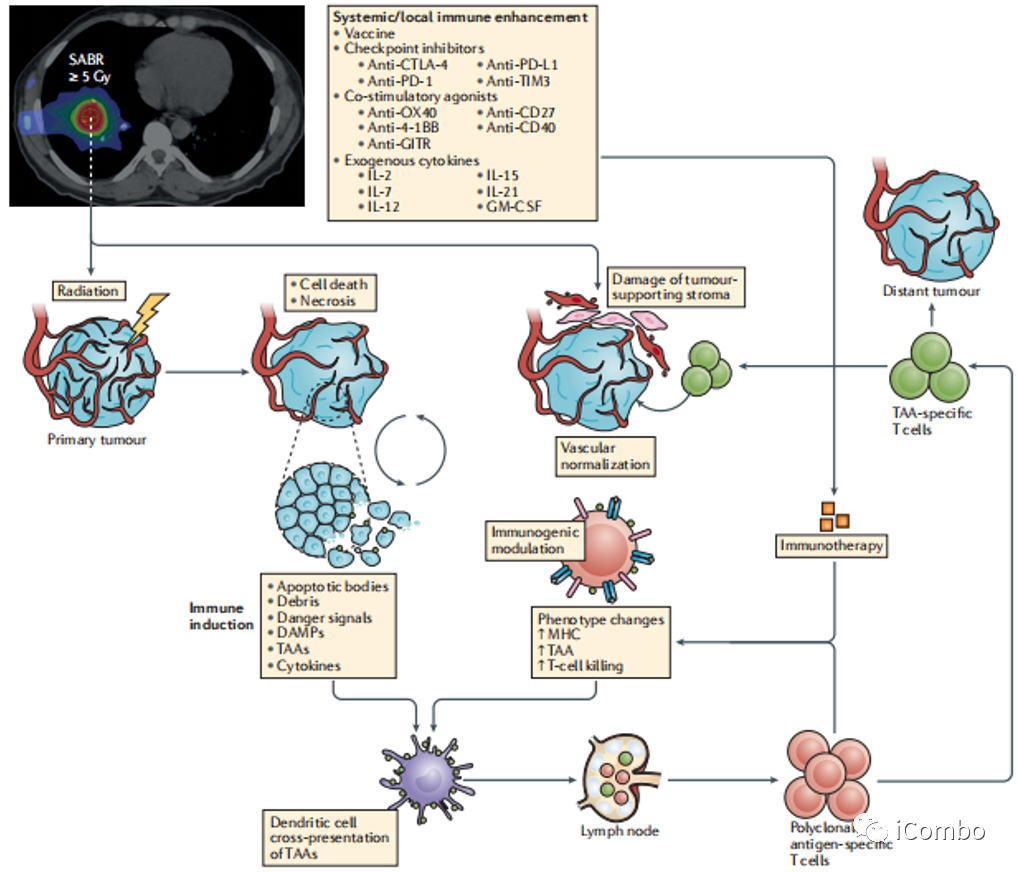
目前的研究表明放射治疗和免疫治疗可能具有协同效应,特别是以高BED(≥100Gy)低分割次数(1~10f)给予时。SABR可能通过促进肿瘤相关抗原的释放、增加PD-L1的表达、激活肿瘤特异性T淋巴细胞以增强局部抗肿瘤效应以及更好地消除微转移灶,将肿瘤本身转化为原位疫苗。
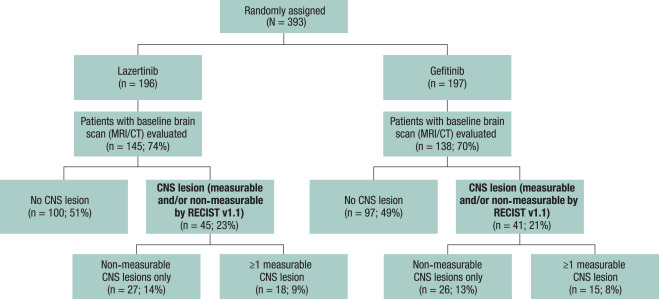
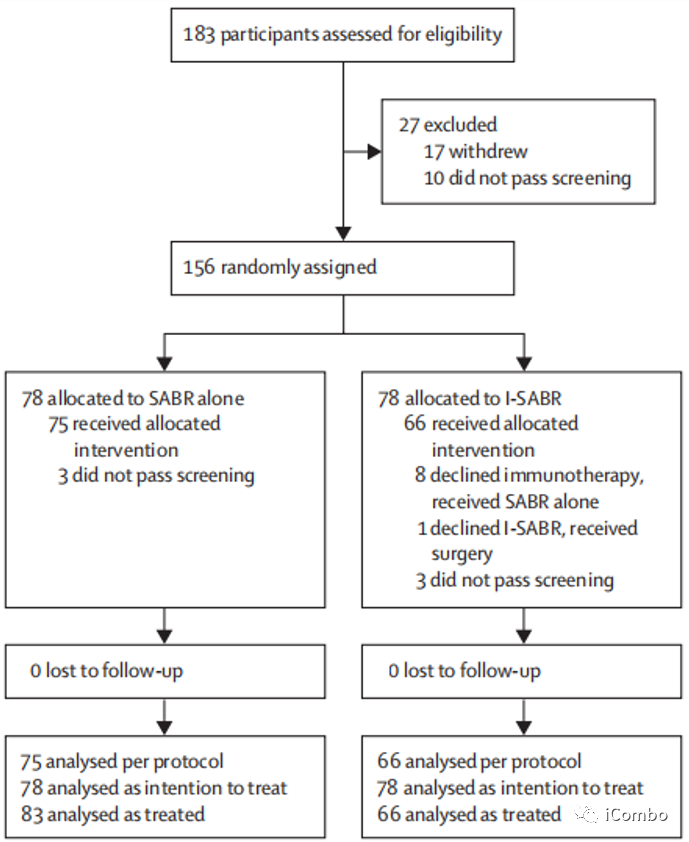
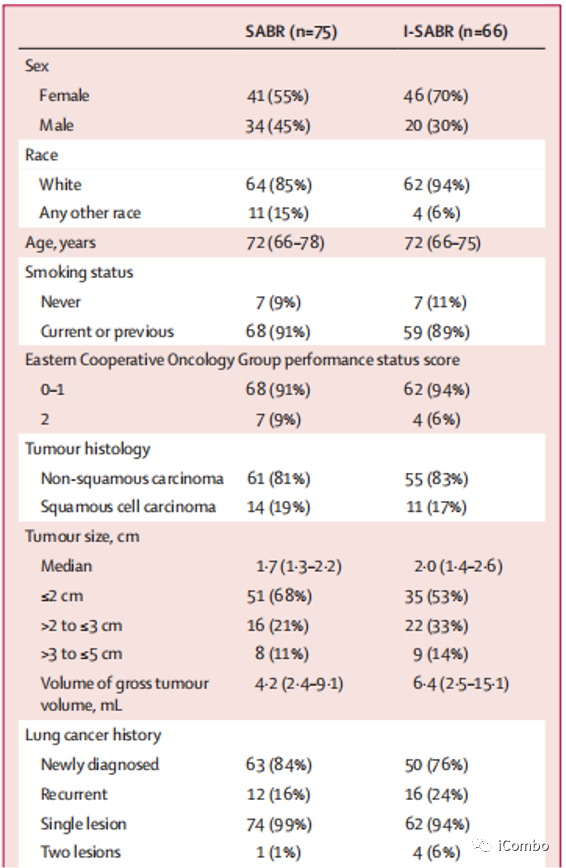
研究设计:本研究是一个开放标签,随机II临床试验,在MD安德森综合网络内的美国德克萨斯州的三家不同医院进行。主要入组标准:年龄≥18岁、ECOG评分0-2,不能或不愿接受手术的早期NSCLC患者[AJCC 8th,IA-IB期(≤4cm,N 0 M0)、IIA期(≤5cm,N 0 M0)或IIB期(>5cm且≤7cm,N 0 M0)]或孤立复发患者(≤7cm)。治疗方案:I-SABR组:Nivo首剂480mg与SABR同步或放疗后36h内,此后240mg q2w,7cycle;SABR处方剂量为50Gy-80Gy(满足剂量体积限制)。主要观察指标:4年EFS,EFS事件定义为:疾病复发、远处转移、第二原发性肺癌或死亡。随访:前2年每3个月一次CT/PET-CT,3-5年每6个月一次CT/PET-CT,之后每年一次;
结果:I-SABR组4年EFS为77%,SABR组4年EFS为53%。从I-SABR治疗中显著获益的主要是原发肿瘤≤2cm及初治的患者,且I-SABR组15例PD-L1阳性患者中无一复发,但PD-L1阴性患者也有显著EFS获益(HR=0.27)。即使PD-L1表达小于1%的患者也能从I-SABR中获益。并且似乎获益更多,而作者在这里的解释是SABR可诱导某些人群中的PD-L1表达,从而使PD-1抗体+SABR联合治疗促进某些PD-L1原本阴性的患者获益。
安全性方面,I-SABR组有10例(15%)患者报告3级不良事件,均与免疫治疗有关,但患者均能从不良事件中恢复,减停免疫治疗的比例也较低,SABR组治疗则整体安全。而免疫治疗与放疗联合使用时,常常被顾虑的肺炎副反应发生率并未显著升高,I-SABR组仅报告2例可能与治疗有关的2级肺炎。
结论:相对于既往的Impower010、Keynote-091、CheckMate 816和PACIFIC 等临床试验,I-SABR方案取得优异的EFS结果的可能因素为:① 由SABR产生的强烈免疫刺激;② 相对于常规放疗,SABR可以最大限度地减少淋巴细胞减少;③ 照射较小的靶区范围,尤其是避免照射淋巴结,避免了淋巴细胞的损失;④ SABR与ICIs的同步给药。对于初治的早期或孤立的实质复发性淋巴结阴性NSCLC患者,I-SABR显著改善了无事件生存期,可能是此类患者的治疗选择之一(Lancet. 2023 Jul 18;S0140-6736(23)01384-3. doi: 10.1016/S0140-6736(23)01384-3)。
背景
1、肺癌已成为我国发病率和死亡率最高的恶性肿瘤,每年新发肺癌病例近80万例,因肺癌死亡高达60余万例,其中约80%为非小细胞肺癌(non-small cell lung cancer, NSCLC);
2、对于可手术的早期NSCLC,标准治疗模式为根治性手术,而SABR对于IA期(<3cm)患者已经可实现与可手术相似的总生存率,且毒性显著降低;对于不可手术或拒绝手术的患者,SABR为标准治疗模式,2年局部控制率为80%-97%;
3、尽管SABR后照射野的可以得到满意的局部控制率,但仍有较高的照射野外的复发(5年11-13%)或远处(5年11-20%)转移,同时联合化疗并未显著改善RFS和OS;

-
SABR:高生物效应剂量BED(≥100Gy)低分割次数(1~10f)
-
4R(肿瘤细胞再修复、肿瘤细胞再氧合、肿瘤细胞再群体化、肿瘤细胞周期再分布)+内皮损伤+血管阻塞+免疫激活
研究设计
开放标签,随机II临床试验,在MD安德森综合网络内的美国德克萨斯州的三家不同医院进行
主要入组标准:年龄≥ 18岁、ECOG评分0-2,不能或不愿接受手术的早期NSCLC患者[AJCC 8th,IA-IB期(≤4cm,N 0 M0)、IIA期(≤5cm,N 0 M0)或IIB期(>5cm且≤7cm,N 0 M0)]或孤立复发患者(≤7cm)
主要排除标准:肿瘤> 7cm、超中央型病灶(主支气管、食管、心脏、大血管和臂丛神经 0.5cm范围内)、既往接受过ICIs、存在淋巴结或远处转移、6个月内的全身治疗、不符合SABR剂量体积限制最低要求以及存在免疫治疗相关禁忌症
I-SABR组:Nivo首剂480mg与SABR同步或放疗后36h内,此后240mg q2w,7cycle
SABR处方剂量为50Gy-80Gy(满足剂量体积限制)
随访:前2年每3个月一次CT/PET-CT,3-5年每6个月一次CT/PET-CT,之后每年一次;
主要观察指标:4年EFS,EFS事件定义为:疾病复发、远处转移、第二原发性肺癌或死亡。
结果
结果——EFS
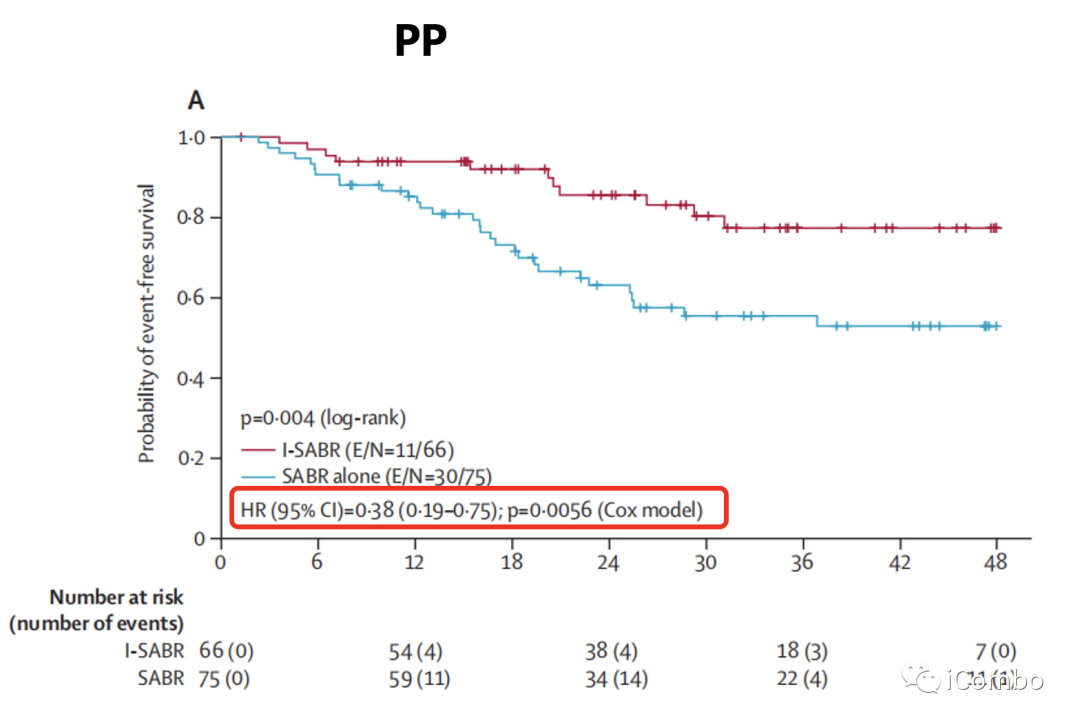
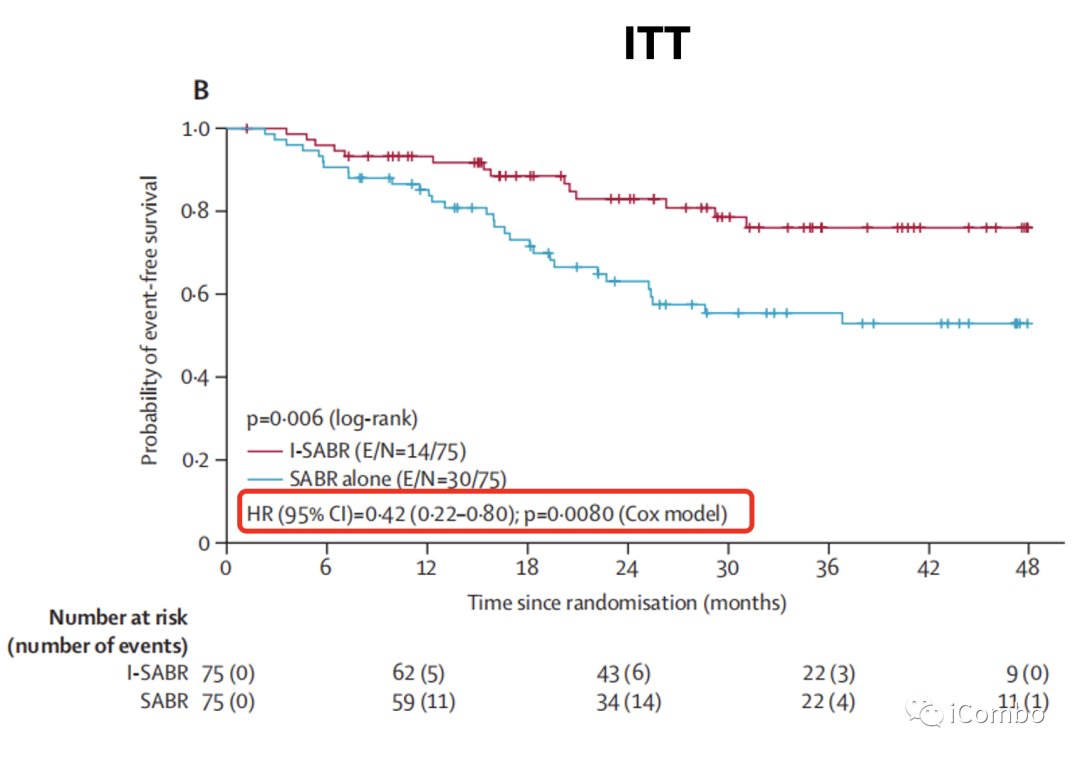
4year EFS:77%(I-SABR组)VS 53%(SABR组)
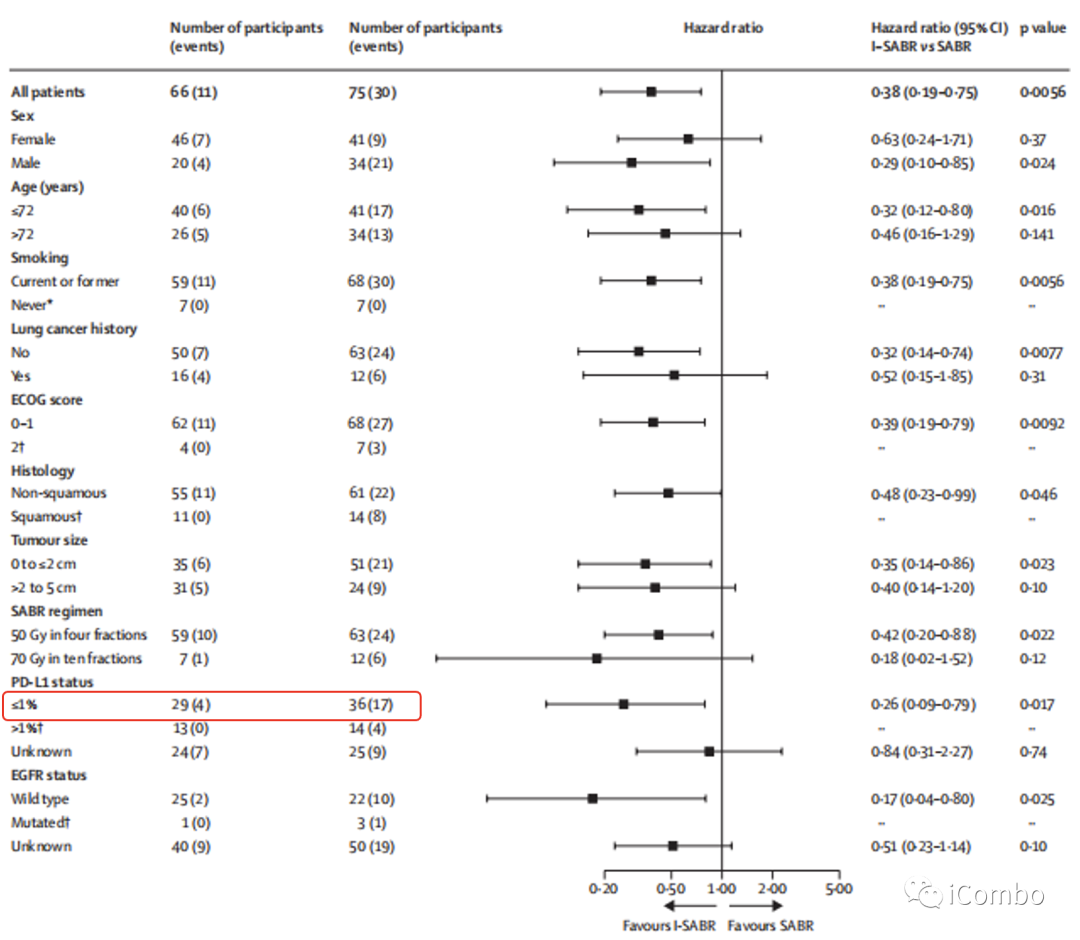
从I-SABR治疗中显著获益的,主要是原发肿瘤≤2cm及初治的患者,且I-SABR组15例PD-L1阳性患者中无一复发,但PD-L1阴性患者也有显著EFS获益(HR=0.27)。
结果——不良反应
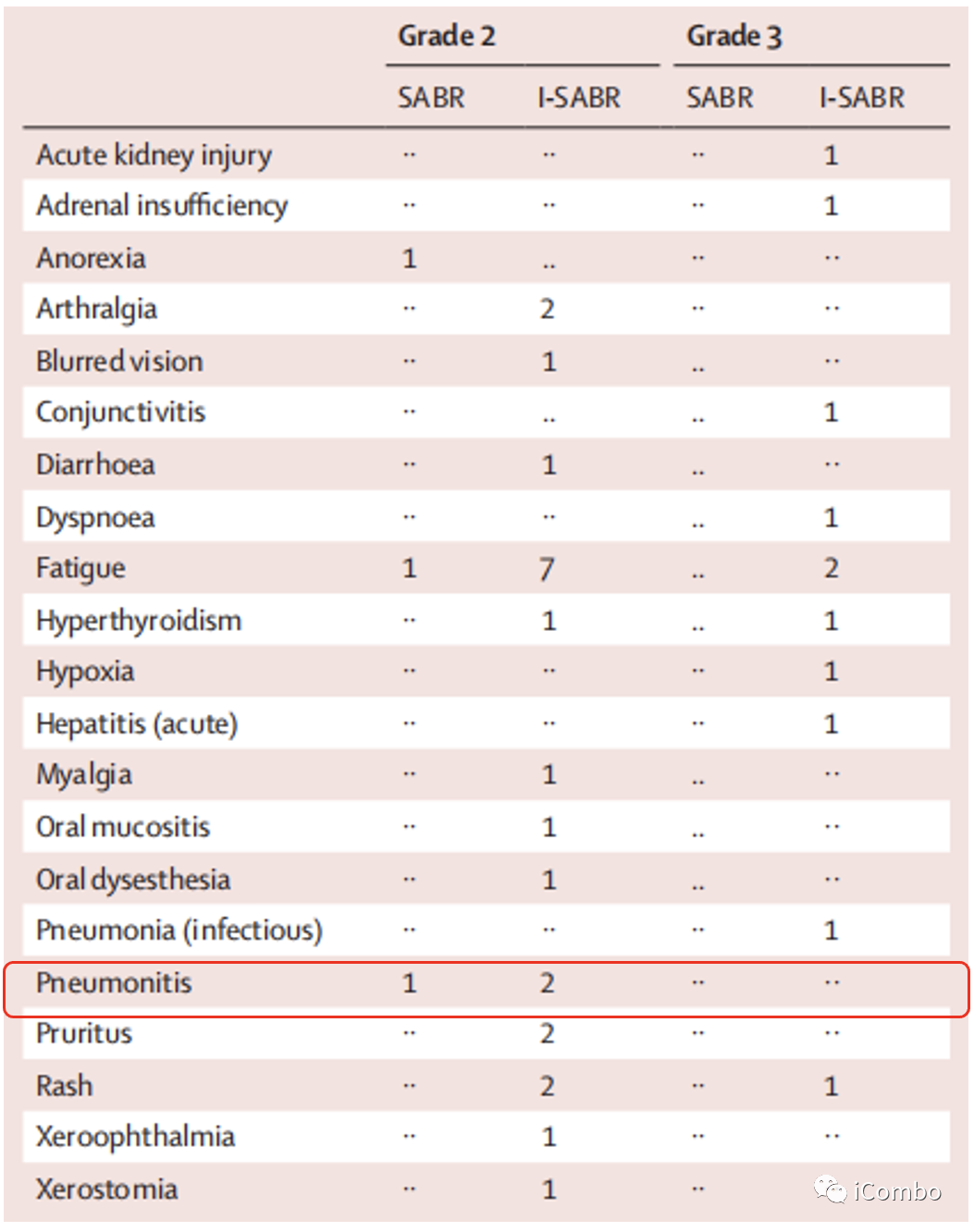
I-SABR组有10例(15%)患者报告3级不良事件。
小结
1、相对于既往的Impower010、Keynote-091、CheckMate 816和PACIFIC 等临床试验,I-SABR方案取得优异的EFS结果的可能因素为:① 由SABR产生的强烈免疫刺激;② 相对于常规放疗,SABR可以最大限度地减少淋巴细胞减少;③ 照射较小的靶区范围,尤其是避免照射淋巴结,避免了淋巴细胞的损失;④ SABR与ICIs的同步给药;
2、样本量较小,因此在亚组分析肿瘤大小、既往治疗、多发性病变、组织病理和对EGFR突变或其他致癌驱动因素方面把握度不足;
3、对于初治的早期或孤立的实质复发性淋巴结阴性NSCLC患者,I-SABR显著改善了无事件生存期,可能是此类患者的治疗选择。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言