Cell Reports Medicine | 普特利单抗治疗晚期错配修复缺陷或微卫星不稳定性高实体瘤患者:一项多中心 2 期研究
2024-02-22 daikun MedSci原创 发表于上海
该研究旨在评估普特利单抗在经治的晚期dMMR/MSI-H实体瘤患者中的疗效和安全性,普特利单抗在经治的晚期dMMR/MSI-H实体瘤患者中表现出持久的抗肿瘤活性和可管理的毒性。
dMMR/MSI-H肿瘤发生率约为所有诊断癌症的2-4%,在子宫内膜癌、胃癌和结直肠癌等类型中更为常见,这类肿瘤具有高突变负荷、表达新抗原和增加淋巴细胞浸润等免疫原性特征。抗PD-1抗体在dMMR/MSI-H肿瘤治疗中展现出活性,部分药物如帕博利珠单抗和纳武利尤单抗已被批准用于治疗,普特利单抗是一种抗PD-1单克隆抗体,前期研究表明其对实体瘤患者具有潜在抗肿瘤活性和可管理的安全性,该研究旨在评估普特利单抗在经治的晚期dMMR/MSI-H实体瘤患者中的疗效和安全性,并探索潜在预测疗效的生物标志物。

方法
这是一项多中心、开放标签、单臂的II期临床试验,纳入的患者年龄≥18岁,经组织学确诊为晚期dMMR/MSI-H实体瘤,经治且至少接受过一线系统性治疗,ECOG评分0-1分,至少有一个可测量病灶,器官和造血功能良好,过去5年有第二原发癌,有症状的脑转移,既往接受过免疫检查点抑制剂治疗,有活动性自身免疫病或严重感染等。符合条件的患者接受静脉注射普特利单抗 200mg,每3周1次,直至疾病进展或出现不可接受的毒性。主要终点为IRC评估的ORR,次要终点包括安全性、研究者评估的ORR、疾病控制率、响应持续时间、无进展生存期和总生存期。
人群和基线特征
该研究共纳入100例患者,中位年龄53岁,男性54例,最常见的肿瘤类型为结直肠癌(71例)、胃癌(10例)和子宫内膜癌(7例),98例患者有远处转移,2例为局部晚期;所有患者均接受过系统性治疗,其中44例接受过至少两线治疗;97例因疾病进展入组,3例因化疗不耐受入组,81例为dMMR和MSI-H,12例仅dMMR,7例仅MSI-H;27例经基因测序确诊为林奇综合征,71例结直肠癌患者中,30例接受过氟尿嘧啶、奥沙利铂和伊立替康治疗,25例接受过贝伐珠单抗治疗,7例接受过西妥昔单抗治疗,6例接受过多靶点血管内皮生长因子受体抑制剂治疗,所有10例胃癌患者均为HER2阴性。
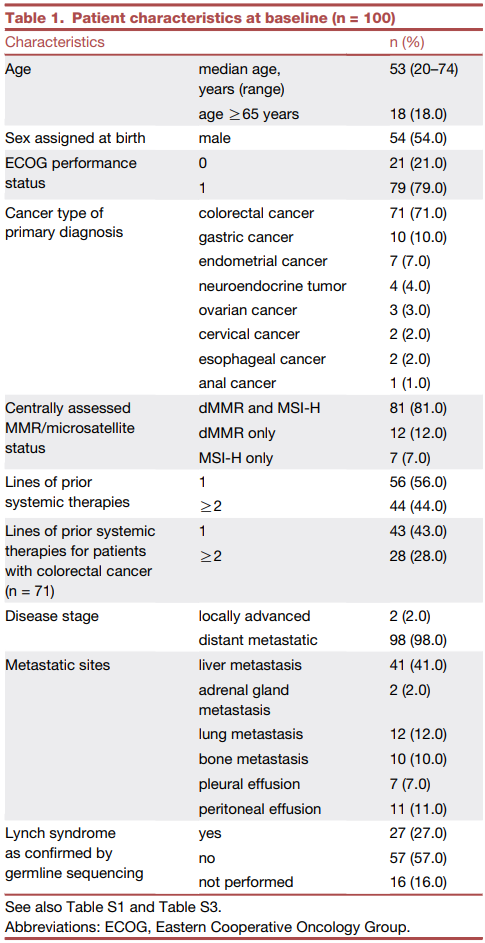
研究结果
ORR:根据独立审查委员会(IRC)评估,100例患者中,ORR为49.0%,中位PFS和OS未达到,12个月PFS率为56.1%,24个月OS率为68.9%,在71例晚期结直肠癌患者中,ORR为56.3%。生物标志物分析:PD-L1表达与疗效无关;NLR<4的患者疗效更好;KMT2D突变与更好的疗效相关;高肿瘤突变负荷(TMB)与更好的疗效相关;HLA-I基因型与疗效无关。

安全性
100例患者中,83%出现治疗相关不良反应(TRAEs),18%出现3级及以上TRAEs,最常见的不良反应包括AST/ALT升高、贫血、甲状腺功能减退等,5%的患者出现治疗相关严重不良反应(SAEs),4%因TRAEs而停药,最常见严重不良反应包括贫血、白细胞减少和高血压,29%的患者出现免疫相关不良反应(irAEs),3%出现免疫相关严重不良反应,最常见irAEs为甲状腺功能减退、甲状腺功能亢进和甲状腺功能异常,其中,1例因免疫相关心肌炎和疾病进展而死亡。
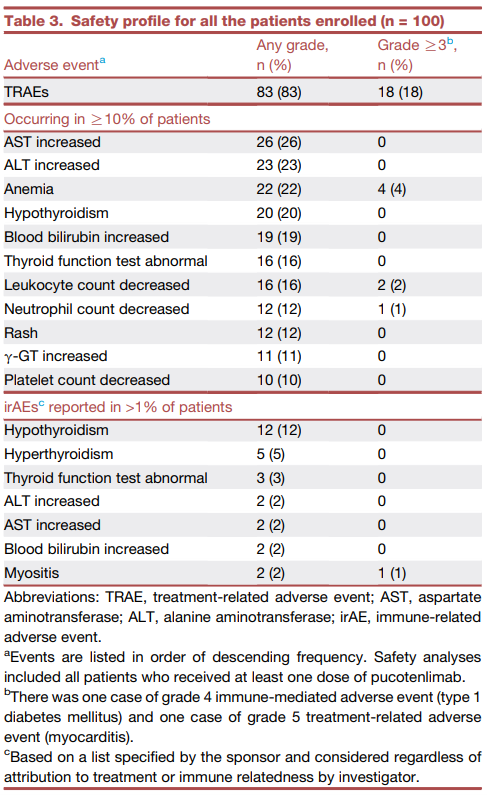
结论
普特利单抗在经治的晚期dMMR/MSI-H实体瘤患者中表现出持久的抗肿瘤活性和可管理的毒性,支持在dMMR/MSI-H肿瘤患者中使用,KMT2D突变可能成为dMMR/MSI-H肿瘤患者中预测PD-1抑制剂疗效的生物标志物,此外,治疗后的NLR变化与疗效相关,同时KMT2D突变、高TMB和NLR变化可能是预测疗效的生物标志物。
原始出处
Zhang B, et al. 2023. Pucotenlimab in patients with advanced mismatch repair-deficient or microsatellite instability-high solid tumors: A multicenter phase 2 study. Cell Reports Medicine 4:101301.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








