PNAS:南方医科大学黎孟枫/中山大学蔡俊超合作揭示ATOH8结合SMAD3诱导细胞衰老并阻止Ras驱动的恶性转化
2023-01-16 iNature iNature 发表于威斯康星
癌基因诱导衰老(OIS)的发生过程以及OIS与恶性转化之间的关系尚不清楚。
癌基因诱导衰老(OIS)的发生过程以及OIS与恶性转化之间的关系尚不清楚。
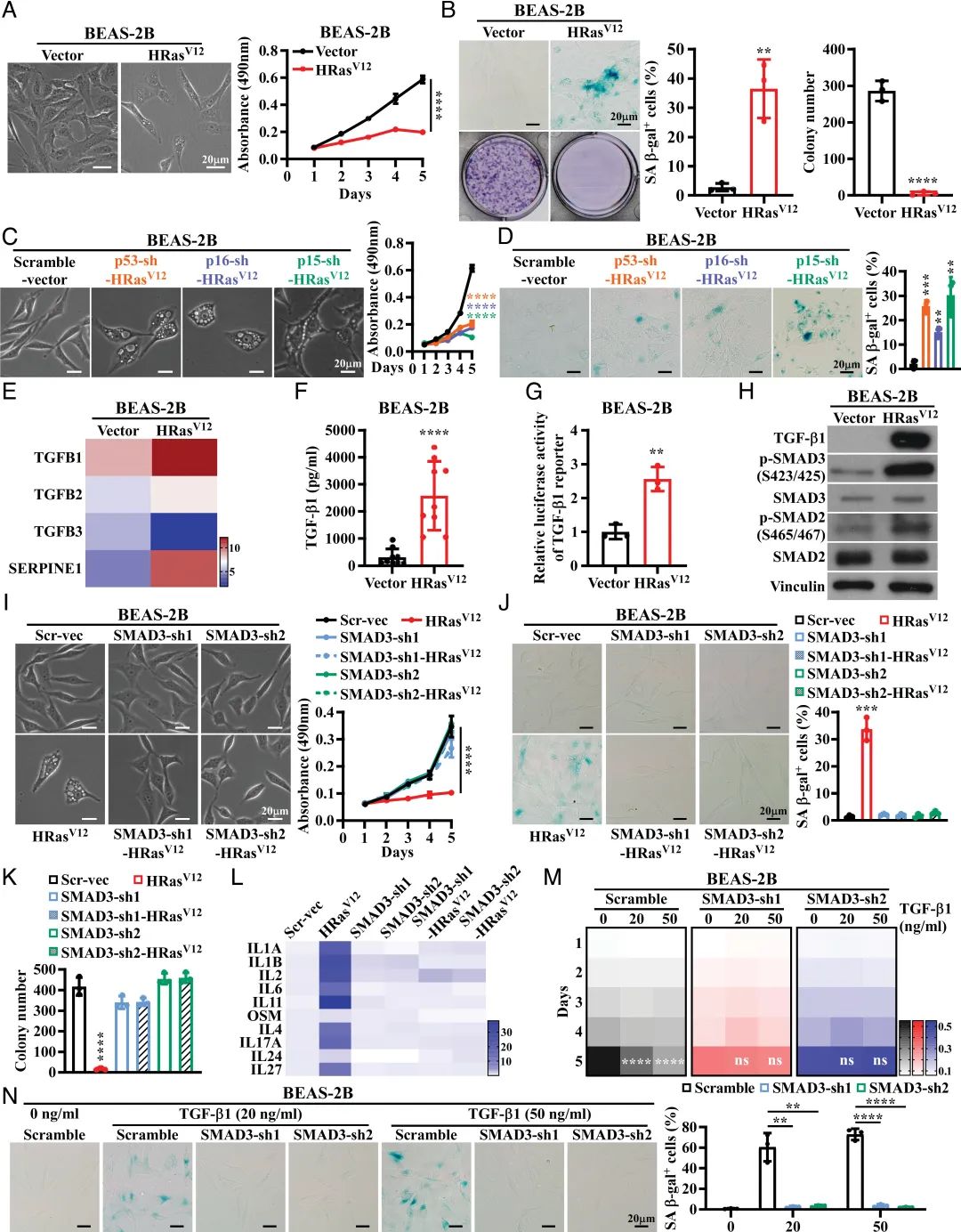
2023年1月10日,南方医科大学黎孟枫及中山大学蔡俊超共同通讯在PNAS 上在线发表题为“ATOH8 binds SMAD3 to induce cellular senescence and prevent Ras-driven malignant transformation”的研究论文,该研究发现在肺上皮细胞中癌基因Ras过度激活后,高水平的转化生长因子β 1 ( transforming growth factorβ1,TGF-β1 )激活的SMAD3,而不是SMAD2或SMAD4,在诱导细胞衰老中起着不依赖于p53/p16/p15衰老通路的决定性作用。重要的是,SMAD3与潜在的肿瘤抑制因子ATOH8结合形成转录复合物,直接抑制一系列细胞周期促进基因,从而导致肺上皮细胞衰老。
有趣的是,衰老的SMAD3转化为致癌物质,本质上促进了致癌Ras驱动的恶性转化。此外,敲除Atoh8会迅速加速致癌Ras驱动的肺癌发生,并且由突变Ras和Atoh8缺失驱动的肺癌对特异性SMAD3抑制剂的治疗敏感,而不是由突变Ras驱动的肺癌。此外,在大约12 %的临床肺癌病例中可以发现ATOH8基因的高甲基化。总之,该发现不仅证明了上皮细胞衰老是由一个潜在的肿瘤抑制因子控制的转录程序指导的,而且证明了TGF-β/SMAD3的促衰老和转化作用之间的重要相互作用,为开发早期检测和抗癌策略奠定了基础。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







